1��ѡ���� �������ӷ���ʽ��д��ȷ���ǣ�������
A����FeBr2��Һ��ͨ������������2Fe2++4Br-+3Cl2=2Fe3++2Br2+6Cl-
B����CaCl2��Һ��ͨ�������̼���壺Ca2++CO2+H2O=CaCO3+2H+
C����ˮ�м���ϡ���H++OH-=H2O
D��������п����Ӧ��2H++Zn2+=H2��+Zn
�ο��𰸣�A����FeBr2��Һ��ͨ�����������������ܽ��������Ӻ�������ȫ�������������������Ӻ������ӵ����ʵ���֮��Ϊ1��2���з�Ӧ����A��ȷ��
B����CaCl2��Һ��ͨ�������̼���岻������Ӧ��������ֳ�������B����
C����ˮ��������ʣ�������������ӷ�Ӧ�в��ܲ�����ӵ���ʽ����C����
D�����������ᣬ��������ʣ�������������ӷ�Ӧ�в��ܲ�����ӵ���ʽ����D����
��ѡA��
���������
�����Ѷȣ���
2������� ��14�֣���BaCl2��Һ�ֱ���뵽K2SO4��ϡH2SO4��Һ�У����а�ɫ�������������ǵ����ӷ���ʽ��?��˵�����ӷ���ʽ������ʾһ�����ʼ�����?�����ұ�ʾ��?���ӷ�Ӧ����CuSO4��Һ�еμ�NaOH��Һ����Һ��?���ӵ���Ŀ���٣�?���ӵ���Ŀ���ӣ�?���ӵ���Ŀû�б仯����Ӧ�����ӷ���ʽ��?��
�ο��𰸣���14�֣�Ba2++ SO42-�� BaSO4 �� ��?��ѧ��Ӧ��ͬһ���͵�?��
___Cu2+_��___Na+__?��? SO42-__�� __? _Cu2+ +? 2OH-_ ��? Cu(OH)2
�����������
�����Ѷȣ�һ��
3��ѡ���� ���б�ʾ��Ӧ��ѧ��Ӧ�����ӷ���ʽ��ȷ���ǣ�?��
A������Fe2O3����Һ��ͨ��HI�� Fe2O3 + 6H��= 2Fe3�� + 3H2O
B����1 mol/L NaAlO2��Һ��1.5 mol/L HCl��Һ�����������Ȼ�ϣ�
6AlO2��+9H��+3H2O��5Al(OH)3��+Al3��
C��������Һ��ˮ���е�CaCO3��Ӧ��CaCO3��2H����Ca2����H2O��CO2��
D��Ba��OH��2��Һ�е���NaHSO4��Һ����ȫBa2+������2H++ SO42-+Ba2++2OH��=BaSO4��+2H2O
�ο��𰸣�B
��������������Ӿ��������ԣ������Ӿ��л�ԭ�ԣ�A�з���������ԭ��Ӧ���ɵ��ʵ���������ӣ�A����ȷ��B��ƫ�����ƺ���������ʵ���֮����2:3���������ɵ������������Ȼ��������ʵ���֮����5:3����ѡ��B��ȷ������ʱ���ᣬӦ���л�ѧʽ��ʾ��C����ȷ��D����ȷ��Ӧ����H++ SO42-+Ba2++OH��=BaSO4��+H2O����ѡB��
�����������Ǹ߿��еĸ�Ƶ�⣬�����е��Ѷȵ����⣬���ض�ѧ��������������ѵ����������Ҫ��ȷ�ж����ӷ���ʽ��ȷ���ķ���һ�㣬����1����鷴Ӧ�ܷ�������2����鷴Ӧ��������Ƿ���ȷ����3���������ʲ���Ƿ���ȷ����4������Ƿ�����غ��ϵ���磺�����غ�͵���غ�ȣ�����5������Ƿ����ԭ��ѧ����ʽ��Ȼ��������ü��ɡ���������������ѧ���������⡢��������������
�����Ѷȣ���
4��ѡ���� �������ӷ���ʽ��ȷ����?��?��
A�����������Ũ���ᷴӦ��2 MnO4- + 10 Cl- + 16 H+ =" 2" Mn2+ + 5 Cl2�� + 8 H2O
B����״��112 mLCl2ͨ��10 mL 1mol/LFeBr2��Һ��2Fe2++4Br-+3Cl2=2Fe3++6Cl-+2Br2
C��Ũ�����KClO3��Ӧ��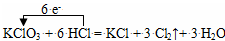
D����������ˮ�Լ��ԣ�S2- + 2H2O = H2S + 2OH-
�ο��𰸣�A
���������
��ȷ�𰸣�A
B������ȷ��Cl2Ϊ0.005mol,FeBr20.04mol,Cl2ֻ����Fe2����Ӧ��Cl2��2Fe2��=2Fe3����2Cl�D
C������ȷ������ת����Ϊ5e-
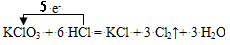
D������ȷ����������ˮ�ֲ�ˮ�⣺S2�D��H2O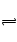 HS�D��OH�D
HS�D��OH�D
�����Ѷȣ�һ��
5��ѡ���� �������ӷ���ʽ��д������ǣ�?��
A����������ϡH2SO4��Ӧ��2H�� + FeS �� H2S��+ Fe2��
B��̼��������Һ�м���ϡ���HCO3�� + H���� CO2��+ H2O
C��NaHSO3��Һ��NaHSO4��Һ��ϣ�HSO3��+ H��= H2O + SO2��
D�����������Һ��ͨ��������������Ӧ��Ca2��+ 2ClO��+ H2O + SO2��CaSO3��+ 2HClO
�ο��𰸣�D
����������������ξ��������ԣ��ܰ�SO2�����������ᣬ����ѡ��D�е�������Ӧ�����Ȼ��ƺ����ᣬ��˴�ѡD��
�����Ѷȣ�һ��