1������� ��A��B��C��D����Ԫ�أ�AԪ�غ�BԪ�ص�ԭ�Ӷ���1��δ�ɶԵ��ӣ�A+��B-��һ�����Ӳ㣬Bԭ�ӵ�һ����������3p�����3p����ѳ�����Cԭ�ӵ�p�������3��δ�ɶԵ��ӣ�����̬�⻯����ˮ�е��ܽ����ͬ��Ԫ�����γɵ��⻯�������D������ϼۺ���ͻ��ϼ۵Ĵ�����Ϊ4��������������к�D��������Ϊ40%���������������������������R����A��D��Ԫ���γɵ����ӻ��������A+��D2-������֮��Ϊ2:1����ش��������⣺
(1)AԪ���γɵľ�������____���壬���۷е��ͬ���ڵĽ���Ԫ�ص��ʵ�Ҫ�ͣ�������Ϊ___________��
(2)B-�ĵ����Ų�ʽΪ______����CB3������CԪ��ԭ�ӵ�ԭ�ӹ����������____�ӻ���
(3)C���⻯��Ŀռ乹��Ϊ________________��
(4)BԪ�صĵ縺��____DԪ�صĵ縺�ԣ��>������<����=��������һ����ѧ����ʽ˵��B��D��Ԫ���γɵĵ��ʵ�������ǿ����__________________��
�ο��𰸣�(1)��������Ϊ����ͬ�����е�ԭ�Ӱ뾶��λ����ڵ����ɵ�����Ŀ�٣����Խ����������۷е��
(2)1s22s22p63s23p6��sp3
(3)������
(4)>��H2S+Cl2=2HCl+S��
���������
�����Ѷȣ�һ��
2��ѡ���� �ڽ��ʯ�ľ����У������ɹ��ۼ��γɵ�̼ԭ�ӻ���������С�Ļ�������̼ԭ������ÿ��̼ԭ������������C--C����ļн���(? )
A��6��120��
B��5��108��
C��4��109��28��
D��6��109��28��
�ο��𰸣�D
������������ݽ��ʯ�ľ���ṹ�ص��֪����С�Ļ�����6��̼ԭ�ӡ�����ÿ��̼ԭ�Ӷ����γɸ���ͬ�Ĺ��ۼ������Ի����������������壬������109��28�䣬��ѡD��
�����������ǻ���������Ŀ��飬��Ҫ�ǿ���ѧ���Խ̲��н��ʯ����ṹ����Ϥ�˽�̶ȣ����ڵ���ѧ����ѧϰ��Ȥ������ѧ����ѧϰ�����Ժ�ѧϰЧ�ʡ������ѶȲ���ס���ɡ�
�����Ѷȣ���
3������� ������Ԫ��A��B��C��D�����ڱ��е�λ������ͼ��ʾ���ش��������⣺
��1����A��B��C��D����Ԫ�ص�ԭ������֮��ΪM����M____________��
A����Ϊ����?B����Ϊż��?C������Ϊ������Ҳ����Ϊż��
 ��2����D�ǵؿ��к���λ�ӵڶ���Ԫ�أ��䵥��������̫���ܵ�ذ�Ĺؼ����ϣ��������������ݴ��䷽�湱��ͻ������
��2����D�ǵؿ��к���λ�ӵڶ���Ԫ�أ��䵥��������̫���ܵ�ذ�Ĺؼ����ϣ��������������ݴ��䷽�湱��ͻ������
��D��Ԫ�ط���Ϊ____________��
��B�γɵ�һ�ֵ��ʷ��ӣ��ף����Ժͼء����ӡ�
��һ��������������ң��侧������ͼ��ʾ����þ�
���м��Ӻͼ�ԭ�ӵĸ�����Ϊ?��
��3����DԪ��ԭ�ӵĴ��������������������������֮�ͣ���
���õ���ʽ��ʾDԪ���⻯����γɹ���?��?
�ڹ���AԪ�ص��⻯����DԪ������������Ӧˮ���ﷴӦ���ɻ�����Z���� Z��ˮ��Һ���������ӵ�Ũ���ɴ�С��˳��Ϊ?��
Z��ˮ��Һ���������ӵ�Ũ���ɴ�С��˳��Ϊ?��
��������ijԪ�ص��⻯��X����һԪ�ص�������Y��Ӧ��������һ��ǿ�ᣬ��X��Y����Ϊ��
����?���������������������������������������������ʽ����
�ο��𰸣�����13�֣�
�E
�E
�����������
�����Ѷȣ�һ��
4������� ������Է��Լ�______________________________________��������Է��Ե�����֮һ��__________________________��������۵�__________,���Ǿ�����۵�_____________�����־�����Ǿ�����ɿ��Ŀ�ѧ������______________��
�ο��𰸣��������Է��Եس��ֶ��������ε����ʣ���������������ʵ����̶����̶���x-��������ʵ�顣
���������
�����Ѷȣ�һ��
5������� ��8�֣����мס��ҡ����������־�������ͼ��ʾ��������֪��������A��B�����Ӹ�����Ϊ?���Ҿ���Ļ�ѧʽΪ?��������Ļ�ѧʽΪ___?___��������Ļ�ѧʽΪ____?__��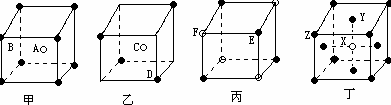
�ο��𰸣�1��1? C2D? EF? XY2Z
����������ھ����ж��㴦��ԭ��ֻ�ṩ1/8�������ϵ���1/4�����ϵ���1/2�������ĵ���1.���Լ���Bԭ�ӹ���8��1/8��1��A��1�����Ը�������1�U1.ͬ������ɵó�һ��C��D�ĸ�����2�U1������ѧʽΪC2D���Դ����ƣ��������ֱ�ΪEF��XY2Z��
�����Ѷȣ�һ��