1、选择题 在稀硫酸中加入一块铜片,铜片不会溶解,加入下列物质后,能使铜片溶解的是
A.稀盐酸
B.氢氧化钠
C.硫酸钠
D.硝酸钾
参考答案:D
本题解析:铜片不溶于非氧化性酸中,但稀硫酸中加入硝酸钾后,溶液中存在H+和 ,相当于稀硝酸,铜片能溶于稀硝酸中。
,相当于稀硝酸,铜片能溶于稀硝酸中。
本题难度:简单
2、实验题 下图是一位学生设计的实验室制取和收集氯气并验证其性质的装置图。

(1)找出在此装置图中出现的错误加以改正。
(2)实验过程中,在D装置中观察到的实验现象是?;在E装置中观察到的实验现象是?,反应的化学方程式是?;
(3)F装置的作用是?,反应的离子方程式是?。
参考答案:(1)稀盐酸改用浓盐酸。B应在A的左边。C中进气管应该长,排气管应该短。(每空1分,共3分。)
(2)溶液先变红后褪色;(2分) 有白色沉淀生成,Cl2+H2O =HClO +HCl
HCl+AgNO3=AgCl↓ +HNO3(每个答案1分,共3分。写总反应、写离子方程式都可)。
(3)吸收多余的氯气,防止污染环境,(1分)?Cl2+2OH―=ClO―+Cl―+H2O(2分)
本题解析:(1)观察装置图中试剂和仪器,出现的错误有:制取Cl2反应物为MnO2和浓盐酸,把装置图中的稀盐酸改为浓盐酸;应先用饱和食盐水除去HCl,再用浓硫酸除去H2O,所以B应在A的左边;Cl2的密度大于空气,收集时进气管应该长,排气管应该短。
(2)Cl2通入石蕊溶液,酸性使石蕊变化,Cl2与H2O反应生成的HClO具有漂白性,使石蕊褪色;Cl2与H2O反应生成的HCl与AgNO3反应生成白色AgCl沉淀,化学方程式有2个,首先是Cl2与H2O反应生成HCl和HClO,然后是HCl与AgNO3反应生成AgCl沉淀和HNO3。
(3)NaOH能与Cl2反应,所以NaOH溶液的作用是吸收多余的氯气,防止污染环境;Cl2与OH?反应生成Cl?、ClO?和H2O,配平可得离子方程式。2实验室制法的实验仪器和试剂及作用、实验现象的观察、方程式的书写。
本题难度:一般
3、实验题 (8分)为测定Cl2、Br2的氧化性强弱,设计了如下实验:
(可供选择的试剂有:氯水、溴水、NaCl溶液、NaBr溶液、酒精、四氯化碳)
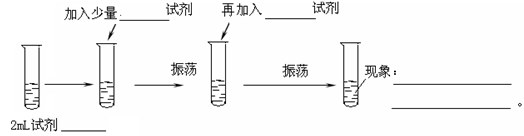
实验步骤如下:
由上回答下列问题:
(1)2ml试剂是?,加入少量?试剂,再加入?试剂
(2)现象是?。
(3)此实验可以证明Cl2的氧化性?(填强于、弱于)Br2的氧化性,此反应
的离子反应方程式为:?。
参考答案:(1)NaBr溶液、氯水、四氯化碳
(2)溶液分层,下层溶液显红棕色。
(3)强于? Cl2+2Br-=2Cl-=Br2
本题解析:要想证明氯气的氧化性强于单质溴的,可以利用单质间的相互置换能量来进行。因此可想溴化钠人员占和加入少量的氯水,反应后如果再加入四氯化碳,下层溶液如果显红棕色就能证明有单质溴生成。
本题难度:一般
4、选择题 不能由单质直接化合而得到的化合物有( )
A.Fe3O4
B.NaCl
C.FeCl2
D.CuO
参考答案:A.铁与氧气在点燃时直接生成四氧化三铁,故A不选;
B.钠与氯气在点燃时直接生成氯化钠,故B不选;
C.铁与氯气在点燃或加热时直接生成氯化铁,而不生成氯化亚铁,故C选;
D.Cu与氧气在加热时直接生成氧化铜,故D不选;
故选C.
本题解析:
本题难度:一般
5、计算题 将一定量的氯气通入250毫升溴化钾溶液中然后将所得溶液蒸干,得干燥固体40克,经分析知其中含25%的化合态的溴(质量)。试计算:
(1)40克固体中KBr的质量。?
(2)通入氯气在标况下的体积。
(3)原溴化钾溶液的百分比浓度(设溴化钾溶液的密度为1克/厘米3)。
参考答案:(1) 14.875 g
(2) 4.81 L
(3)26.4%
本题解析:略
本题难度:一般