1、填空题 常温下,下列各组离子在指定溶液中可能大量共存的是
A.在碱性溶液中:K+、Cl-、Na+、CO32-
B.在c(H+)/ c(OH-)=1×10-12的溶液中:Ca2+、Cl?-、K+、NH4+
C.澄清透明溶液中:Cu2+、Fe3+、I-、SO42-
D.与铝粉反应放出氢气的无色溶液中:K+、NO3-、Cl-、HCO3-
参考答案:A
本题解析:A、在碱性溶液中:K+、Cl-、Na+、CO32-均可以大量共存,A正确;B、在c(H+)/ c(OH-)=1×10-12的溶液中根据水的离子积常数可知,溶液中在c(H+)=1×10-13mol/L,即溶液显碱性,因此Ca2+、NH4+不能大量共存,B不正确;C、Cu2+、Fe3+与I-均发生氧化还原反应而不能大量共存,C不正确;D、与铝粉反应放出氢气的无色溶液可能显酸性,也可能显碱性,如果显碱性,HCO3-不能大量共存,如果显酸性HCO3-也不能大量共存,且在酸性溶液中NO3-与铝反应得不到氢气,D不正确,答案选A。
本题难度:一般
2、选择题 25 ℃时,x mol・L-1氢氟酸水溶液中,加入KOH固体调节溶液的pH(忽略加入固体引起的溶液体积变化),得到c(HF)、c(F-)与溶液pH的变化关系如图所示。下列说法正确的是? ( )。
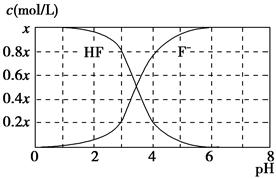
A.当c(F-)>c(HF)时,溶液呈碱性
B.当pH=2时,c(F-)<c(K+)
C.25 ℃时,氢氟酸的电离平衡常数为4×10-6
D.当pH=5时,c(HF)+c(K+)+c(H+)-c(OH-)=x mol・L-1
参考答案:D
本题解析:A项,根据图像可以得出当c(F-)>c(HF)时,溶液也可以呈酸性;B项,由电荷守恒得,c(K+)+c(H+)=c(F-)+c(OH-),当pH=2时,c(H+)>c(OH-),则c(F-)>c(K+)时才满足电荷守恒;Ka=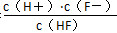 ,由图像可知两曲线交点时c(F-)=c(HF),pH约为3;即c(H+)=10-3 mol・L-1所以Ka=c(H+)=10-3,所以C项不正确;D项,根据电荷守恒,得c(K+)+c(H+)=c(F-)+
,由图像可知两曲线交点时c(F-)=c(HF),pH约为3;即c(H+)=10-3 mol・L-1所以Ka=c(H+)=10-3,所以C项不正确;D项,根据电荷守恒,得c(K+)+c(H+)=c(F-)+
c(OH-),若两边均加上c(HF),可得c(HF)+c(K+)+c(H+)=c(F-)+c(OH-)+c(HF),移项可得c(HF)+c(K+)+c(H+)-c(OH-)=c(F-)+c(HF),忽略加入固体引起的溶液体积变化,得c(F-)+c(HF)=x mol・L-1。
本题难度:一般
3、选择题 下列离子在溶液中能大量共存的是?(?)

A.Ba2+、SO42-、K+、 OH-
B.Na+、H+、NO3-、SO42-

C.Al3+、HCO3-、K+、 OH-
D.Fe2+、NH4+、NO3-、H+
参考答案:B
本题解析:略
本题难度:简单
4、选择题 下列各组离子在溶液中一定能大量共存的是
A.PH=0的溶液:K+、Ca2+、HCO3-、NO3-
B.c(H+水)=1×10-10 mol/L溶液中:K+、Fe2+、SO42-、NO3-
C.使紫色石蕊变蓝的溶液:K+、Na+、CH3COO-、SO42-
D.存在较多的Na+、SO42-、OH-的溶液中:Mg2+、Ba2+、Br-
参考答案:C
本题解析:A为强酸性溶液,碳酸氢根不能共存。B可能为强酸,或者强碱性溶液,若为强酸性,则亚铁离子与硝酸根离子在酸性条件下不共存。C中为碱性溶液,可以共存。D中氢氧化镁为沉淀,不共存。
点评:首先判断溶液酸碱性,再判断离子是否能够共存。属于简单题
本题难度:一般
5、填空题 (9分)分析、归纳、探究是学习化学的重要方法和手段之一.下面就电解质A回答有关问题(假定以下都是室温时的溶液).
(1)电解质A的化学式为NanB,测得浓度为c mol/L的A溶液的pH=a.
①试说明HnB的酸性强弱_______________________________________.
②当a=10时,A溶液呈碱性的原因是(用离子方式程式表示)________________.
③当a=10、n=1时,A溶液中各种离子浓度由大到小的顺序为
_______________________________________________________.
c(OH-)-c(HB)=________.
④当n=1、c=0.1、溶液中c(HB)∶c(B-)=1∶99时,A溶液的pH为__________(保留整数值).
(2)已知难溶电解质A的化学式为XnYm,相对分子质量为M,测得其饱和溶液的密度为ρ g/cm3,Xm+离子的浓度为c mol/L,则该难溶物XnYm的溶度积常数为Ksp=__________________________,该温度下XnYm的溶解度S=____________.
参考答案:(1)①当a=7时,HnB为强酸,当a>7时HnB为弱酸
②Bn-+H2O HB(n-1)-+OH-
HB(n-1)-+OH-
③c(Na+)>c(B-)>c(OH-)>c(H+) 10-10 mol/L
④11
(2)(m/n)m・cm+n 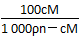
本题解析:略
本题难度:一般