1、选择题 将0.5 mol钠与0.5 mol镁分别加入2 mol・L-1、400 mL的硫酸中,所得溶液的质量是
A.硫酸钠溶液的质量大
B.同样大
C.硫酸镁溶液的质量大
D.无法确定
参考答案:B ?
本题解析:由反应方程式知,二者均是硫酸过量,
2Na+2H+===2Na++H2↑ Δm
2 mol? 44 g
0.5 mol? 11 g
Mg+2H+===Mg2++H2↑ Δm
1 mol? 22 g
0.5 mol? 11 g
溶液质量增加相等。充分利用质量差量法(Δm)解有关金属与酸反应所得溶液质量增重问题。
本题难度:一般
2、选择题 向一定量的饱和NaOH溶液中加入少量Na2O固体,恢复到原来温度时,下列说法中正确的是(?)
A.溶液中的Na+总数不变
B.溶液中的OH-数目不变
C.溶质的物质的量浓度不变
D.溶液的质量不变
参考答案:C
本题解析:加入的Na2O与水反应:Na2O+H2O=2NaOH,原NaOH饱和溶液的水减少,溶质析出,所以溶液的质量减小,溶质的物质的量浓度不变,Na+总数和OH?数目减少,故C项正确。
本题难度:一般
3、填空题 (10分)实验室利用右图所示装置进行NaHCO3的受热分解实验。请回答:
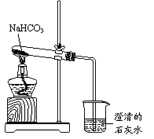
(1)加热一段时间后,烧杯中观察到的实验现象是?。
(2)实验结束时的正确操作是?;理由是?。?
(3)NaHCO3受热分解的化学方程式:?。
(4)33.6gNaHCO3受热分解放出气体在标况下的体积?
参考答案:(1)澄清石灰水变浑浊?(2)先将导管从溶液中移出,再熄灭酒精灯;?反过来操作会引起倒吸?
(3)2 NaHCO3  ?Na2CO3 + CO2↑+ H2O?(4)4.48L
?Na2CO3 + CO2↑+ H2O?(4)4.48L
本题解析:2 NaHCO3  ?Na2CO3 + CO2↑+ H2O?,所以烧杯中澄清石灰水变浑浊,实验结束的时候应先撤导管再熄灭酒精灯。33.6g NaHCO3为0.4mol,根据方程式可知产生CO20.02mol,体积为4.48L。3受热分解实验
?Na2CO3 + CO2↑+ H2O?,所以烧杯中澄清石灰水变浑浊,实验结束的时候应先撤导管再熄灭酒精灯。33.6g NaHCO3为0.4mol,根据方程式可知产生CO20.02mol,体积为4.48L。3受热分解实验
点评;本实验题非常基础简单。
本题难度:一般
4、计算题 加热33.6gNaHCO3至没有气体放出时,剩余的物质是什么?计算剩余物质的质量和物质的量。
参考答案:Na2CO3? 0.2mol? 21.2g
本题解析:略
本题难度:简单
5、选择题 化学反应NaOH+HCl==NaCl+H2O属于
A.化合反应
B.分解反应
C.复分解反应
D.置换反应
参考答案:C
本题解析:化合反应是指有两种或两种以上的物质生成另一种物质的反应;分解反应是指有一种物质生成两种或两种以上的物质的反应;有一种单质和一种化合物生成另一种单质和另一种化合物的反应叫置换反应;两种化合物相互交换成分生成另外两种化合物的反应叫做复分解反应。据此判断,NaOH+HCl==NaCl+H2O属于复分解反应,选C。
本题难度:一般