|
|
|
高考化学知识点整理《化学反应进行的方向》高频考点预测(2019年最新版)(三)
2020-08-13 07:18:35
【 大 中 小】
|
1、选择题 工业上用CO生产甲醇的反应为CO(g)+2H2(g) CH3OH(g)。图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图。下列叙述错误的是 CH3OH(g)。图10表示反应中能量的变化;图11表示一定温度下,在体积固定为2L的密闭容器中加入4mol H2和一定量的CO(g)后,CO(g)和CH3OH(g)的浓度随时间的变化图。下列叙述错误的是
 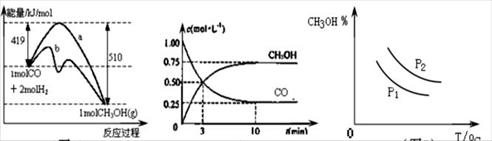
图10 图11 图12
A.CO和H2合成CH3OH的反应:△H<0,△S>0
B.保持温度不变,再充入1molCO和2molH2,反应达到新平衡时n(CH3OH)/n(CO)减小
C.图10中曲线b可表示使用了催化剂的能量变化情况
D.图12中曲线可表示在不同压强P1、P2(P1<P2)条件下甲醇百分含量随温度变化的情况
|
2、选择题 在固定体积的密闭容器中,发生:N2(g)+3H2(g) 2NH3(g)DH=-92.2 kJ・mo1-1 ,下图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件) 2NH3(g)DH=-92.2 kJ・mo1-1 ,下图表示在时间t0~t7中反应速率与反应过程的曲线图,则容器内氨的百分含量最高的一段时间是(只改变单一的条件)
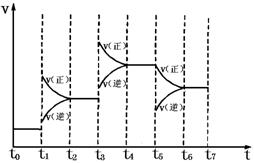
A.t0~t1
B.t2~t3
C.t4~t5
D.t6~t7
3、选择题 下列说法不正确的是?
[? ]
A.吸热反应可以自发进行
B.所有自发过程都将导致体系的熵值增大
C.有序性越高,熵值就越低
D.对于同种物质,在气态时其熵值最大
4、选择题 平衡体系mA(g)+nB(g) pC(g)+qD(g)有下列判断:①温度不变时,将容器体积增大一倍,若A的浓度变为原来的0.48倍,则m+n>p+q②若平衡时A和B的转化率相等,说明起始时A和B的物质的量之比为m:n③若改变一个条件使反应重新达到平衡时,D的浓度增大了,说明平衡向右移动了④若平衡体系中A、B、C、D的物质的量分别为a、b、c、dmol,则再向其中加入a、b、c、dmol的A、B、C、D时,平衡可能不移动⑤若平衡后降低温度,该反应的化学反应平衡常数增大,说明该反应的ΔH>0,其中正确的是(?)? pC(g)+qD(g)有下列判断:①温度不变时,将容器体积增大一倍,若A的浓度变为原来的0.48倍,则m+n>p+q②若平衡时A和B的转化率相等,说明起始时A和B的物质的量之比为m:n③若改变一个条件使反应重新达到平衡时,D的浓度增大了,说明平衡向右移动了④若平衡体系中A、B、C、D的物质的量分别为a、b、c、dmol,则再向其中加入a、b、c、dmol的A、B、C、D时,平衡可能不移动⑤若平衡后降低温度,该反应的化学反应平衡常数增大,说明该反应的ΔH>0,其中正确的是(?)?
A. ②④? B.②③? C. ①④⑤? D. ①②③
5、选择题 下列有关说法正确的是
A.铁表面镀铜时,铜与电源的正极相连,铁与电源的负极相连
B.用pH均为2的盐酸和醋酸分别中和等物质的量的NaOH,消耗醋酸的体积更大
C.一定温度下,反应2Mg(s)+CO2(g)=2MgO(s)+C(s)能自发进行,则该反应△H<0
D.常温下,向饱和Na2CO3溶液中加少量BaSO4粉末,过滤,向洗净的沉淀中加稀盐酸有气泡产生,说明常温下Ksp(BaCO3)<Ksp(BaSO4)
|