1��ѡ���� 16.8gNaHCO3��7.8gNa2O2���ܱ����������գ���ַ�Ӧ���ܱ����������¶�Ϊ500�棬���������������
A��Na2CO3��Na2O��O2
B��Na2CO3��CO2��O2��H2O(g)
C��Na2CO3��O2��H2O(g)
D��NaHCO3��Na2CO3��O2
�ο��𰸣�C
���������16.8gNaHCO3��7.8gNa2O2�����ʵ����ֱ���0.2mol��0.1mol��̼�����Ʒֽ�����0.1molˮ��0.1molCO2��������������������CO2�����Թ��������������յ���CO2��ֻ�е��������ƹ���ʱ���ٺ�ˮ������Ӧ�����������ƺ����������ڹ�������Ҳ��0.1mol�����Ժ�CO2ǡ�÷�Ӧ����˴�ѡC��
����������Ĺؼ���ȷ�жϳ������������Ⱥ�CO2��Ӧ��Ȼ���ٸ��ݷ���ʽ�����йصļ�����жϡ�
�����Ѷȣ�һ��
2��ʵ���� �ס�������̽����ѧϰС�飬������ⶨ����������Ʒ����������Na2O���Ĵ��ȡ�
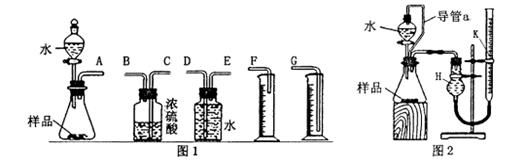
��1������ͬѧ��ѡ��ͼ1ʵ��װ�����ʵ�飺
��д��ʵ������������Ӧ�Ļ�ѧ����ʽ?��
�ڸ���ͬѧѡ�����װ�õ�����˳���ǣ�
A�ӣ� ������ ���ӣ� ������ ���ӣ� ������ӿ���ĸ���ɲ���������
��2�� ����ͬѧ��ϸ��������ͬѧ��ʵ��װ�ú���Ϊ��ˮ������ƿ�У���ʹ������������ Ҳ�Ὣƿ�ڿ����ų���ʹ�����������ƫ��;ʵ�����ʱ�����ӹ��ƿ����Ͳ�ĵ�����������ˮ���ڣ�ʹ�����������ƫС���������������ͼ2��ʾ��ʵ��װ�á�
��װ���е���a�������ǣ�?��
��ʵ�������,�ڶ�ȡ������k��Һ�����ʱ������Ϊ�������˳����??(��A�� B��C��ĸ��ʾ)
A. ������������k�а�Һ�����͵���ƽ
B. �ȴ�ʵ��װ����ȴ
C. �����ƶ�������k,ʹk��Һ����H�е�Һ����ƽ
����ʵ������Ʒ������Ϊwg��ʵ��ǰ��������k��Һ������ֱ�ΪV1��V2(����ɱ����������Ʒ�Ĵ���Ϊ_______ (��w��V�ı���ʽ����
�ο��𰸣���1���� Na2O+H2O=2NaOH��2Na2O2+2H2O=4NaOH+O2����2�֣�����EDG ��1�֣�
��2���ٿ���ʹ��Һ©���������ѹǿ����ƿ������ѹǿ��ȣ���Һ©������ʱˮ��˳�����£��������ڼ���ˮ��������������1�֣���BCA?��1�֣�
��Na2O2%=195��(V1-V2)/28w��100%��2�֣���
�����������1������ͬѧѡ��ͼ1ʵ��װ�����ʵ�飺��ʵ����������Ӧ�Ļ�ѧ����ʽΪ��Na2O+H2O=2NaOH��2Na2O2+2H2O=4NaOH+O2������ʵ�������������������Բ����ų�ˮ������ķ������ⶨ�����Ը���ͬѧѡ�����װ�õ�����˳����A��E��D��G�����Բ���Ũ����������������Ϊ���õ�����ˮ������2��ˮ������ƿ�У���ʹ������������Ҳ�Ὣƿ�ڿ����ų���a�����þ�������������һȱ�㣬��a�������ǿ���ʹ��Һ©���������ѹǿ����ƿ������ѹǿ��ȣ���Һ©������ʱˮ��˳�����£��������ڼ���ˮ��������������ʵ�������,�ڶ�ȡ������k��Һ�����ʱ��Ӧ�õȴ�ʵ��װ����ȴ��Ȼ�������ƶ�������k,ʹk��Һ����H�е�Һ����ƽ��������Ҫ��������������k�а�Һ�����͵���ƽ���ʺ�����˳��ΪBCA������ʵ������Ʒ������Ϊwg��ʵ��ǰ��������k��Һ������ֱ�ΪV1��V2(����ɱ�����������������������Ϊ(V1-V2)mL������2Na2O2+2H2O=4NaOH+O2������������������Ϊ32��(V1-V2)��156/22.4g�����Թ������Ƶ�����m=156��(V1-V2)/22.4������Ʒ�Ĵ���Ϊ��156��(V1-V2)/22.4��100%������Ϊ195��(V1-V2)/28w��100%��
���������⿼�����Ƽ��仯��������ʣ��ÿ����Ǹ߿�������ص���ѵ㣬������ؿ���ѧ����ʵ��ķ��������ͼ��������������Ѷ��еȡ�
�����Ѷȣ�һ��
3��ѡ���� �����й�Na2CO3��NaHCO3���ʵıȽ��У���ȷ���� (? )
A�����ȶ���Na2CO3 < NaHCO3
B��ˮ���� Na2CO3 < NaHCO3
C�������ǵ�Ũ�ȵ���Һ�е���ϡ���ᣬ�ų�����Ŀ���Na2CO3��NaHCO3
D�������ǵ���Һ�зֱ����ʯ��ˮ�����г�������
�ο��𰸣�D
���������A �� ���ȶ���Na2CO3 >NaHCO3
B ��Na2CO3 ���ܽ�ȴ��� NaHCO3
C �������ǵ�Ũ�ȵ���Һ�е���ϡ���ᣬ�ų�����Ŀ���Na2CO3<NaHCO3?
D �Էֱ����ʯ��ˮ�����г�������
�����Ѷȣ���
4������� �п��Ľ���Na��¶�ڿ����У���仯�������£�

��1����Ӧ��ķ�Ӧ�����������仯�Ĺ�ϵ���£�
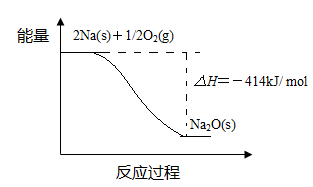
�� ��Ӧ�� ���� ����Ӧ������ȡ������ȡ������ж���������������
�� 1 mol Na(s)ȫ��������Na2O(s)���Ȼ�ѧ����ʽ����������
��2����Ӧ����Na2O��ˮ�ķ�Ӧ�������ĵ���ʽ��?��
��3����ɫ��ĩΪNa2CO3����������ˮ����Ϊ0.1 mol/L Na2CO3��Һ������˵����ȷ����?������ĸ����
A�������¶ȣ���Һ��pH����
B��c(OH��)��c (H��)��c (HCO3��)��2 c (H2CO3)
C����������NaOH���壬c (CO32�D)��c (Na��)������
D��c (Na��) > c (CO32�D) > c (HCO3�D) > c(OH�D) > c (H��)
 ?Ni + 2NaCl����������Ӧʽ��_____��
?Ni + 2NaCl����������Ӧʽ��_____��