1、选择题 下列对于Na2O、Na2O2的比较正确的一项是
[?]
A. Na2O2、Na2O都是钠的氧化物,都是碱性氧化物
B. Na2O、Na2O2都是易溶于水(与水反应)的白色固体
C. Na2O2在和CO2的反应中既是氧化剂又是还原剂
D. Na2O2与水反应时,1 mol Na2O2转移2 mol电子
参考答案:C
本题解析:
本题难度:简单
2、选择题 下列物质间的转化在给定条件下能一步实现的是
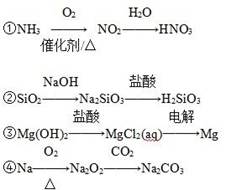
A.②④
B.③④
C.①④
D.①②③
参考答案:A
本题解析:本题考查了给定条件下物质之间的转化,意在考查考生对元素化合物知识的理解与应用能力。氨的催化氧化为4NH3+5O2 4NO+6H2O,一步只能生成NO,①错;SiO2+2NaOH===Na2SiO3+H2O, Na2SiO3+2HCl===H2SiO3↓+2NaCl,②正确;电解MgCl2溶液不能得到金属镁,电解熔融的MgCl2才能得到金属镁,③错;2Na+O2
4NO+6H2O,一步只能生成NO,①错;SiO2+2NaOH===Na2SiO3+H2O, Na2SiO3+2HCl===H2SiO3↓+2NaCl,②正确;电解MgCl2溶液不能得到金属镁,电解熔融的MgCl2才能得到金属镁,③错;2Na+O2 Na2O2,2Na2O2+2CO2===2Na2CO3+O2,④正确。
Na2O2,2Na2O2+2CO2===2Na2CO3+O2,④正确。
本题难度:一般
3、选择题 美国“海狼”潜艇上的核反应堆内使用了液体铝钠合金(单质钠和单质铝熔合而成)作载热介质,有关说法不正确的是
A.原子半径:r(Na)>r(Al)
B.铝钠合金若投入一定的水中可得无色溶液,则n(Al)<n(Na)
C.m g不同组成的铝钠合金投入足量盐酸中,若放出H2越多,则铝的质量分数越小
D.铝钠合金投入到足量氯化铜溶液中,肯定有氢氧化铜沉淀也可能有铜析出
参考答案:C
本题解析:同周期自左向右原子半径逐渐减小,A正确;钠溶于水生成氢氧化钠和氢气,而铝能和氢氧化钠难溶于反应生成NaAlO2和氢气,因此根据得到的是无色溶液可知,单质铝的物质的量小于钠的,B正确;在质量相等的条件下,金属铝放出的氢气多,所以若放出H2越多,则铝的质量分数越大,C不正确;钠溶于水生成氢氧化钠和氢气,因此可以生成氢氧化铜沉淀。如果铝过量,则还能和硫酸铜发生置换反应生成铜,D正确,答案选C。
点评:钠属于活泼的金属,极易和水反应生成氢氧化钠和氢气。所以关于钠投入水溶液中的反应要注意反应的先后顺序,即首先和水,然后生成的氢氧化钠再和溶液反应即可。
本题难度:一般
4、填空题 下面为中学化学常见物质,各物质间有如下转化关系:
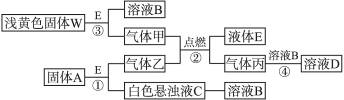
(1)W为_____________________。
(2)固体A是一种重要的工业原料,1 mol气体乙完全燃烧时生成1 mol E和2 mol丙,则乙的分子式为______________________。
(3)C溶液中的溶质和丙以物质的量之比1∶2反应时生成物质丁,该离子方程式为________________________。
(4)利用图中有关物质实现C→B的转变,该物质是________________(填化学式)。
(5)若甲和乙恰好完全反应,则A和W的物质的量之比为______________________。
(6)物质W与丁按物质的量1 mol与1 mol混合并在密闭容器中充分反应,最终生成固体及物质的量为______________________________。
参考答案:(1)Na2O2 (2)C2H2? (3)CO2+OH-====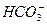 ?(4)Na2CO3
?(4)Na2CO3
(5)1∶2? (6)Na2CO3、CaCO3各1 mol
本题解析:物质的颜色是入手点。浅黄色固体W为Na2O2,联系Na2O2的有关性质的反应结合该图示可以推知液体E为H2O,所以B为NaOH溶液,气体甲为O2。由题意(2)可知A为CaC2,气体乙为C2H2,白色悬浊液C为Ca(OH)2,气体丙为CO2。熟悉物质的量之间的转化关系可以计算推知有关数据。
本题难度:简单
5、实验题 “厨房化学”可以理解为利用家庭生活用品来做化学实验,对化学进行学习和研究的活动。某厨房内有一含NaCl、Na2CO3・10H2O和NaHCO3的混合物,某同学设计如下实验,通过测量反应前后C、D装置质量的变化,测定该混合物中各组分的质量分数。
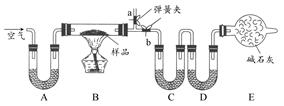
(1)实验时,B中发生的反应的化学方程式为?。
(2)装置C、D中盛放的试剂分别为:C?,D?。(供选试剂为:浓硫酸、无水CaCl2、碱石灰)
(3)E装置中的仪器名称是?,它在该实验中的主要作用是?。
(4)若将A装置换成盛放NaOH溶液的洗气瓶,则测得的NaCl含量将?(填“偏高”“偏低”或“无影响”)。
参考答案:(1)Na2CO3・10H2O Na2CO3+10H2O、2NaHCO3
Na2CO3+10H2O、2NaHCO3 Na2CO3+CO2↑+H2O (2)无水CaCl2;碱石灰 (3)干燥管;防止空气中的H2O和CO2进入D中 (4)偏低
Na2CO3+CO2↑+H2O (2)无水CaCl2;碱石灰 (3)干燥管;防止空气中的H2O和CO2进入D中 (4)偏低
本题解析:将空气通过碱石灰吸收CO2和H2O后进入装置B。在B中,Na2CO3・10H2O和NaHCO3发生分解,产生的H2O被C管(盛无水CaCl2)吸收,CO2被D管(盛碱石灰)吸收,通过C、D管的质量变化可计算出Na2CO3・10H2O和NaHCO3的质量,从而确定各成分的质量分数,但一定要防止外界空气中的CO2和H2O进入装置。若将A装置换作盛NaOH溶液的洗气瓶,则m(H2O)增加,使测得的Na2CO3・10H2O和NaHCO3的含量偏高,NaCl的含量偏低。
本题难度:一般