1、选择题 某元素的一种同位素X的原子质量数为A,含N个中子,它与1H原子组成HmX分子。在ag HmX中所含质子的物质的量是(? )
A. (A-N+m) mol
(A-N+m) mol
B.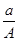 (A-N) mol
(A-N) mol
C. (A-N) mol
(A-N) mol
D.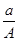 (A-N+m) mol
(A-N+m) mol
参考答案:A
本题解析:本题考查质量数、质子数、中子数的关系。X中含有的质子数=A-N,1 mol HmX中含有的质子数=(A-N+m) mol,则a g HmX中含有的质子数= ?(A-N+m) mol.
?(A-N+m) mol.
本题难度:一般
2、选择题 在周期表主族元素中,甲元素与乙、丙、丁三元素相邻,甲、乙的原子序数之和等于丙的原子序数;这四种元素原子的最外层电子数之和为20。下列判断中正确的是(?)
A.原子半径:丙>乙>甲>丁
B.气态氢化物的稳定性:甲>丙
C.最高价氧化物对应水化物的酸性:丁>甲
D.乙和甲或乙和丁所能形成的化合物都是有毒物质
参考答案:B
本题解析:考查周期表的结构。甲元素与乙、丙、丁三元素相邻,且四种元素原子的最外层电子数之和为20,所以甲的最外层电子数是5。又因为甲、乙的原子序数之和等于丙的原子序数,所以甲是N,乙是O,丙是P,丁是C。原子半径是P>C>N>O,A不正确。N的非金属性强于P的,所以N的氢化物的稳定性强于P的氢化物的稳定性,B正确。C的非金属性弱于N的,所以碳酸的酸性弱于硝酸的,C不正确。CO2不是有毒物质,D不正确。答案选B。
本题难度:简单
3、选择题 X、Y、Z分别代表3种不同的短周期元素,X元素的原子最外层电子数为1,Y元素原子M层有6个电子,Z元素原子的L层电子数6,由这三种元素组成的化合物的化学式是
A.X3YZ4
B.X2YZ3
C.XYZ4
D.X4YZ4
参考答案:B
本题解析:根据元素的结构可知,X的最高价是+1价,Y是S,Z是O,可组成的化学式应该是选项B,其余都是错误的,答案选B。
本题难度:一般
4、选择题 下图是部分短周期元素原子(用字母表示)最外层电子数与原子序数的关系图。下列说法正确的是(双选)? ( )。
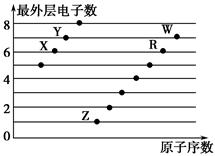
A.X和R在同一周期
B.原子半径:W>R>X
C.气态氢化物的稳定性:Y>X
D.X、Z形成的化合物中可能含有共价键
参考答案:CD
本题解析:由于均为短周期元素,故X、Y在第二周期,Z、R、W在第三周期,X、R位于第ⅥA族,Y、W位于第ⅦA族,原子半径R>W,故A、B错误;X、Z形成的化合物为Na2O和Na2O2,Na2O2中既含有离子键也含有共价键。
本题难度:一般
5、选择题 关于卤素(F、Cl、Br、I)的化学性质的叙述,错误的是
A.随原子序数逐渐增大,单质跟水的反应能力逐渐减弱
B.随原子序数逐渐增大,单质的氧化性逐渐减弱
C.将氯水加到KI-淀粉溶液中,溶液变蓝
D.随原子序数逐渐增大,氢化物的稳定性逐渐增强
参考答案:D
本题解析:A、同主族自上而下非金属性逐渐减弱,因此随原子序数逐渐增大,单质跟水的反应能力逐渐减弱,A正确;B、同主族自上而下原子序数逐渐增大,非金属性逐渐减弱,单质的氧化性逐渐减弱,B正确;C、氯元素的非金属性强于碘元素的,因此氯气能把碘化钾氧化生成单质碘,碘遇淀粉显蓝色,所以将氯水加到KI-淀粉溶液中,溶液变蓝,C正确;D、非金属性越强,氢化物的稳定性越强,因此随原子序数逐渐增大,F、Cl、Br、I的非金属性逐渐减弱,所以氢化物的稳定性逐渐减弱,D不正确,答案选D。
本题难度:一般