1������� ��֪����A��B��C��D��E��F��һ�������µĹ�ϵ��ͼ�����������ʵ���ɫ��Ӧ���ʻ�ɫ��
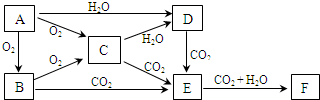
��1��д���������ʵĻ�ѧʽ��A______��D______��F______��
��2��A��B��C��D�������ʷֱ��ڱ�¶�ڿ����У������ղ���Ϊ______�����б��ʹ�������������ԭ��Ӧ�����������ǣ���д���ʶ�Ӧ�Ļ�ѧʽ��______����C����CuSO4��Һ�У������ķ�Ӧ�ķ���ʽΪ______��
�ο��𰸣��������ʵ���ɫ��Ӧ���ʻ�ɫ��������NaԪ�أ���A��B��C��֪��AΪNa��BΪNa2O��CΪNa2O2����DΪNaOH��EΪNa2CO3��FΪNaHCO3��
��1�������Ϸ�����֪AΪNa��DΪNaOH��FΪNaHCO3���ʴ�Ϊ��Na��NaOH��NaHCO3��
��2��AΪNa�����������������Ӧ����Na2O��BΪNa2O��CΪNa2O2�������������ˮ��Ӧ����NaOH���ҹ��������������̼��Ӧ����̼���ƺ�������Ϊ������ԭ��Ӧ��DΪNaOH����������ж�����̼��Ӧ����̼���ƣ��������ƿ���ˮ��Ӧ�����������ƺ���������������ͭ��Һ������������ͭ����������Ӧ�ķ���ʽΪ2Na2O2+2H2O+2CuSO4�T2Cu��OH��2��+4Na2SO4+O2����
�ʴ�Ϊ��Na2CO3��Na2O2��Na��2Na2O2+2H2O+2CuSO4�T2Cu��OH��2��+4Na2SO4+O2����
���������
�����Ѷȣ�һ��
2������� A��B��C��D��E�������ʵ���ɫ��Ӧ���Ի�ɫ��������ڵ�A���Եõ�����B�����A��ˮ��Һ���Եõ�������ҺC��ת����ϵ��ͼ��
��1����Ҫ��д���������ʣ�B��ԭ�ӽṹʾ��ͼ______������C������______��
��2��д��A��C�Ļ�ѧ����ʽ��______��
��3��д��C��Һ��E��Һ��Ӧ�����ӷ���ʽ��______��
��4��д����ȥD�����е�E���ʵĻ�ѧ����ʽ��______��
��5����������A�������ӵ�ʵ����������ǣ�______��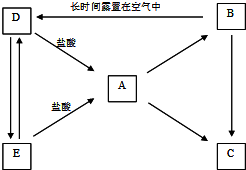
�ο��𰸣�A��B��C��D��E�������ʵ���ɫ��Ӧ���Ի�ɫ��Ӧ����NaԪ�أ�D��E���������ᷴӦ����A����AӦΪNaCl��������ڵ�A���Եõ�����B�����A��ˮ��Һ���Եõ�������ҺC����BΪNa��CΪNaOH��DΪNa2CO3��EΪNaHCO3��
��1��BΪNa��ԭ�Ӻ�����3�����Ӳ㣬����������Ϊ1��ԭ�ӽṹʾ��ͼΪ
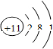
��CΪNaOH���׳��ռ�������ƣ�
�ʴ�Ϊ��
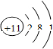
���ռ�������ƣ�
��2��A��C�ķ�ӦΪ���ʳ��ˮ������ʽΪ2NaCl+2H2O?ͨ��?.?2NaOH+H2��+Cl2�����ʴ�Ϊ��2NaCl+2H2O?ͨ��?.?2NaOH+H2��+Cl2����
��3��C��Һ��E��Һ��Ӧ�����ӷ���ʽΪ2HCO3-+OH-�TCO32-+H2O���ʴ�Ϊ��2HCO3-+OH-�TCO32-+H2O��
��4��NaHCO3���ȶ��������ֽ⣬��ͨ�����ȵķ�����ȥ����Ӧ�Ļ�ѧ����ʽΪ2NaHCO3?��?.?Na2CO3+H2O+CO2����
�ʴ�Ϊ��2NaHCO3??��?.?Na2CO3+H2O+CO2����
��5��AӦΪNaCl�����������ӵķ�����ȡ����A��Һ���Թܣ��μ������ữ����������Һ�������ְ�ɫ��������֤�����������ӣ�
�ʴ�Ϊ��ȡ����A��Һ���Թܣ��μ������ữ����������Һ�������ְ�ɫ��������֤�����������ӣ�
���������
�����Ѷȣ�һ��
3���ƶ��� ��֪��A��BΪ�����ڷǽ��������Ҿ�Ϊ���壻�ס���Ϊ�����ڽ������ʣ�����I��Ũ��Һ�з����ۻ���C��H��J����Һ���ʼ��ԣ������ʼ��ת����ϵ����(����������δ��������δע����Ӧ����)

��1��д��A�ĵ���ʽ__________��C���ӵĿռ乹�ͣ�_____________��
��2��д����Ӧ�ڵĻ�ѧ����ʽ____________________________��
��3����Ӧ�ܵĻ�ѧ����ʽΪ______________________________��
��4����Ӧ�ݵĻ�ѧ����ʽ��______________________________��
��5����Ӧ�����ӷ���ʽ��______________________________��
�ο��𰸣���1��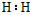 ��������
��������
��2��4NH3+5O2 4NO+6H2O
4NO+6H2O
��3��3NO2+H2O==2HNO3+NO
��4��2Na+2H2O==2NaOH+H2��
��5��2Al+2H2O+2OH-==2AlO2-+3H2��
���������
�����Ѷȣ�����
4������� �����Ѿ�ѧ���˺ܶ����ʣ����������ơ����ᡢ����̼��ơ��������ơ������������Ȼ������������ơ��Ȼ��ơ�����������̼���ơ����ᡢ̼�����ơ��������������ơ����������Ȼ���������������̼��ƫ�����ơ����������
��1�������оٵ������У������������������______
��2��A��B��C��D�������оٵ������е��������ʣ����������µ�ת����ϵ��
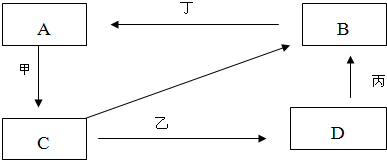
��д��A��B��C��D�������ʵĻ�ѧʽ��A______B______C______D______
��д���ס��ҡ�����������ʾ�ķ�Ӧ��Ļ�ѧʽ��Ӧ����
��______��______��______��______
��3���������оٵ�������ѡ����ʵ����ʣ�����Һ�зֱ������µ����ӷ�Ӧ��д�������ӷ���ʽ��
����һ��������������______
����һ��������������______
����һ�������������______��
�ο��𰸣���1���������������У����������������Ϊ���������ʴ�Ϊ����������
��2��������ת����ϵ��֪A��B��C��DӦ������ͬԪ�أ�����ֻ���������������������Ȼ�����ƫ�����Ʒ��ϣ�����C��ת��ΪB��D�������ʣ�ӦΪNaAlO2���������ᷴӦ�ֱ�����Al��OH��3��AlCl3����DΪAl��OH��3��BΪAlCl3��AΪAl2O3��
�������Ϸ�����֪AΪAl2O3��BΪAlCl3��CΪAlCl3��DΪAl��OH��3���ʴ�Ϊ��Al2O3��AlCl3��NaAlO2��Al��OH��3��
��AΪAl2O3������NaOH��Ӧ����NaAlO2��NaAlO2�������������̼��Ӧ����Al��OH��3��Al��OH��3�������ᷴӦ����AlCl3�������Ȼ�����Һ���ٽ������ӵ�ˮ�������������������տ�������������
�ʴ�Ϊ��NaOH��CO2��HCl�����ȣ�
��3���������������ƺ����Ȼ������Ȼ�����Ӧ���ɳ������緢��Fe3++3OH-=Fe��OH��3�����ʴ�Ϊ��Fe3++3OH-=Fe��OH��3����
���������������ᡢ�������̼���ơ�̼�����Ʒ�Ӧ���ɶ�����̼���壬�ɷ���HCO3-+H+=CO2��+H2O���ʴ�Ϊ��HCO3-+H+=CO2��+H2O��
�۶�Ӧ���������Ϊˮ����Ϊ����кͷ�Ӧ����������������ķ�Ӧ���ɷ���Al2O3+6H+=2Al3++3H2O���ʴ�Ϊ��Al2O3+6H+=2Al3++3H2O��
���������
�����Ѷȣ�һ��
5������� ����A��B��C��D���ֻ��������ɫ��Ӧ���ʻ�ɫ��A��B��C�ֱ�����������ᷴӦ��������D����������C���Ⱥ������A����ɫ��ζ������E������A��Һ��ͨ������E��������C����B��C����Һ��Ͽ�����A����ش��������⣺
��1���ƶ�A��B��C��D�Ļ�ѧʽ��A______��B______��C______��D______
��2��A��Һ��ͨ������E��Ӧ�����ӷ���ʽΪ______
��3��B��Һ��C��Һ��Ӧ�����ӷ���ʽΪ______��
�ο��𰸣�A��B��C��D���ֻ��������ɫ��Ӧ���ʻ�ɫ��Ӧ������NaԪ�أ�A��B��C�ֱ�����������ᷴӦ��������D��
DӦΪNaCl��������C���Ⱥ������A����ɫ��ζ������E��CӦΪ�ֽ�����Σ�ΪNaHCO3����AΪNa2CO3��EΪCO2��
��Na2CO3��Һ��ͨ������CO2��������NaHCO3��B��NaHCO3����Һ��Ͽ�����Na2CO3����BӦΪNaOH����
��1�������Ϸ�����֪AΪNa2CO3��BΪNaOH��CΪNaHCO3��DΪNaCl���ʴ�Ϊ��Na2CO3��NaOH��NaHCO3��NaCl��
��2����Na2CO3��Һ��ͨ������CO2��������NaHCO3����Ӧ�����ӷ���ʽΪH2O+CO2+CO32-�T2HCO3-��
�ʴ�Ϊ��H2O+CO2+CO32-�T2HCO3-��
��3��NaOH��NaHCO3����Һ��Ͽ�����Na2CO3����Ӧ�����ӷ���ʽΪHCO3-+OH-�TCO32-+H2O��
�ʴ�Ϊ��HCO3-+OH-�TCO32-+H2O��
���������
�����Ѷȣ�һ��