1、简答题 KClO3和浓盐酸在一定温度下反应生成绿黄色的易爆物ClO2,其变化可表述为:
______KClO3+______HCl(浓)→______KCl+______ClO2↑+______Cl2↑+____________
(1)请完成该化学方程式平配平(未知物化学式和系数填入横线里)
(2)浓盐酸在反应中显示出来的性质是______
①只有还原性②还原性和酸性
③只有氧化性④氧化性和酸性
(3)ClO2具有很强的氧化性.因此,常被用作消毒剂,其消毒效率(以单位质量得到的电子数表示)是Cl2的______倍.
参考答案:(1)氧化还原反应中化合价不交叉,所以氯酸钾中的氯元素化合价由+5降到二氧化氯中的+4价,得1mol电子,盐酸中的氯元素由-1价升到0价,共失2mol电子,根据电子守恒,得失电子数目应相等,所以氯酸钾前是2,观察法配平其他系数,故答案为:2,4,2,2,1,2;
(2)氯元素的化合价升高,表现了还原性,化合价不变得到氯化钾,表现了盐酸的酸性,故答案为:②;
(3)1molCl2可以获得2mol电子,1molClO2可以获得电子5mol电子,作消毒剂,其消毒后的还原产物是氯离子;令其质量为mg,则消毒效率为m67.5×5m71×2×1=2.63,故答案为:2.63.
本题解析:
本题难度:简单
2、填空题 (12分)实验室可由软锰矿(主要成分为MnO2)制备KMnO4,方法 如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。请回答:
如下:软锰矿与过量固体KOH和KClO3在高温下反应,生成锰酸钾(K2MnO4)和KCl;用水溶解,滤去残渣,滤液酸化后,K2MnO4转变为MnO2和KMnO4;滤去MnO2沉淀,浓缩滤液,结晶得到深紫色的针状KMnO4。请回答:
(1)软锰矿制备K2MnO4的化学方程式是
;
(2)K2MnO4制备KMnO4的离子方程式是 ;
(3)若用2.5g软锰矿(含MnO280%)进行上述实验,计算KMnO4的理论产量;
(4)KMnO4能与热的经硫酸酸化的Na2C2O4反应生成Mn2+和CO2,该反应的化学方程式是 ;
(5)上述制得的KMnO4产品0.165g,恰好与0.335g纯Na2C2O4反应完全,计算该KMnO4的纯度。
参考答案:(12分)(1)3MnO2+6KOH+KClO3 3K2MnO4+KCl+3H2O(2分)
3K2MnO4+KCl+3H2O(2分)
(2)3Mn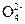 +4H+ = MnO2↓+2Mn
+4H+ = MnO2↓+2Mn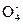 +2H2O(2分)
+2H2O(2分)
(3)由上述两个化学方程式可知,反应物和生成物间的计量关系为:(3分)
 ? MnO2? K2MnO4?
? MnO2? K2MnO4?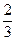 KMnO4
KMnO4
87? 158×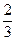
2.5×80%? x
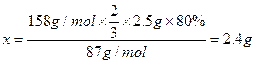
答:KMnO4的理论产量是2.4g
(4)2KMnO4+5Na2C2O4+8H2SO4 K2SO4+2MnSO4+5Na2SO4
K2SO4+2MnSO4+5Na2SO4 +10CO2↑+8H2O(2分)
+10CO2↑+8H2O(2分)
(5)设该KMnO4的纯度为y,根据化学方程式可知(3分)
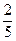 KMnO4―――Na2C2O4
KMnO4―――Na2C2O4
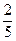 ×158? 134
×158? 134
0.165 × y? 0.335
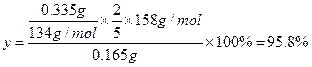
本题解析:略
本题难度:一般
3、填空题 已知氨气跟氯气可迅速反应生成氯化铵和氮气。当转移的电子总数为a个时,生成的氮气的物质的量bmol.

 ?(1)写出该反应配平的化学方程式:?
?(1)写出该反应配平的化学方程式:?
 ?(2)该反应中参加氧化还原反应的氧化剂和还原剂的物质的量之比为?。
?(2)该反应中参加氧化还原反应的氧化剂和还原剂的物质的量之比为?。
 ?(3)阿伏加德罗数常数为(用含a、b的代数式表示)?。
?(3)阿伏加德罗数常数为(用含a、b的代数式表示)?。
参考答案:(1)8NH3+3Cl2?6NH4Cl+N2(2)3:2 (3)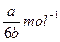
本题解析:根据电子转移守恒,配平的化学方程式8NH3+3Cl2?6NH4Cl+N2,根据化学方程式可知NH3为还原剂,Cl2为氧化剂,参加氧化还原反应的氧化剂和还原剂的物质的量之比为3:2.
本题难度:一般
4、选择题 1.52 g铜镁合金完全溶解于50 mL密度为1.40 g/mL、质量分数为63%的浓硝酸中,得到NO2和N2O4的混合气体1120 mL(标准状况)。向反应后的溶液中加入1.0 mol/L NaOH溶液,当金属离子全部沉淀时,得到2.54 g沉淀。下列说法不正确的是
A.该合金中铜与镁的物质的量之比是2?1
B.该浓硝酸中HNO3的物质的量浓度是14.0 mol/L
C.得到2.54 g沉淀时,加入NaOH溶液的体积是600 mL
D.NO2和N2O4的混合气体中,NO2的体积分数是80%
参考答案:C
本题解析:本题考查有关合金的化学计算,意在考查考生的化学计算能力。设合金中Cu、Mg的物质的量分别为x、y,根据题目所给信息知x×64 g/mol+y×24 g/mol=1.52 g ①;设金属为M,在反应过程中有:M-ne-===Mn+,Mn++OH-===M(OH)n↓,从而可以看出,金属单质失去电子的物质的量等于金属阳离子完全沉淀所需OH-的物质的量,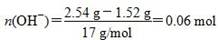 ,故2x+2y=0.06 mol ②,由①②解得x=0.02 mol,y=0.01 mol,显然A正确。
,故2x+2y=0.06 mol ②,由①②解得x=0.02 mol,y=0.01 mol,显然A正确。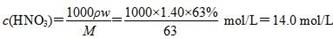 ,B正确。得到2.54 g沉淀时,消耗0.06 mol NaOH,其体积为60 mL,C错误。由上述分析可知,Cu、Mg共失去0.06 mol电子,根据得失电子守恒知,如果硝酸完全被还原为NO2,NO2的物质的量应为0.06 mol。现得到0.05 mol混合气体,是由于2NO2?N2O4,由差量法可求得N2O4为0.01 mol,则NO2为0.04 mol,显然D正确。
,B正确。得到2.54 g沉淀时,消耗0.06 mol NaOH,其体积为60 mL,C错误。由上述分析可知,Cu、Mg共失去0.06 mol电子,根据得失电子守恒知,如果硝酸完全被还原为NO2,NO2的物质的量应为0.06 mol。现得到0.05 mol混合气体,是由于2NO2?N2O4,由差量法可求得N2O4为0.01 mol,则NO2为0.04 mol,显然D正确。
本题难度:一般
5、填空题 利用I2O5可消除CO污染或定量测定CO,反应为:5CO(g)+I2O5(s) 5CO2(g)+I2(s);ΔH 1
5CO2(g)+I2(s);ΔH 1
(1)已知:2CO(g)+O2(g) 2CO2(g);ΔH 2
2CO2(g);ΔH 2
2I2(s)+5O2(g) 2I2O5(s);ΔH 3
2I2O5(s);ΔH 3
则ΔH 1=?(用含ΔH 2和ΔH 3的代数式表示)。
(2)不同温度下,向装有足量I2O5固体的2 L恒容密闭容器中通入2molCO,测得CO2的体积分数φ(CO2)随时间t变化曲线如图。请回答:

①从反应开始至a点时的反应速率为v(CO)=?,b点时化学平衡常数Kb=?。
②d点时,温度不变,若将容器体积压缩至原来的一半,请在图中补充画出CO2体积分数的变化曲线。
③下列说法正确的是?。(填字母序号)
A.容器内气体密度不变,表明反应达到平衡状态
B.两种温度下,c点时体系中混合气体的平均相对分子质量相等
C.增加I2O5的投料量有利于提高CO的转化率
D.b点和d点的化学平衡常数:Kb<Kd