1、推断题 有A、B、C、D、E五种元素,它们原子的核电荷数依次递增且均小于18;A原子核内仅有1个质子;B原子的电子总数与C原子的最外层电子数相等;C原子有两个电子层,最外层电子数是次外层电子数的3倍;D元素的最外层电子数是其电子层数的三分之一。E的单质是黄绿色气体且有毒。
(1)写出A分别与B、C所形成化合物的化学式:_______,_______。
(2)分别写出C和D的原子结构示意图:____________,______________。
(3)写出C、D、E所形成的化合物的电离方程式:_____________________。
(4)写出E的单质与A、C、D三元素所形成的化合物反应的化学方程式,若是氧化还原反应,请用双线桥标出电子转移的数目和方向:_____________________。
2、填空题 (A)
(1)在上图元素周期表中画出金属元素与非金属元素的分界线。
(2)根据NaH的存在,有人提议可以把氢元素放在 ⅦA族,那么根据其最高正价与最低负价的绝对值相等,又可把氢元素放在周期表中的____族。
(3)现有甲、乙两种元素,甲元素原子核外3p亚层上有5个电子,乙元素的焰色反应呈黄色。 ①用元素符号将甲、乙两元素填写在上图元素周期表中对应的位置上。
②甲元素与硫元素相比较,非金属性较强的是_______(填名称),写出可以验证该结论的一个化学方程式_____________________。
(B)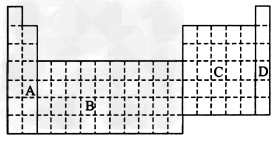
(4)在上图元素周期表中全部是金属元素的区域为____。
(5)有人认为形成化合物最多的元素不是ⅣA族碳元素,而是另一种短周期元素,请你根据学过的化学知识判断这一元素是____元素(填化学符号)。
(6)现有甲、乙两种短周期元素,室温下,甲元素的单质在冷的浓硫酸或空气中,表面都生成致密的氧化膜,乙元素原子核外M电子层与K电子层上的电子数相等。
①用元素符号将甲、乙两种元素填写在上图元素周期表中对应的位置上。
②甲、乙两元素相比较,金属性较强的是____ (填名称),可以验证该结论的实验是一__________(填序号)。
a.将在空气中放置已久的这两种元素的块状单质分别放入热水中
b.将这两种元素的单质粉末分别和同浓度的盐酸反应
c.将这两种元素的单质粉末分别和热水作用,并滴入酚酞试液
d.比较这两种元素的气态氢化物的稳定性
3、填空题 X、Y、Z、W均为短周期非金属主族元素,原子序数依次增大。Z的质子数等于X、Y质子数之和;W与Z最外层电子数相同,且W的电子总数是Z的电子总数的二倍。
(1)Y单质的结构式:___________其氢化物的空间结构呈________________形。
(2)X、Z元素可组成原子个数比为1∶1的化合物甲,其电子式为___________Z、W元素可组成质量比为
1∶1的化合物乙,甲与乙反应生成一种常见强酸丙,化学方程式为:________________;用惰性电极电解丙溶液的阳极反应式_______________________________ 。
(3)Y的氢化物与化合物乙有许多性质相似。结合图回答:如何通过它们溶于水时的现象不同来鉴别它们:________________________________。

(4)由X、Y、Z、W四种元素可组成多种离子化合物,其中有一种,溶于水时完全电离产生三种离子,且溶液呈酸性,0.1mol/L该盐溶液中,离子浓度由小到大的顺序是:_____________________。
4、选择题 第七周期为不完全周期,若将来的发现可把这一周期元素排满,则下列有关第七周期元素的推论正确的是
[? ]
A.第七周期排满时,最后一种元素的单质将很稳定
B.第七周期排满时,应该有32种元素
C.第七周期ⅡA族元素的氢氧化物性质与Al(OH)3相似
D.第七周期最后一种元素的原子序数为118
5、选择题 下列关于周期表的说法正确的是?
[? ]
A.在周期表中,族序数都等于该族元素的最外层电子数
B.同主族第三周期和第四周期原子序数都相差18
C.同周期ⅡA与ⅢA原子序数可能相差1、11、25?
D.周期表分为7个主族、7个副族和1个零族