1��ѡ���� ���й���ԭ��ص���������ȷ����
[? ]
A�������������������ֲ�ͬ�Ľ���?
B��ԭ����ǰѻ�ѧ��ת���ɵ��ܵ�װ��
C��ԭ��ع���ʱ�����������Ϸ����Ķ���������ԭ��Ӧ
D��п��ͭ�����ṹ�ɵ�ԭ��ع���ʱ��пƬ����6.5gп�ܽ⣬�����Ͼ���0.1g��������
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ���������缫����KOH��Һ�У��������ֱ�ͨ��H2��O2�����ɹ�������ȼ�ϵ�ء��õ�طŵ�ʱ�������й������У�����ȷ����
A��ͨ��H2�ĵ缫Ϊ����, ��缫��Ӧʽ�ǣ� H2��2OH����2H2O+2e��
B�������ĵ缫��Ӧʽ�ǣ�O2��2H2O��4e���� 4OH��,����������Ӧ
C��ȼ�ϵ�ع���ʱ��Һ�е����������ƶ�
D���õ�طŵ�ʱ,ÿ��Ӧ1mol������ת��2mol����
�ο��𰸣�B
�����������ȼ�ϵ���и���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�����������ڸ���ͨ�룬��ʧ���Ӿ����ߴ��ݵ������ϣ�������Һ�е��������������ƶ������������ƶ����õ���У��������ĵ缫��Ӧʽ�ֱ���O2��2H2O��4e���� 4OH����H2��2OH�D�D2e����2H2O������ѡ��B�Ǵ���ģ���ѡB��
�����Ѷȣ�һ��
3��ѡ���� Ϊ��ʹ��Ӧ2HCl+2Ag=2AgCl+H2����˳�����У�ijͬѧ����������ĸ�ʵ�飬��ͼ��ʾ������Ϊ���е��ǣ�������
A��
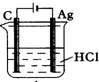
B��
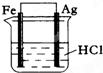
C��

D��
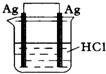
�ο��𰸣�C
���������
�����Ѷȣ���
4��ѡ���� ��ͼ��ʾ��Zn��Cu�γɵ�ԭ��أ�ijʵ����ȤС������ʵ����ڶ��鿨�ϵļ�¼���£���Ƭ�ϵ�������������?��?��

�� ʵ���ļ�¼��
��Cu������Zn����
��Cu���������ݲ�����������ԭ��Ӧ
��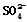 ��Cu���ƶ� ��Cu���ƶ�
������0.5mol�����������ߣ���ɲ���0.25mol����
�ݵ��ӵ������ǣ�Cu�D��Zn
��������Ӧʽ��Cu��2e��===Cu2��������������Ӧ
|
A���٢ڢ�? B���ڢۢ�? C���ڢ�? D���ۢܢ�
�ο��𰸣�C
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ�������Zn��Cuԭ����У�Zn��������������ط�ӦZn+2H+��Zn2++H2���������ɸ��������������������������ƶ���
ZnΪ������CuΪ�������ʢٴ���H+�������ƶ�����ͭ�缫�ϵõ����ӣ��ų��������ʢ���ȷ��SO42����п�缫�ƶ�������ѡ��۴���Cu�缫�Ϸ���2H++2e����H2�����ʢ���ȷ������0.5mol���������ߣ����������0.25mol���ʢ���ȷ��������Zn�缫����Cu�缫���ʢݲ���ȷ����ѡC��
�����������Ǹ߿��ֵij������ͺ���Ҫ�Ŀ��㣬��Ҫ�ǿ���ѧ����ԭ���ԭ�����缫���ơ��缫��Ӧʽ���˽����������ּ������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷԭ��صĹ���ԭ�����缫���жϡ������ĵ缫��Ӧ�����ӡ����ӵ��ƶ�����Ȼ��������������ü��ɡ�
�����Ѷȣ�һ��
5��ѡ���� ͭпԭ��أ�����ͼ������ʱ������������ȷ���� ��?��

A��������ӦΪ��Zn��2e-=Zn2+
B����ط�ӦΪ��Zn+Cu2+=Zn2+ +Cu
C�������·�У����Ӵ���������
D�������е�K+����ZnSO4��Һ
�ο��𰸣�B
���������ԭ����нϻ��õĽ����Ǹ�����ʧȥ���ӣ�����������Ӧ�����Ӿ����ߴ��ݵ�������������Һ�е��������������ƶ��������õ����ӣ�������ԭ��Ӧ��п��ͭ���ã��ݴ˿�֪����ԭ�����п�Ǹ�����ͭ����������Һ�е�ͭ�����������õ����ӣ�����ѡ��B����ȷ�ģ�����ѡ��Ǵ���ģ���ѡB��
�����������Ǹ߿��еij������ͣ������е��Ѷȵ����⡣���������ǿ�����ض�ѧ������֪ʶ�Ĺ� �̺�ѵ��������������ѧ�������������������ѧ��������û���֪ʶ���ʵ�����������������Ĺؼ�����ȷԭ��صĹ���ԭ����Ȼ��������������ü��ɡ�
�����Ѷȣ���