1、填空题 质能守恒定律包括______________定律和_____________定律。化学反应中能量变化的主要表现为
___________变化。化学反应中当断裂反应物中的化学键所吸收能量小于形成生成物中的化学键所放出能量时,则反应为_______________反应。当反应物中包含的化学能小于生成物中包含的化学能时,则反应为_____________反应。
2、选择题 氢气在氯气中燃烧时产生苍白色火焰。在反应过程中,断裂1 mol H2中的化学键消耗
的能量为Q1kJ,断裂1 mol Cl2中的化学键消耗的能量为Q2 kJ,形成1 mol HCl中的化学
键释放的能量为Q3 kJ。下列关系式中一定正确的是
A.Q1+Q2<Q3
B.Q1+Q2>2Q3
C.Q1+Q2=2Q3
D.Q1+Q2<2Q3
3、选择题 下列变化过程属于吸热反应的是(?)
(1) 液氨汽化 (2) 将胆矾加热变为白色粉末 (3) 浓硫酸稀释 (4) 氨催化氧化生成一氧化氮 (5) 酸碱中和生成水? (6) FeCl3溶于水显酸性
A.(1) (2) (6)
B.(1) (2) (4) (6)
C.(2) (5) (6)
D.(2) (4) ( 6)
4、选择题 下列说法正确是( )
A.由H原子形成1molH-H键要吸收热量
B.在稀溶液中,酸与碱发生中和反应生成H2O时所释放的热量称为中和热
C.N2性质非常稳定,是因为N2分子中含有氮氮叁键,要破坏氮氮叁键需吸收更多的能量
D.凡经加热而发生的化学反应都是吸热反应
5、填空题 (12分)下列三个反应在某密闭容器中进行:
反应①? Fe(s)+CO2(g) FeO(s)+CO(g)?△H1=" a" kJ・mol-1
FeO(s)+CO(g)?△H1=" a" kJ・mol-1
反应②? 2CO(g)+O2(g) 2CO2(g)?△H2=" b" kJ・mol-1
2CO2(g)?△H2=" b" kJ・mol-1
反应③? 2Fe(s)+O2(g) 2FeO(s)?△H3
2FeO(s)?△H3
(1)则△H3=?(用含a、b的代数式表示)
(2)已知500℃时反应①的平衡常数K=1.0,在此温度下2L密闭容器中进行反应①,Fe和CO2的起始量均为2.0mol,达到平衡时CO2的转化率为?
(3)将上述平衡体系升温至700℃,再次达到平衡时体系中CO的浓度是CO2浓度的两倍,则
a?0(填“>”、“<”或“=”)。为了加快化学反应速率且使体系中CO的物质的量增加,其它条件不变时,可以采取的措施有?(填序号)。
A.缩小反应器体积
B.再通入CO2
C.升高温度
D.使用合适的催化剂
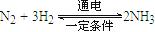 。则在电解法合成氨的过程中,应将H2不断地通入?极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为?。
。则在电解法合成氨的过程中,应将H2不断地通入?极(填“正”、“负”、 “阴” 或“阳”);在另一电极通入N2,该电极反应式为?。