1、选择题 实验室配制1mol・L-1盐酸250mL,下列不需用的仪是:
A.250ml容量瓶
B.托盘天平
C.胶头滴管
D.烧杯
参考答案:B
本题解析:盐酸是液体,不是固体,不需要称量,故不需要托盘天平,答案选B。
本题难度:简单
2、选择题 在实验室中,对下列事故或药品的处理正确的是
A.金属钠失火时可用水灭火
B.少量的金属钠应保存在煤油中
C.少量浓硫酸沾在皮肤上,立即用氢氧化钠溶液冲洗
D.有大量的氯气泄漏时,应用浸有弱碱性溶液的毛巾捂住口鼻向低处跑
参考答案:B
本题解析:A.金属钠能与水发生反应产生NaOH和氢气,反应放出热量,产生的氢气能够燃烧。因此Na失火时不可用水灭火,而应该用沙子或土来灭火。错误。B.由于Na的密度比煤油大,与煤油又不发生反应,放在煤油中可以隔绝空气及水。因此少量的金属钠应保存在煤油中。正确。C.少量浓硫酸沾在皮肤上,立即用干抹布擦干净,再用大量的水冲洗,最后涂上少量3%-5%的稀碳酸氢钠溶液。错误。D.有大量的氯气泄漏时,由于氯气的密度比空气大,所以应用浸有弱碱性溶液的毛巾捂住口鼻向高处跑。错误。
本题难度:一般
3、实验题 CuSO4・5H2O是铜的重要化合物,有着广泛的应用。以下是CuSO4・5H2O的实验室制备流程图。
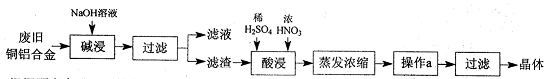
根据题意完成下列填空:
(1)“碱浸”的目的是?,写出有关的离子方程式?。
(2)向滤渣中先加入足量稀硫酸,然后再滴加少量浓硝酸,在废渣溶解时可以观察到的实验现象有?。
(3)操作a的名称为?,制得的CuSO4・5H2O中可能存在硝酸铜杂质,除去这种杂质的实验操作名称为?。
(4)已知:CuSO4+2NaOH=Cu(OH)2↓+ Na2SO4。称取0.26 g提纯后的CuSO4・5H2O试样于锥形瓶中,加入0.1000 mol/L氢氧化钠溶液28.00 mL,反应完全后,过量的氢氧化钠用0.1000 mol/L盐酸滴定至终点,耗用盐酸8.00 mL,则该试样中CuSO4・5H2O的质量分数为?;上述滴定中,滴定管在注入盐酸之前,先用蒸馏水洗净,再用?。
(5)在“酸浸”的步骤中,①若只加入浓硫酸,写出加热时的化学方程式?。
②若将浓硝酸换成过氧化氢,常温时即可生成硫酸铜,指出此种方法的优点?。
参考答案:
(1)溶解金属铝、除去油污? 2Al+2H2O+2OH-=2AlO2-+3H2↑
(2)金属溶解,溶液变蓝,有无色气体产生且在溶液上方变为红棕色
(3)冷却结晶?重结晶
(4)0.92?用标准盐酸润洗2~3次
(5)Cu+2H2SO4(浓)==CuSO4+SO2↑+2H2O
本题解析:(1)实验目的是利用废旧铝铜合金制备硫酸铜晶体,故应先除杂。碱浸即是除杂过程,除去表面的油污和溶解金属铝,离子方程式为2Al+2H2O+2OH-=2AlO2-+3H2↑;(2)加入少量浓硝酸后稀释,与铜反应,生成硫酸铜和NO气体,故现象为铜溶解,溶液变为蓝色,有无色气体产生并只溶液上方变为红棕色(变成NO2);(3)采用冷却结晶的方法分理出硫酸铜晶体,除去晶体中的可溶性杂质的方法是重结晶;
(4)与CuSO4的氢氧化钠的量n(NaOH)=28.00×0.1000×10-3-8.00×0.1000×10-3=2×10-3mol
n(CuSO4・5H2O) = n(NaOH)/2=10-3mol? w(CuSO4・5H2O)=10-3×250÷0.26=0.92
(5)过氧化氢是一种绿色氧化剂,相对浓硝酸而言不产生污染性气体,不产生杂质
本题难度:一般
4、选择题 下列物质的保存方法正确的是(? )
A.少量白磷保存在水中
B.氢氧化钠固体敞口放在空气中
C.生石灰露置于空气中
D.浓盐酸盛放在敞口玻璃瓶中
参考答案:A
本题解析:氢氧化钠可与空气中的二氧化碳反应,生石灰可与空气中的水蒸气及二氧化碳反应,浓盐酸则极易挥发。
本题难度:简单
5、实验题 (10分)为维持人体血液中的血糖含量,在给病人输液时,通常用葡萄糖注射液,下图是医院给病人输液时使用的一瓶质量分数为5%的葡萄糖(C6H12O6)注射液的标签。某学生欲在实验室中配制500 mL该葡萄糖注射液。
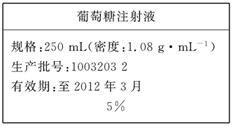
实验用品:葡萄糖晶体(摩尔质量:180 g/mol)、蒸馏水、烧杯、容量瓶(500 mL)、药匙、胶头滴管、量筒。
(1)还缺少的仪器有_?。
(2)下列对容量瓶及其使用方法的描述中正确的是_?_。
A.使用前要检查容量瓶是否漏水
B.容量瓶用蒸馏水洗净后,再用标准葡萄糖注射液润洗
C.配制溶液 时,把称好的葡萄糖晶体小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2 cm处,改用胶头滴管加蒸馏水至刻度线
时,把称好的葡萄糖晶体小心倒入容量瓶中,加入蒸馏水到接近刻度线1~2 cm处,改用胶头滴管加蒸馏水至刻度线
D.容量瓶上标有容积、温度和浓度
(3)实验中需取用晶体的质量为__?__,物质的量浓度_?_。
(4)配制0.1 mol/L的NaCl溶液,下列操作会导致所配溶液的物质的量浓度偏高的是__?。
A.没有将洗涤液转移到容量瓶? B.定容时俯视读取刻度
C.原容量瓶洗净 后未干燥? D.定容时液面超过了刻度线
后未干燥? D.定容时液面超过了刻度线
参考答案:(1)托盘天平、玻璃棒? (2)A
(3)27 g? 0.3 mol/L? (4)B
本题解析:略
本题难度:一般