1��ѡ���� ����ʵ������������ȷ���ǣ�������
A���Ȼ����백���������д����İ�������
B���ò�˿պȡ��������Һ���գ�����ʻ�ɫ
C��SO2ͨ��Ʒ����Һ����ɫ��ȥ���ټ��ȣ���ɫ���ٳ���
D���Ȼ�������Һ����ɫ��KSCN��Һ��ϣ���Һ�ʺ�ɫ
�ο��𰸣�B
���������
�����Ѷȣ�һ��
2��ѡ���� ����˵����ȷ���ǣ�������
A�����Ȼ�����Һ��ͨ��SO2��û�г�������ͨ��NO2��Ҳ����������
B������ˮ�����Һ©�����������Ҵ������ã��ɽ�����ȡ���Ҵ���
C�������£�Al��Cu��Ũ������Һ���ɵ�ԭ�����Al������
D������ǵı�����Һ�м�������̼���ƾ��壬����Һ�����
�ο��𰸣�D
���������
�����Ѷȣ�һ��
3������� ����ͼװ�ÿ��Խ��вⶨSO2ת����SO3��ת���ʵ�ʵ�飮��֪SO3���۵���16.8�棬�е���44.8�森��֪����װ�������漰��Ӧ�Ļ�ѧ����ʽΪ��Na2SO3��s��+H2SO4��85%���TNa2SO4+SO2��+H2O
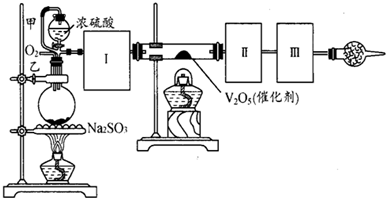
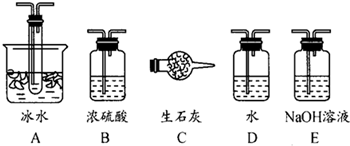
��1������ʵ����Ҫ��Ӧ���ڢ����Ӻ��ʵ�װ�ã����ͼA��Eװ����ѡ�����ʺ�װ�ò����������������Ŀո��У������ӵ�װ�÷ֱ���______��______��______��
��2�����Ҵ�����ͨ��O2��ΪʹSO2�нϸߵ�ת���ʣ�ʵ�����ڼ��ȴ�����μ�Ũ�����˳���У�����Ӧ��ȡ�IJ�����______��
��3����һС����ʵ���з��֣�SO2����������������º���ʵ���������ԣ����ֲ��������������⣬�����Ʋ���ܵ�ԭ��˵����Ӧ����֤���������Բ���������
��ԭ��______����֤����______��
��ԭ��______����֤����______��
��ԭ��______����֤����______��
��4����SO2ͨ�뺬1.5mol�������Һ�У�������һ��ǿ���һ�����������1.5��6.02��1023������ת��ʱ���÷�Ӧ�Ļ�ѧ����ʽ______��
��5����amolNa2SO3��ĩ������Ũ������д�ʵ�飬����Ӧ����ʱ������ͨ��O2һ��ʱ����װ�â�������bg����ʵ����SO2��ת����Ϊ______%���ú�a��b�Ĵ���ʽ��д��
�ο��𰸣���1��SO2ת����SO3֮ǰ����Զ���������и��������Ũ���ᣬSO3���۵���16.8�棬�е���44.8�棬���¶ȵ���?16.8��ʱ�����������Ծ���״̬���ڣ������������������β���������ռ���Һ���գ��ʴ�Ϊ��B��A��E��
��2��Ϊ��֤���ɵĶ��������ܶ��ת��Ϊ��������Ӧ�ȼ��ȴ����ٽ��еμ�Ũ�����������֤���ɵĶ��������ܵIJ��뷴Ӧ���ʴ�Ϊ���ȼ��ȴ����ٵ���Ũ���
��3��Ӱ��ѧ��Ӧ���ʵ������У�Ũ�ȡ��¶ȵȣ��������Ʊ��ʻ����������ƣ������ƺ�Ũ�����Ӧ�������������ƺ�ϡ���ᷴӦ�����Ķ����������ʻ���������ܵ�ԭ����Na2SO3���ʻ���Ũ�����ͨ��ȡ�����������Թ��У�������������ˮ�����Һ���μ�������ϡ���ᣬ�ټ����Ȼ�����Һ������а�ɫ�������ɣ���֤�������������ѱ��ʻ����ýྻ�IJ�����մȡ�����������ε���ֽ�ϣ��������ڣ���֤������Һ����Ũ���ᣬ
�ʴ�Ϊ��Na2SO3���ʣ�ȡ�����������Թ��У�������������ˮ�����Һ���μ�������ϡ���ᣬ�ټ����Ȼ�����Һ������а�ɫ�������ɣ���֤�������������ѱ��ʣ�����Ũ����ýྻ�IJ�����մȡ�����������ε���ֽ�ϣ��������ڣ���֤������Һ����Ũ���
��4��SO2ͨ�뺬1.0mol���������Һ�У�ת�Ƶĵ���Ϊ2mol��������1molSO2��1mol�����ᷴӦ������������ᣬ
�ʴ�Ϊ��SO2+H2O+HClO�THCl+H2SO4��
��5������Ԫ���غ�Na2SO3��SO2����amol�����ɶ�������amol��װ�â�������bg��˵��ʣ��Ķ�������Ϊbg
����bg64g/mol=b64mol�������Զ��������ת����=a-b64a��100%=1600a-25b16a%��
�ʴ�Ϊ��1600a-25b16a%������64a-b64a��100%����
���������
�����Ѷȣ�һ��
4��ѡ���� ����������ȷ���ǣ�������
A��SO2��Cl2��Ư��ԭ����ͬ
B��SO3����������
C�������£�Ũ�����ͭ��Ӧ������Ϊͭ���ۻ�
D�������������������桢�������Ũ����
�ο��𰸣�A��������������ɫ���ʻ��ϣ�������ˮ��Ӧ����HClO������ǿ�����ԣ�����ʹ��ɫ������ɫ����ԭ����ͬ����A����
B��SO3�У�SΪ+6�ۣ��ɵõ����ӣ����������ԣ���B��ȷ��
C�������£�Ũ�����ͭ��Ӧ�����ۻ�������������ԭ��Ӧ��Cuû�з����ۻ�����C����
D�������£�Fe��Ũ���ᷢ���ۻ�����ֹ��Ӧ�Ľ�һ��������������������������桢�������Ũ���ᣬ��D��ȷ��
��ѡD��
���������
�����Ѷȣ���
5��ѡ���� Ʈ��������ȼ��ʱ��������״Ʈ���������С�����׳��������������SO2��O2�Ӵ�ʱ��SO2�Ჿ��ת ��ΪSO3��ʹ������������ӣ�Ʈ����������ÿ�����
[? ]
A��������
B����ԭ��
C������
D��������
�ο��𰸣�CD
���������
�����Ѷȣ�һ��