1、选择题 对于可逆反应4NH3(g)+5O2(g)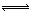 4NO(g)+6H2O(g)下列叙述正确的是(?)。
4NO(g)+6H2O(g)下列叙述正确的是(?)。
A.达到平衡时:4v正(O2)=5v逆(NO)
B.若单位时间内生成x mol NO的同时,消耗x mol NH3,则反应达到平衡状态。
C.达到平衡时,若增加容器容积,则正反应速率减小,逆反应速率增大
D.化学反应的速率关系是:2v正(NH3)=3v逆(H2O)
2、填空题 (14分)氢是一种重要的非金属元素。氢的单质及其化合物在科学研究和工业生产中有着广泛而重要的作用。
(1)某硝酸厂处理尾气中NO的方法是:催化剂存在时用H2将NO还原为N2。
已知:
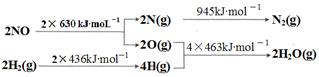
则H2还原NO生成氮气和水蒸气的热化学方程式是:
?。
(2)在一定条件下,用H2将二氧化碳转化为甲烷的反应如下:
CO2(g)+4H2 (g)  CH4 (g)+2H2O(g)
CH4 (g)+2H2O(g)
向一容积为2 L的恒容密闭容器中充人一定量的CO2和H2,在300℃时发生上述反应,达到平衡时各物质的浓度分别为CO2 0.2mol・L一1,H2 0.8mol・L一1,CH40.8mol・L一1,H2O1.6mol・L一1。则CO2的平衡转化率为?。上述反应的平衡常数表达式K=?。200℃时该反应的平衡常数K=64.8,则该反应的△H?0(填“>’’或“<”)。
(3)某研究小组以H2与CaCl2制备某种钙的化合物。已知反应只生成甲、乙两种化合物。对产物分析发现:化合物甲的组成中钙、氯元素的质量分数分别为52.29%、46.41%,化合物乙的水溶液显酸性。请回答下列问题:
①乙的化学式为?。
②甲与水反应可得H2,其化学方程式是:
?。
(4)H2的获得途径很多,由哈工大研究小组设计的微生物电解有机废水法,既可以清除废水中的有机杂质,同时可以获得氢气。下图为一种处理含甲醇工业废水的微生物电解池,写出电解过程中,阳极发生的电极反应式:?。

3、填空题 (16分)环境中常见的重金属污染有:汞、铅、锰、铬、镉。处理工业废水中常含有的Cr2O2-7和CrO2-4离子,常用的方法有两种。
方法1:还原沉淀法
该法的工艺流程为:
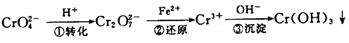
其中第①步存在平衡:

(1)写出第①步反应的平衡常数表达式?。
(2)关于第①步反应,下列说法正确的是?。
A.通过测定溶液的pH值可以判断反应是否已达平衡状态
B.该反应为氧化还原反应
C.强酸性环境,溶液的颜色为橙色
(3)第②步中,还原0.1 molCr2O2-7离子,需要?mol的FeSO4・7H2O。
(4)第③步除生成的Cr(OH)3,还可能生成的沉淀为?。在溶液中存在以下沉淀溶解平衡: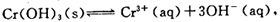 常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH值调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)
常温下,Cr(OH)3的溶度积Ksp=10-32,当c(Cr3+)降至10-5mol/L,认为c(Cr3+)已经完全沉淀,现将第③步溶液的pH值调至4,请通过计算说明Cr3+是否沉淀完全(请写出计算过程)
?
?
方法2:电解法
(5)实验室利用如图装置模拟电解法处理含Cr2O2-7的废水,电解时阳极反应式为?,阴极区反应式为?,得到的金属阳离子在阴极区可沉淀完全,从水的电离平衡角度解释其原因是?。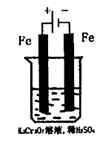
4、选择题 能证明反应:H2(g)+ I2(g)  2HI(g)已经达到平衡状态的是
2HI(g)已经达到平衡状态的是
①c(H2):c(I2):c(HI)=1:1:2
②单位时间内生成nmolH2的同时消耗nmolI2
③反应速率2v(H2)=2v(I2)= v(HI)
④温度和体积一定时,容器内压强不再变化
⑤温度和压强一定时,混合气体的密度不再变化
⑥温度和体积一定时,混合气体的颜色不再变化
A.①③
B.②⑥
C.③⑥
D.④⑤
5、选择题 一定温度下,固定体积的密闭容器中发生下列反应:?2HI(g)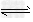 H2(g)+I2(g),若c(HI)由0.1?mol/L降到0.07?mol/L需要15?s,那么c(HI)由0.07?mol/L降到0.05?mol/L,需要的时间为
H2(g)+I2(g),若c(HI)由0.1?mol/L降到0.07?mol/L需要15?s,那么c(HI)由0.07?mol/L降到0.05?mol/L,需要的时间为
[? ]
A.等于5?s?
B.等于10?s
C.大于10?s?
D.小于10?s