1��ѡ���� �ɷǽ���Ԫ����ɵĻ�����(? )
A��һ���ǹ��ۻ�����
B��һ�������ӻ�����
C����������ԭ�Ӿ���
D�����������Ӿ���
�ο��𰸣�D
����������ɷǽ���Ԫ����ɵ����ʿ�����NH4Cl��NH4NO3(���Ӿ���)��H2O(���ۻ�����)�����ʯ(ԭ�Ӿ���)��
�����Ѷȣ�һ��
2������� ��7�֣���MgCl2?�ڸɱ��۱�?��Na2O2?�ݰ��ף�P4�������?��Na2CO3?����ʯ?��NaOH?��SiO2
(1)�����������������Ӿ������?��(2)���ڷ��Ӿ������?��(3)����ԭ�Ӿ������______��������ţ���
�����������У���1����Ϊͬ���칹�����?����2����Ϊͬ�����������?����3������ͬλ�ص���?����4������ͬһ�����ʣ����������ͬ������?��(��?�����)
��Һ��?��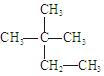 �۰���?������?��
�۰���?������?��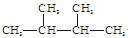
��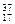 Cl?��
Cl?��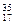 Cl?�����
Cl?�����
�ο��𰸣�ÿ��1�֣���7�֡�
��1���٢ܢߢ�?��2���ڢۢݢ�?��3�����
��1���ڢ�?��2���ۢ�?��3���ޢ�?��4���٢�
�����������
�����Ѷȣ�һ��
3��ѡ���� ��������Ҫ���ྻ����Դ��Ҫ������������Դ�����밲ȫ��Ч�ش����������б�����ij�ֺϽ�����нϴ�Ĵ����������侧��ṹ����С��Ԫ����ͼ��ʾ�������ֺϽ�Ļ�ѧʽΪ
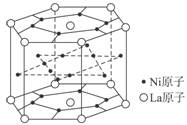
A��LaNi6
B��LaNi3
C��LaNi4
D��LaNi5
�ο��𰸣�D
������������ü�������⡣���ڲ���ԭ�ӣ���ȫ���ڸþ��壻�����ϵ�ԭ�ӣ�ֻ���ھ����1/2���ڶ����ϵ�ԭ�ӣ����ڸþ����1/6��
�����Ѷȣ�һ��
4��ѡ���� ���и����У����ɡ����ۼ������ϵ����ȷ����
ѡ��
| ����
| ����
|
A
| ���ܣ�N��N��Cl��Cl
| ���ʷе㣺N2��Cl2
|
B
| �����пɵ����H+������H2SO4��CH3COOH
| ���ԣ�H2SO4��CH3COOH
|
C
| Ԫ�صķǽ����ԣ�N��P
| ���ԣ�HNO3��H3PO4
|
D
| �����ԣ�Fe3+��Cu2+
| ��ԭ�ԣ�Fe2+��Cu
|
?
�ο��𰸣�C
������������Ӿ���ļ��ܾ��������ǵ��ȶ��ԣ������Ӽ��������������ܷе㣬����B�����Ե�ǿ����������H+�����׳̶��йأ���ÿ�����ӵ����H+�����أ�����C��Ԫ�صķǽ�����Խǿ��������������Ӧˮ���������Խǿ����ȷ��D��һ����˵����������Խǿ�����Ӧ�ĵõ��Ӻ�Ļ�ԭ������ԭ�Ծ�Խ������Fe2+��Cu������
�����Ѷȣ���
5������� ��֪�й����ʵ��ܡ��е��������±���ʾ��
������
| MgO
| Al2O3
| MgCl 2
| AlCl3
|
�۵㣯��
| 2852
| 2072
| 714
| 190(2.5*105Pa)
|
�е㣯��
| 3600
| 2980
| 1412
| 182.7
|
��ο�����������պͻش����⣺
��1����ҵ�ϳ��õ������MgCl 2�ķ�����������þ�����Al2O3�����ʯ���ڻ����ķ�����������Ϊʲô���õ��MgO�ķ�������þ��Ҳ���õ��AlCl3�ķ�����������
��__________________________________________________________________
(2)�Ȼ�����________________(�������)
��3����500K��1.01*105Paʱ���Ȼ����������ܶȣ�����Ϊ��״��ʱ��Ϊ11.92g/L����ȷ���Ȼ���������״̬ʱ�Ļ�ѧʽΪ___________________
��4����ˮ�Ȼ����ڿ����о��ҡ����̡�����ԭ����________________
(5)��ƿɿ���ʵ��֤��MgCl 2��AlCl3�����ľ������ͣ���ʵ�鷽����_____________.
�ο��𰸣���1����ΪMgO���۵�Զ����MgCl 2�����Ե�����ڵ�MgNa��Ҫ�ṩ��������������ߵ��¶ȣ������ڲ������ӱ������ݿ��Է��֣�AlCl3������۵�ܵͣ������������ڷ��Ӿ��壬���������ӣ�����ʱ���ܵ��磬���ܱ���⡣
��2�����ڷ��Ӿ���
��3�������Ȼ����������ܶȿ��������Ħ������������ȷ����ѧʽ
M=�ѩ~Vm=11.92g/L��22.4L/mol=267g/mol,���Ի�ѧʽΪAl2Cl6
��4����ˮ�Ȼ����ڿ�������ˮ����ˮ�ⷴӦ����HCl���壬HCl�ڿ������γ������������̡�
��5�������־�����ȵ��ۻ�״̬��MgCl 2�ܵ����AlCl3���ܵ��磬�ʿ�֤��MgCl 2Ϊ���Ӿ��壬AlCl3Ϊ���Ӿ��塣
�������������ͬ��
�����Ѷȣ�һ��