1、选择题 下列说法正确的是
[? ]
A.NH4NO3溶于水虽然吸热,但其溶于水是自发过程
B.过热液体(温度高于沸点)会自发转变成气体,可用焓变解释
C.对于同一物质来讲,熵值的大小与其状态有关,固态物质的熵值通常最大
D.有序火柴散落的自发过程可用能量判据解释
参考答案:A
本题解析:
本题难度:一般
2、选择题 下列说法正确的是( )
A.能自发进行的反应一定能迅速发生反应
B.非自发进行的反应一定不可能发生反应
C.能自发进行的反应实质可能没有发生反应
D.常温下,2H2O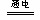 2 H2↑+O2↑,即常温下水的分解反应是自发反应
2 H2↑+O2↑,即常温下水的分解反应是自发反应
参考答案:C
本题解析:△H-T△S这个判据指的是在温度、压强一定的条件下,化学反应自动发生的趋势,即反应发生的可能性,它并不能说明在该条件下一个可能自发进行的化学反应能否实际发生,因为化学反应能否实际发生还设计到反应速率问题,所以,A不正确。非自发不含有“不可能”之意,所以B错误。水在常温、常压下电解才会发生分解,即需要外界对它作功才能分解,所以是非自发的反应,故D错误。
本题难度:简单
3、选择题 下列说法正确的是
A.可逆反应在其他条件不变时,升高温度,可以减小反应的活化能,加快反应速率
B.S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表一个电子
C.氮原子的第一电离能低于氧原子的第一电离能,因为氮比氧非金属性弱
D.Fe3+比Fe2+稳定,因为Fe3+价电子构型是3d5,d亚层处于半充满状态,稳定
参考答案:D
本题解析:可逆反应在其他条件不变时,升高温度,可以增大活化分子的百分数,加快反应速率,A错;S电子云是球形对称的,P电子云是纺锤形,电子云中每个小黑点代表电子出现的几率,B错;氮原子的第一电离能低于氧原子的第一电离能,这个根据结构化学来解释。氮的结构是1S2 2S2 2P3。P轨道正好为半满结构,比碳和氧都稳定。然后还要注意除了第五主族和第六主族,第二主族和第三主族也会出现电能不规则排布。C错。故选D。
点评:熟练掌握原子、离子的电子排布规律,尤其是半满,全满的离子排布给离子带来的特殊性质。
原子核外电子排布有3大原则1、Pauli不相容原理:每个轨道最多只能容纳两个电子,且自旋相反配对。
2、能量最低原理:电子尽可能占据能量最低的轨道
3、Hund规则:简并轨道(能级相同的轨道)只有被电子逐一自旋平行地占据后,才能容纳第二个电子另外:等价轨道在全充满、半充满或全空的状态是比较稳定的,亦即下列电子结构是比较稳定的:全充满---p6或d10或f14半充满----p3或d5或f7
Ni的基态原子外围电子(价电子)排布为3d84s2符合半满全满规则,而离子外围就是全满的所以满足的,很稳定。
本题难度:简单
4、选择题 下列说法中,正确的是 ( )
A.自发过程一定会导致熵增加
B.能够自发进行的反应一定都是放热反应
C.化学反应除了生成新的物质外,还伴随着能量的变化
D.能够自发进行的反应一定能够发生并完成