|
高考化学知识点归纳《电解池原理》试题强化练习(2020年最新版)(六)
2020-08-23 06:35:44
【 大 中 小】
|
1、选择题 下列关于下图装置的说法正确的是

A.若断开K1关闭K2,X、Y均为石墨,Z是NaCl溶液,则X 附近能得到氢氧化钠
B.若断开K1关闭K2,X是纯铜,Y是粗铜,Z是CuSO4溶液,则该装置可用于铜的精炼
C.若断开K2关闭K1,X是Cu,Y是Fe,Z是含有空气的海水,则该装置可用于保护Fe
D.若断开K2关闭K1,X是Cu,Y是Zn,Z是稀H2SO4,则在X极有气泡生成。
|
参考答案:D
本题解析:A.若断开K1关闭K2则构成电解池,X、Y均为石墨,Z是NaCl溶液,X 是阳极,氯离子放电生成氯气,错误;B.若断开K1关闭K2则构成电解池,X是阳极,电极材料为粗铜,Y是精铜,Z是CuSO4溶液,才可用于铜的精炼,错误;C.若断开K2关闭K1则构成原电池,X是Cu,Y是Fe,Z是含有空气的海水,铁比铜活泼做负极,受到腐蚀,该装置不能用于保护Fe,错误;D.若断开K2关闭K1则构成原电池,X是Cu,Y是Zn,Z是稀H2SO4,锌比铜活泼,则在X极有气泡生成,正确;选D。
考点:考查原电池、电解池的工作原理。
本题难度:一般
2、填空题 某化学兴趣小组在实验室条件下以硫酸铜溶液为电解液,用电解的方法实现了粗铜(含有少量的锌、铁、银、金等金属和少量矿物杂质)的提纯,并对阳极泥和电解液中金属进行回收和含量测定。请回答以下问题。
(1)电解时,粗铜应与电源的 极相连,阴极上的电极反应式为 ;电解过程中,硫酸铜的浓度会 (选填“变大”“不变”或“变小”)。
(2)电解完成后,该小组同学将电解液过滤后对滤液和阳极泥分别进行处理:
①阳极泥的综合利用:稀硝酸处理阳极泥得到硝酸银稀溶液,请你写出该步反应的离子方程式: 。
②Cu的回收、滤液成分及含量的测定:以下是该小组设计的一个实验流程。

在上述流程中空格内填上相应的操作: 、 ;100 mL滤液中Cu2+的浓度为 mol/l,Fe2+的浓度为 mol/l。
参考答案:(1)正 Cu2++2e-=Cu 变小 (2) ① 3Ag+4H++NO3-=3Ag++NO+2H2O ② 过滤 洗涤 0.5 0.1
本题解析:(1)电解时,粗铜应与电源的正极极相连,作阳极;阴极上铜离子得到电子,电极反应式为Cu2++2e-=Cu;由于阳极粗铜中还有活泼的金属失去电子,而阴极上始终是溶液中的铜离子放电,因此电解过程中,硫酸铜的浓度会变小;
(2)①金属银可以和稀硝酸反应生成硝酸银、一氧化氮和水,即3Ag+4H++NO3-=3Ag++NO↑+2H2O;
②100mL的滤液中含有亚铁离子、铜离子、锌离子,当加入足量的金属Fe以后,会将金属铜全部置换出来,所得固体是铁与铜的混合物。酸浸后铁溶解,要得到金属铜,需要进行的操作是过滤、洗涤、干燥、称量,所以生成的3.2g金属是Cu,物质的量是3.2g÷64g/mol=0.05mol,所以铜离子的浓度c=0.05mol÷0.1L=0.5 mol/L;亚铁离子和氢氧化钠反应生成氢氧化亚铁,在空气中更易被氧化为氢氧化铁,受热分解生成的氧化铁的质量是4.8g,物质的量是4.8g÷160g/mol=0.03mol。根据原子守恒,亚铁离子的物质的量是:0.03mol×2=0.06mol。其中与铜离子反应的铁的物质的量是0.05mol,生成亚铁离子的物质的量是0.05mol,所以原溶液中亚铁离子的物质的量是0.06mol-0.05mol=0.01mol,浓度c=0.01mol÷0.1L=0.1mol/L。
考点:考查电解精炼铜以及物质的含量测定的实验方案设计
本题难度:一般
3、填空题 碳及其化合物有广泛应用。
(1)工业冶炼铝,以石墨为阳极。阳极反应式为 ,可能发生副反应有 。
(2)一氧化碳和空气在酸性介质中构成燃料电池,负极反应式为 。
(3)向75 mL 4 mol?L-1KOH溶液中缓慢通入4480 mL CO2气体(标准状况)恰好完全被吸收。①写出该反应的离子方程式: 。(只用一个离子方程式表示)
②该吸收溶液中离子浓度大小排序为 。
(4)已知:① 2H2(g)+O2(g)=2H2O(l) △H1=―571.6kJ?mol-1
② 2CO(g)+O2(g)=2CO2(g) △H2 = ―566.0kJ?mol-1
③ CO(g)+2H2(g) CH3OH(g) △H3 = ―90.8kJ?mol-1 CH3OH(g) △H3 = ―90.8kJ?mol-1
计算甲醇蒸气的燃烧热 = 。 = 。
(5)某温度下,发生可逆反应:CO(g)+H2O(g) CO2(g)+H2(g) CO2(g)+H2(g) 
①向某容器中充入1.0 molH2和1.0 molCO2(g),在一定条件下发生上述反应。混合气体中CO的物质的量与时间关系如下列所示:
| 0
| 5 min
| 10 min
| 15 min
| 20 min
| 25 min
| I(800℃)
| 1.0
| 0.80
| 0.70
| 0.65
| 0.50
| 0.50
| II(800℃)
| 1.0
| 0.7
| 0.60
| 0.50
| 0.50
| 0.50
|
相对实验I,实验II可能改变的条件可能是 ,该温度下,平衡常数= 。
②若开始向绝热容器中投入一定量二氧化碳、氢气在一定条件下发生上述可逆反应。
下列图像正确且说明可逆反应达到平衡状态的是 。(填序号)
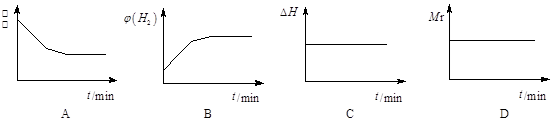
参考答案:(11分)
(1)2O2---4e-=O2↑(1分) C+O2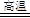 CO2(或2C+O2 CO2(或2C+O2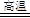 2CO)(1分) 2CO)(1分)
(2)CO-2e-+H2O=CO2+2H+(1分)
(3)① 2CO2+3OH--=CO32--+HCO3--+H2O(2分)
②c(K++)>c(HCO3--)>c(CO32--)>c(OH--)>c(H++)(2分)
(4)-763.8 kJ?mol-1(1分)
(5)①增大压强(或缩小体积)、加催化剂(1分) 1(1分) ② A(1分)
本题解析:(1)以石墨为阳极,电解氧化铝冶炼铝,所以阳极是O2-发生氧化反应,反应式为2O2---4e-=O2↑;因为用石墨作阳极,所以可能发生的副反应是C与生成的氧气发生反应生成二氧化碳或一氧化碳,C+O2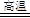 CO2(或2C+O2 CO2(或2C+O2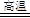 2CO); 2CO);
(2)一氧化碳和空气在酸性介质中构成燃料电池,则CO在该反应中作还原剂,发生氧化反应,结合电解质溶液,所以负极的电极反应式为CO-2e-+H2O=CO2+2H+;
(3)①4480mL的二氧化碳气体的物质的量是0.2mol,75 mL 4 mol?L-1KOH溶液中KOH的物质的量是0.3mol,所以该反应中有0.1mol碳酸钾和0.1mo碳酸氢钾,故离子方程式为2CO2+3OH--=CO32--+HCO3--+H2O;
②该吸收溶液为等浓度的碳酸钾和碳酸氢钾的混合液,溶液呈碱性,其中碳酸根离子的水解程度大于碳酸氢根离子的水解程度,所以混合液中离子浓度大小排序为c(K++)>c(HCO3--)>c(CO32--)>c(OH--)>c(H++);
(4)根据盖斯定律可得甲醇蒸气的燃烧热 =①+②/2-③=△H1+△H2 /2-△H3 =-763.8 kJ?mol-1; =①+②/2-③=△H1+△H2 /2-△H3 =-763.8 kJ?mol-1;
(5)①该反应是反应前后气体的物质的量不变的可逆反应,根据表中数据可知,实验II与实验I达到的平衡状态相同,但缩短了反应时间,说明反应速率加快,所以可能改变的条件是使用了催化剂、或者增大压强(缩小容器的体积);该温度下,平衡时各气体的物质的量浓度均相同,所以平衡常数为1;
②A、在绝热的容器中,加入一定量二氧化碳、氢气,反应逆向进行,逆向为放热反应,因为该容器绝热,使体系温度升高,则反应又正向进行,而正向是吸热反应,所以开始的温度最高后逐渐降低,达平衡时不再下降,正确;B、反应逆向进行,氢气的浓度逐渐减小直至不变,错误;C、对于该反应而言,反应放热,所以△H逐渐增大,达平衡时不再增大,错误;D、对于该反应而言,混合气体的相对分子质量始终不变,不能作为平衡状态的标志,错误,答案选A。
考点:考查电解质溶液、电化学反应原理、热化学的知识的应用
本题难度:一般
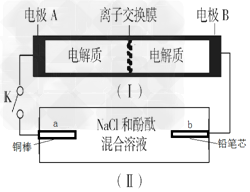
4、选择题 下图所示装置Ⅰ是一种可充电电池,装置Ⅱ为电解池。离子交换膜只允许Na+通过,充放电的化学方程式为2Na2S2+NaBr3 Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是? Na2S4+3NaBr。闭合开关K时,b极附近先变红色。下列说法正确的是?
[? ]
A.当有0.01?mol?Na+通过离子交换膜时,b电极上析出标准状况下的气体112?mL
B.负极反应为4Na-4e-=4Na+
C.闭合K后,b电极附近的pH变小
D.闭合K后,a电极上有产生氢气
参考答案:A
本题解析:
本题难度:一般
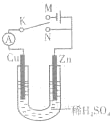
5、选择题 如图所示,将Zn棒和Cu棒插入1L?2mol?L-1稀H2SO4中下列说法正确的是( )
A.若电键K与N连接,由于发生原电池反应,Zn棒被保护不会腐蚀
B.若电键K与N连接,Zn棒上发生的反应是2H+-2e-=H2↑
C.若电键K与M连接,将稀H2SO4换成CuSO4溶液,可实现Zn棒上镀铜
D.若电键K与M连接,Cu棒上发生还原反应
|