1、填空题 已知元素的电负性和原子半径等内容一样,也是元素的一种基本性质,下面给出14种元素的电负性
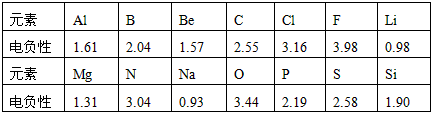
试结合元素周期律知识完成下列问题:
(1)根据上表给出的数据,可推知元素的电负性具有的变化规律是:_____________________________
(2)预测Br与I元素电负性的大小关系_________,电负性最小的元素在周期表中的位置是_________(放射性元素除外)。
参考答案:(1)同周期主族元素电负性从左到右增大,同主族元素电负性从上到下减弱(或元素非金属性越强电负性越大,金属性越强电负性越弱小)
(2)Br>I;第六周期第ⅠA族
本题解析:
本题难度:一般
2、选择题 某元素M的逐级电离能(kJ/mol)分别为580、1820、2750、11600.该元素氧化物的化学式最可能是( )
A.MO
B.MO2
C.MO3
D.M2O3
参考答案:D
本题解析:
本题难度:简单
3、选择题 下列对电负性的理解不正确的是
[? ]
A.电负性是人为规定的一个相对数值,不是绝对标准
B.元素电负性的大小反映了元素对键合电子吸引能力的大小
C.元素的电负性越大,则元素的非金属性越强
D.元素的电负性是元素固有的性质,与原子结构无关
参考答案:D
本题解析:
本题难度:一般
4、选择题 已知A、B元素同周期,且电负性A<B,下列说法正确的是
[? ]
A.A与B形成化合物时,A显正价,B显负价且A原子的半径小于B原子的半径
B.A与B形成的共价化合物分子一定是极性分子
C.气态氢化物的稳定性:HmB小于HnA
D.最高价含氧酸的酸性:A对应的酸性弱于B对应的酸性
参考答案:D
本题解析:
本题难度:一般
5、填空题 (三选一)【物质结构与性质】
A、B、C、D分别代表四种不同的短周期元素。A元素的原子最外层电子排布为ns1,B元素的原子价电子排布为ns2np2,C元素的最外层电子数是其电子层数的3倍,D元素原子的M电子层的P亚层中有3个电子。
(1)C原子的电子排布式为____________,若A元素的原子最外层电子排布为1s1,则按原子轨道的重迭方式,A与C形成的化合物中的共价键属于________键。
(2)当n=2时,B的原子结构示意图为____________,B与C形成的晶体属于__________?晶体。当n=3时,B与C形成的晶体中微粒间的作用力是_______________
(3)若A元素的原子最外层电子排布为2s1,B元素的原子价电子排布为3s23p2,元素A在周期表中的位置是__________,A、B、C、D四种元素的第一电离能由大到小的顺序是_______________?(用元素符号表示)。
参考答案:(1)1s22s22p4;σ?
(2)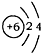 ;分子;共价键或极性共价键
;分子;共价键或极性共价键
(3)第2周期I?A族;O>P>Si>Li
本题解析:
本题难度:一般