1��ѡ���� ��ȥNaCl�л��е�MgCl2��Na2SO4ѡ�õĻ�ѧҩƷ�ǣ���
A��NaOH ��Ba(NO3)2
B��Ca(OH)2��AgNO3
C��NaOH��BaCl2
D��Na2CO3��BaCl2
2������� �����ͷ�ˮ���ؽ���Ԫ�ظ��Ķ��ԣ��ɽ�Cr2O72-ת��ΪCr��OH��3������ȥ�����ֽ����������ɳ�����pH�����
| ��ʼ������pH | ��ȫ������pH
Fe��OH��2
7.0
9.0
Fe��OH��3
1.9
3.2
Cr��OH��3
6.0
8.0
|
��1��ij������ˮ��������Ҫ������ͼ��ʾ��
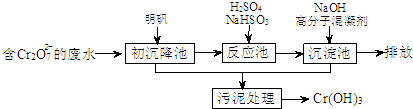
�ٳ������м����������������������õ�ԭ���ǣ������ӷ���ʽ��ʾ��______��
���벹�䲢��ƽ���·�Ӧ���з�����Ҫ��Ӧ�����ӷ���ʽ��
______Cr2O72-+______HSO3-+______�T______Cr3++______SO42-+______H2O��
�۸��ݡ����������͡��кͷ�����ԭ������������м���NaOH��Һ���˹����з�����Ҫ��Ӧ�����ӷ���ʽ�ǣ�H++OH-=H2O��______��֤��Cr3+������ȫ�ķ�����______��
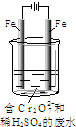
��2����ҵ���õ�ⷨ��������Cr2O72-��ˮ��ʵ����������ͼģ�����Cr2O72-�ķ�ˮ��������Ӧ��Fe-2e-=Fe2+��������Ӧʽ��2H++2e-=H2����
��Fe2+��������Һ�е�Cr2O72-��Ӧ�����ӷ���ʽ��______��
��������Ӧ�õ��Ľ������������������ɳ�����ȫ�������ˮ�ĵ���ƽ��ǶȽ�����ԭ��______��
������Һ�к���0.01molCr2O72-����������ȫ�����ɳ��������ʵ�����______mol��
3��ʵ���� ij�о���ѧϰС����ʵ��ʱżȻ���֣������ȥ����Ĥ��þƬ����NaHCO3��Һ��Ӧ������������Ͱ�ɫ�������С��ͬѧͨ������ʵ�飬��֤���ﲢ̽����Ӧԭ����
ʵ��٣���ɰֽ��ȥþ����������Ĥ���������ʢ�������з�̪��Һ�ı���̼��������Һ���ձ��У�Ѹ�ٷ�Ӧ�������������ݺͰ�ɫ�������Һ��dz��ɫ���
����ʵ��
��1������ļ���?
ʵ��ڣ���ʵ������ռ����������ȼ���������尲��ȼ�գ�����ʵ���ɫ��������Ϊ?��
��2����С��ͬѧ�Է�Ӧ�в����İ�ɫ�������������²²⣺
�²�1����ɫ���������Ϊ����������??
�²�2����ɫ���������ΪMgCO3
�²�3����ɫ���������Ϊ��ʽ̼��þ[yMg(OH)2?xMgCO3]
�����һ��ʵ�����������Ƿ���MgCO3��д��ʵ�����������ͽ��ۣ�?��
��3��ʵ��ۣ�ȡʵ����е���Һ�������м�������CaCl2ϡ��Һ��������ɫ��������Һ��ɫ��dz��˵����Һ�д���CO32�����ӡ�
����ʵ��
��4��Ϊ��һ��ȷ��ʵ��I�İ�ɫ������ijɷ֣��������¶�ʵ�飬װ����ͼ��ʾ��

��ȡ��������İ�ɫ������ 7.36 g����ּ��������ٲ�������Ϊֹ����ʹ�ֽ����������ȫ������װ��A��B�С�ʵ���װ��A����0.72g��װ��B����2.64 g����ɫ������Ļ�ѧʽΪ?��
��5��д��þ�뱥��̼��������Һ��Ӧ�Ļ�ѧ����ʽ?��
��Ӧԭ������
��6��NaHCO3��Һ�д������µ���ƽ�⣺H2O H+ + OH����HCO3��
H+ + OH����HCO3�� H+ +CO32�������ƽ���ƶ��Ƕȷ���ʵ��ٲ�����������Ͱ�ɫ�������ԭ��?��
H+ +CO32�������ƽ���ƶ��Ƕȷ���ʵ��ٲ�����������Ͱ�ɫ�������ԭ��?��
4��ѡ���� ����ʵ���������ȷ����
ѡ��
| ʵ�����������
| ʵ�����
|
A
| ��ij��Һ�м���μ�BaCl2��Һ������������ɫ������
| ԭ��Һ��һ����SO42��
|
B
| ��K2CrO7��Һ�м���NaOH��Һ����Һ�ɳ�ɫ��Ϊ��ɫ��
| K2CrO7��NaOH��Һ������������ԭ��Ӧ
|
C
| �ڵ��з�̪��Na2CO3��Һ�У��μ���BaC12��Һ����Һ��ɫ����ȥ��
| Na2CO3��Һ�д���ˮ��ƽ��?
|
D
| �ò�˿պȡ��Һ������ɫ��Ӧ���۲쵽����ʻ�ɫ��
| ����Һһ����������Һ?
|
?
5��ѡ���� �����й�ʵ��Ľ�����ȷ����
ѡ��
| ʵ�����������
| ʵ�����
|
A
| ��ij��Һ�м��������ữ���Ȼ�����Һ���а�ɫ��������
| ��Һ��һ������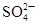
|
B
| ��ij��Һ�м������ᣬ������ʹ����ʯ��ˮ����ǵ���ɫ����
| ��Һ��һ������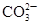
|
C
| ����ȼƲⶨSO2��CO2������Һ��pH��ǰ��pHС
| H2SO3����ǿ��H2CO3
|
D
| �ò�����պȡŨ��ˮ�㵽��ɫʯ����ֽ�ϣ���ֽ����ɫ
| Ũ��ˮ�ʼ���
|
?