1、选择题 以下说法正确的是( )。
A.海洋约占地球表面积的71%,所以地球上不缺水,人类可以随意使用水资源,不必节约
B.海水淡化的主要方法有蒸馏法、电渗析法、离子交换法
C.海水淡化的各种方法中,蒸馏法的成本比较低
D.以上说法都正确
参考答案:B
本题解析:地球上的淡水资源才是我们可以直接利用的水资源,其资源量很少,我们必须节约用水,A错。常见的海水淡化方法有蒸馏法、电渗析法、离子交换法,蒸馏法因其高耗能而成本高,C错。
本题难度:简单
2、填空题 (12分)综合利用海水可以制备食盐、纯碱、金属镁、溴等物质,其流程如下图所示:
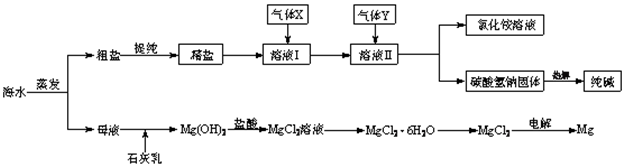
(1)粗盐中含有硫酸钠、氯化镁、氯化钙等可溶性杂质,为除去这些杂质而得精盐,进行如下操作:①溶解;②加过量的BaCl2溶液;③加过量的NaOH溶液;④加过量的Na2CO3溶液;⑤ ;⑥加适量的盐酸;⑦ 。
(2)溶液Ⅱ中发生反应的化学方程式是: 。
(3)Mg(OH)2沉淀中因混有Ca(OH)2,可选用___ ___ 溶液进行洗涤以除之。
(4)高温灼烧六水合氯化镁晶体(MgCl2・6H2O)所得固体是氧化镁,试写出该反应的化学方程式________ __ 。
(5)若在母液中通入氯气可提取海水中的溴,反应的离子方程式为:_____?_______。
参考答案:(1)过滤?蒸发结晶(只写“蒸发”给分,只写“结晶”不给分)
(2)NaCl + NH3 + CO2 + H2O=NaHCO3 + NH4Cl(2分,不追究沉淀符号)
(3)MgCl2或写“氯化镁”
(4)MgCl2・6H2O MgO+ 2HCl↑+5H2O↑?(5)Cl2 + 2Br―=2Cl―+ Br2
MgO+ 2HCl↑+5H2O↑?(5)Cl2 + 2Br―=2Cl―+ Br2
本题解析:(1)考查粗盐的提纯加入碳酸钠溶液之后,溶液中含有硫酸钡、氢氧化镁和碳酸钡以及碳酸钙沉淀,需要通过过滤除去。酸化后通过蒸发结晶即得到氯化钠。
(2)根据生成物碳酸氢钠和氯化铵可知,反应的方程式为NaCl + NH3 + CO2 + H2O=NaHCO3 + NH4Cl,
(3)由于氢氧化镁的溶解度小于氢氧化钙的,所以要除去氢氧化镁中的氢氧化钙,可以加入氯化镁生成氢氧化镁和氯化钙而除去。
(4)氯化镁在溶液中存在水解平衡,水解是吸热的,所以直接加热得不到氯化镁,而是得到氧化镁,方程式为MgCl2・6H2O MgO+ 2HCl↑+5H2O↑。
MgO+ 2HCl↑+5H2O↑。
(5)氯元素的非金属性强于溴元素的,所以氯气能把溴离子氧化生成溴单质,方程式为Cl2 + 2Br―=2Cl―+ Br2。
本题难度:一般
3、选择题 “耐高温长寿命抗氧化陶瓷复合材料应用技术”获2004年度国家技术发明一等奖。该复合材料的强度比钢还大,在航空航天器中用来替代金属材料,可节约20~30%的燃料。下列关于该材料的叙述中不正确的是
[? ]
A.该材料属于传统无机非金属材料
B.该材料的化学性质非常稳定
C.与金属一样有较好的传热性能
D.可以替代金属做耐高温结构材料
参考答案:AC
本题解析:
本题难度:简单
4、选择题 化学与工农业生产、人类生活都有密切相关,下列说法中正确的是
A.CO2和CH4都是造成温室效应的气体
B.石油裂解、煤的气化、海水制镁等过程中都包含化学变化
C.铝合金的大量使用归功于人们能使用焦炭等还原剂从氧化铝中获得铝
D.海水中含有钾、钠元素,只需经过物理变化就可以得到钾和钠单质
参考答案:AB
本题解析:C选项,冶炼金属铝应是用电解法冶炼。D选项还需经过一系列的化学反应才能得到钾或钠的单质。
本题难度:一般
5、简答题 氮化硅是一种高温陶瓷材料,它熔点高、硬度大、化学性质稳定,工业上曾普遍采用高纯硅与纯氮在1?300℃下反应制得.
(1)根据性质,推测氮化硅的用途是______(填序号).
①制汽轮机叶片?②制有色玻璃?③制永久性模具?④制柴油机
(2)氮化硅陶瓷抗腐蚀能力强,除氢氟酸外,它不与其他无机酸反应,试推测该陶瓷被氢氟酸腐蚀的化学反应方程式:______.
(3)四氯化硅和氮气在氢气的气氛保护下,加强热发生反应,可得较高纯度的氮化硅,反应的化学方程式为______.
参考答案:(1)氮化硅是一种高温陶瓷材料,它熔点高、硬度大、化学性质稳定,可用作制汽轮机叶片、制永久性模具、制柴油机,而有色玻璃只是在制作玻璃的过程中熔入了有颜色的化合物如Co2O3、Cu2O等,所以①③④正确,
故答案为:①③④;
(2)氮化硅与氢氟酸反应生成四氟化硅和一种铵盐,该铵盐为氟化铵,反应方程式为:Si3N4+16HF=4NH4F+3SiF4,
故答案为:Si3N4+16HF=4NH4F+3SiF4;
(3)四氯化硅和氮气在氢气的气氛保护下,加强热发生反应,可得较高纯度的氮化硅以及氯化氢,方程式为:3SiCl4+2N2+6H2?△?.?Si3N4+12HCl;
故答案为:3SiCl4+2N2+6H2?△?.?Si3N4+12HCl.
本题解析:
本题难度:一般