1��ѡ���� ����������ȷ���ǣ�������
A��Ũ�Ⱦ�Ϊ0.1mol?L-1��CH3COOH��CH3COONa��Һ�����������õ���Һ�У�c��CH3COOH��+c��CH3COO-��=0.2mol?L-1
B��0.1mol?L-1NaHCO3��Һ�У�c��Na+��=c��HCO3-��+c��H2CO3��+2��CO32-��
C��0.2mol?L-1HCl��Һ������0.1mol?L-1NaOH��Һ��Ϻ���Һ��pH=1
D��0.1mol?L-1��ˮ�е���0.1mol?L-1��������Һ������ʱ�������Һ�У�c��NH4+��=c��Cl-��
�ο��𰸣�A�����ʵ���Ũ�ȸ�Ϊ0.1mol?L-1��CH3COOH��CH3COONa��Һ�������Ϻ���ҺΪԭ���������2�������У�c��CH3COOH��+c��CH3COO-��=0.1mol/L����A����
B�����������غ��֪����Һ��Ӧ����c��Na+��=c��HCO3-��+c��H2CO3��+��CO32-������B����
C��c��H+��=0.2mol/LV-0.1mol/LV2V=0.05mol/L����pH=1.7����C����
D����Ӧ�����Һ����غ㣬����c��NH4+��+c��H+��=c��Cl-��+c��OH-������Һ�����ԣ�����c��H+��=c��OH-����������c��NH4+��=c��Cl-������D��ȷ��
��ѡD��
���������
�����Ѷȣ�һ��
2��ѡ���� �����ε�ˮ��Һ����pHֵС��7���ǣ�������
A��NH4Cl��Һ
B��NaCl��Һ
C��Na2SO4��Һ
D��NaHCO3��Һ
�ο��𰸣�A
���������
�����Ѷȣ�һ��
3��ѡ���� ��CH3COONa��Һ�и����ӵ�Ũ�ȵĹ�ϵ����ȷ���ǣ�������
A��c��Na+��+c��H+��=c��CH3COO-��+c��OH-��
B��c��Na+��=c��CH3COO-��+c��CH3COOH��
C��c��CH3COO-����c��Na+����c��OH-����c��H+��
D��c��Na+����c��CH3COO-����c��OH-����c��H+��
�ο��𰸣�A������Һ�ĵ����غ��֪c��Na+��+c��H+��=c��CH3COO-��+c��OH-������A��ȷ��
B���������غ��֪c��Na+��=c��CH3COO-��+c��CH3COOH������B��ȷ��
C��CH3COONaΪǿ�������Σ���CH3COO-����ˮ������CH3COOH������c��Na+����c��CH3COO-������C����
D��CH3COONaΪǿ�������Σ�ˮ��ʼ��ԣ���CH3COO-����ˮ������CH3COOH����c��Na+����c��CH3COO-����c��OH-����c��H+������D��ȷ��
��ѡ��C��
���������
�����Ѷȣ���
4������� �ۺ����ú�ˮ�����Ʊ�ʳ�Ρ��������þ��������ʣ���������ͼ��ʾ��
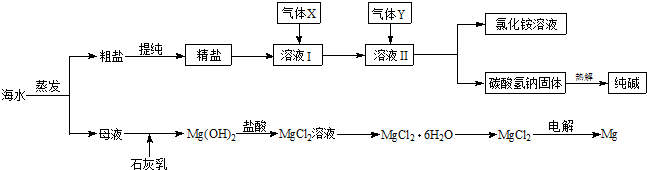
����������
��1��ʵ�����ᴿ���ε�ʵ���������Ϊ��ȡ����______��______������Ũ����______��______����ɣ�
��2������X��______���ѧʽ������ҺII�з�����Ӧ�Ļ�ѧ����ʽ�ǣ�______��
��3��Ϊ�����Ʒ̼�������Ƿ����Ȼ��ƣ���ȡ������������ˮ���ٵμ�______��
��4������ĸҺ��ͨ����������ȡ��ˮ�е��壬��Ӧ�����ӷ���ʽΪ______��
��5����MgCl2?6H2O��ȡ��ˮMgCl2�IJ���װ�ã�����̨���ƾ������ԣ����£�
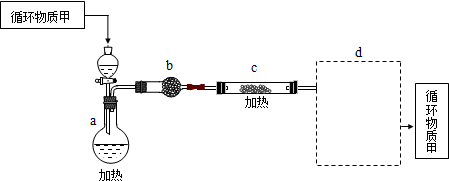
����ͼ�У�װ��a��______��______��˫�����͵������
��ѭ�����ʼ�������______��
����ȡ��ˮ�Ȼ�þ�������Ȼ�����ڵ������½��У���Ҫԭ����______��
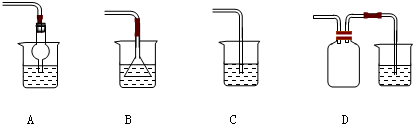
��װ��b���������ʿ�����______�������ţ�
e���轺?f����ʯ��?g��?��ˮ�Ȼ���?h��Ũ����
�ݷ����е�dװ�ÿ�ѡ��______��
�ο��𰸣���1�������ᴿ����Ҫ���裺����ȡ�������ܽ⣬����������ʢ��ˮ���ձ���ӱ��ò��������裨�������������ǽ��裬�����ܽ⣩��ֱ�ӵ����β����ܽ�ʱΪֹ���۲�����ʳ��ˮ�Ƿ���ǣ��۹��ˣ�����ʳ��ˮ����ϸ�۲���ֽ��ʣ���P��Һ��ɫ������Һ���ǣ�Ӧ�ٹ���һ�Σ��������ᾧ����������Һ�����������þƾ��Ƽ��ȣ����������г��ֽ϶����ʱ��ֹͣ���ȣ������������ɣ����ٹ��ˣ����Ƿ����ϲ���������Ϊֹ���ʴ�Ϊ���ܽ⣻���ˣ��ᾧ�����ˣ�����ˣ�ϴ�ӣ���
��2����ʳ��ˮ��ͨ�백����ͨ�������̼��������̼�����ƹ��壬�ʴ�Ϊ��NH3��NaCl+NH3+CO2+H2O�TNaHCO3��+NH4Cl��
��3�������ӵļ��鷽����ȡ������������ˮ���ٵμ������ữ�������������Ƿ��а�ɫ�������ɣ��ʴ�Ϊ��HNO3��AgNO3��
��4���������������ԣ���������ǿ���嵥�ʣ����������������ӣ���Ӧʵ��Ϊ��Cl2+2Br-�TBr2+2Cl-��
��5���ٸ���װ���õ��������У�Բ����ƿ����Һ©����˫�����͵��ܣ��ʴ�Ϊ��Բ����ƿ����Һ©����
���Ȼ�þ��ˮ�⣬Ӧ���Ȼ��������л���侧�壬�Ȼ������ѭ��ʹ�ã��ʴ�Ϊ�����
���Ȼ�þ��ˮ�⣬Ӧ���Ȼ��������л���侧�壬�ʴ�Ϊ����ֹþ����ˮ�⣻
����������ĸ�����������Ը���������Ը��������ѡ���У��轺�����Ը��������ʯ���Ǽ��Ը�������ܺ��������ʷ�Ӧ����ˮ�Ȼ��������Ը������Ũ���������Ը���������Ǿ���ǿ�����ԣ������ã�
���Ȼ��⼫������ˮ��ǿ�ҩҪ��ֹ��������ѡAD��
���������
�����Ѷȣ�һ��
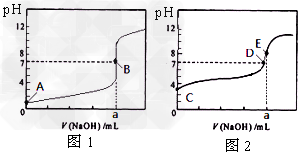
5��ѡ���� �����£���0.1000?mol/L?NaOH��Һ�ֱ�ζ�20.?00?mL?0.1000?mol/L?�����20.?00?mL?0.1000?mol/L?������Һ���õ�2���ζ����ߣ�����ͼ��ʾ������˵����ȷ���ǣ�A����ʾCl����
CH3COO����
[? ]
A���ζ������������ͼ2?
B���ﵽB��D״̬ʱ������Һ������Ũ�Ⱦ�Ϊ?c(Na��)?=?c(A��)
C���ﵽB��E״̬ʱ����Ӧ���ĵ�n(CH3COOH)��n(HCl)?
D����0?mL��V(NaOH)��20.?00?mLʱ����Ӧ�����Һ�и�����Ũ���ɴ�С��˳���Ϊ
c(A��)?��c(Na+)��c(H+)��c(OH��)
�ο��𰸣�B
���������
�����Ѷȣ�һ��