1��ѡ���� ��373Kʱ���ܱ������г���һ�����ʵ�����NO2��SO2���������·�Ӧ��
NO2+SO2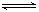 ?NO+SO3������Ӧ��ƽ��ʱ������������ȷ��ʱ:
?NO+SO3������Ӧ��ƽ��ʱ������������ȷ��ʱ:
A? NO��SO3�����ʵ���һ�����
B? NO2��SO2�����ʵ���һ�����
C?ƽ����ϵ�������ʵ���һ�����ڷ�Ӧ��ʼʱ�����ʵ���
D? SO2��NO2��NO��SO3�����ʵ���һ�����
�ο��𰸣�C
�����������һ�������£������淴Ӧ������Ӧ���ʺ��淴Ӧ�������ʱ���������ʵ�Ũ�Ⱥͺ���������ʱ��仯���仯��������״̬����ƽ��״̬�����A��B��D��һ����ȷ����Ϊ��Ӧǰ������������䣬����ƽ����ϵ�������ʵ���һ�����ڷ�Ӧ��ʼʱ�����ʵ�������ѡ��C����ȷ�ġ���ѡC��
�����Ѷȣ�һ��
2��ѡ���� ij�¶��µĺ����ܱ������з������·�Ӧ��2X(g)+Y(g)? 2Z(g)��ʼʱֻ����2.0molX��1.0molY�Ļ�����壬�ﵽƽ��ʱ����������ѹǿ�ȿ�ʼʱ������20%������ʼֻ����2.0molZ�����壬�ﵽƽ��ʱ��Z�ķֽ���Ϊ(? )
2Z(g)��ʼʱֻ����2.0molX��1.0molY�Ļ�����壬�ﵽƽ��ʱ����������ѹǿ�ȿ�ʼʱ������20%������ʼֻ����2.0molZ�����壬�ﵽƽ��ʱ��Z�ķֽ���Ϊ(? )
A��20%
B��40%
C��60%
D��80%
�ο��𰸣�B
����������������⣺���������Ӧ�ﵽƽ��ʱ����ɳɷֵ����ʵ�����
2X(g) + Y(g) 2Z(g) ?��X�ı仯��Ϊa
2Z(g) ?��X�ı仯��Ϊa
��ʼ����2.0 mol? 1.0 mol
�仯��: a?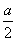 ? a
? a
ƽ��ʱ��2-a?1-a/2? a?2-a+1-a/2+a=3��(1-20%)
a="1.2" mol
��ͬ�º�ͬһ�����н�������Ӧ��ƽ��ʱ������ɳɷֵ����ʵ�����������Ӧ��ͬ��
2Z? ?2X(g)+Y(g)
?2X(g)+Y(g)
��ʼʱ? 2.0 mol ?0? 0
ƽ��ʱ? 1.2 mol ? 0.4 mol? 0.8 mol
Z�ķֽ���Ϊ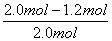 ��100%=40%����ΪB�
��100%=40%����ΪB�
�����Ѷȣ�һ��
3��ѡ���� ���º��������£�����������ȷ����
A����ͬ�ļס����������зֱ����1 g SO2��1 g O2��2 g SO2��2 g O2��������Ӧ2SO2(g)��O2(g)  SO3(g)�ﵽƽ�⣬SO2��ת����ǰ�ߴ�
SO3(g)�ﵽƽ�⣬SO2��ת����ǰ�ߴ�
B����Ӧ2HI(g)  H2(g)��I2(g)�ﵽƽ�⣬����HI�����ʵ�����ƽ�ⲻ�ƶ�
H2(g)��I2(g)�ﵽƽ�⣬����HI�����ʵ�����ƽ�ⲻ�ƶ�
C����Ӧ2NO2(g )  N2O4(g)�ﵽƽ��ʱ������������ͨ��һ������NO2(g)�����´ﵽƽ��ʱ�����һ��ƽ��ʱ��ȣ�NO2�������������
N2O4(g)�ﵽƽ��ʱ������������ͨ��һ������NO2(g)�����´ﵽƽ��ʱ�����һ��ƽ��ʱ��ȣ�NO2�������������
D����Ӧ2HI(g)  H2(g)��I2(g)�ﵽƽ�⣬����HI�����ʵ�����HI�ķֽ��ʺ��������������
H2(g)��I2(g)�ﵽƽ�⣬����HI�����ʵ�����HI�ķֽ��ʺ��������������
�ο��𰸣�D
���������A�к���c(SO2)��c(O2)����ѹǿ�����Ժ���SO2��ת���ʴ�
B������HI�����ʵ�������������c(HI)��ƽ�����ƣ���ѹǿ������Ӱ��ƽ���ƶ������Դﵽ����ƽ��̬��ԭƽ��̬��ͬ����D��ȷ��
C������������ͨ��һ������NO2(g)����������c(NO2)��ƽ�����ƣ����ԣ����´ﵽƽ��ʱ�����һ��ƽ��ʱ��ȣ�NO2�����������С��
�����Ѷȣ�һ��
4������� ��һ���ݻ�Ϊ4L���ܱ������г���7molSO2��4molO2����һ���¶Ⱥ�ѹǿ�£��������·�Ӧ��2SO2��g��+O2��g��?
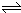
2SO3��g������4s��ﵽƽ��״̬�����SO2�����ʵ�����3mol�����㣺
��1����O2��ʾ�ĸ÷�Ӧ������______
��2��ƽ��ʱSO3�����ʵ���Ũ��______��
�ο��𰸣���1����SO2��ʾ�ĸ÷�Ӧ������v��SO2��=(7-3)mol4L4s=0.25mol?L-1?s-1������֮�ȵ��ڻ�ѧ������֮�ȣ������У�
v��O2��=12v��SO2��=12��0.25mol?L-1?s-1=0.125mol?L-1?s-1��
�ʴ�Ϊ��0.125mol?L-1?s-1
��2���μӷ�Ӧ��SO2�����ʵ���Ϊ7mol-3mol=4mol�����ݷ���ʽ2SO2��g��+O2��g��?2SO3��g����֪�����ɵ�SO3�����ʵ������ڲμӷ�Ӧ��SO2�����ʵ�����ƽ��ʱSO3�����ʵ���Ũ��Ϊc��SO3��=4mol4L=1mol/L��
�ʴ�Ϊ��1mol/L
���������
�����Ѷȣ�һ��
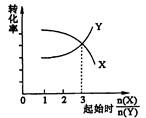
5��ѡ���� ��һ�������£���X��Y�������ʰ���ͬ�ı��������ܱ������з�Ӧ��ƽ�����X��Y��ת��������ʼʱ�����ʵ����ʵ���֮��nx/ny�Ĺ�ϵ��ͼ��ʾ����X��Y�ķ�Ӧ����ʽ�ɱ�ʾΪ
A? 2X��Y 3Z? B? 3X��2Y
3Z? B? 3X��2Y 2Z
2Z
C? X��3Y Z? D? 3X��Y
Z? D? 3X��Y Z
Z
�ο��𰸣�D
�����������Ӧ��ֻ�а��շ���ʽ�еĻ�ѧ������������з�Ӧ����ת���ʲ�����ȵģ����Ը���ͼ����жϣ�X��Y�����ʵ���֮����3�U1������ѡ��D��ȷ��
�����Ѷȣ�һ��