1�������� Ϊ�������÷Ϸ�����(����V2O5��VOSO4�������Բ�������������Ա����������һ�����ӽ��������շ����¹��գ���Ҫ�������£�
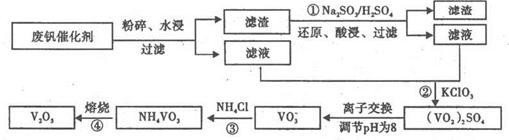
���ֺ���������ˮ�е��ܽ������£�

�ش��������⣺
(1)��ҵ����V2O5ұ���������������ȷ����÷�Ӧ�Ļ�ѧ����ʽΪ_______
(2)Ϊ����߷��Ľ����ʣ������ʹ�����е�V2O5ת��ɿ�����ˮ��VOSO4����ˮ��Һ�ϲ�������KClO3����,ʹ+4�۵�V������������ˮ��(VO2)2SO4����Ӧ�ٵ����ӷ���ʽΪ_______;��Ӧ�ڵ����ӷ���ʽΪClO3����6VO2����3H2O��6VO2����6H����Cl����
(3)�ù����з�Ӧ�۵ij������ǻ��շ��Ĺؼ�֮һ,�ò���Ӧ�����ӷ���ʽΪ_______��
(4) ʵ�����õ�ԭ����V2O5ռ6%(ԭ���е����з��ѻ����V2O5)��ȡ100g�÷Ϸ���������ҵ�����IJ������ʵ�飬������100 mL 0.1 mol��L-1��KC1O3��Һʱ,��Һ�еķ�ǡ�ñ���ȫ�����������Ժ������û����ʧ�����ʵ���з��Ļ�������_______ (��֪V2O5����Է�������Ϊ182)��
(5)?ȫ��Һ���ܵ�������ò�ͬ��̬�����Ӷ�֮���������ԭ��Ӧ��ʵ�ֻ�ѧ�ܺ͵����ת����װ��,��ԭ��������ͼ��ʾ����֪��ص��ܷ�ӦʽΪVO2����V2����2H�� VO2����V3����H2O
VO2����V3����H2O
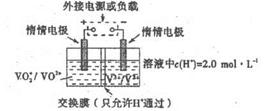
�ٷŵ�ʱ��������ӦʽΪ______________��
�ڷŵ�����������ӵ�������______________�����ʱ��ת�Ƶĵ���Ϊ2mol���������Һ��n��H+)�ı仯��Ϊ______________��
�ο��𰸣���16�֣���1��3V2O5+10Al 6V+5Al2O3?(2��) ��2����V2O5+SO32-+4H+��2VO2++SO42-+2H2O(3��)
6V+5Al2O3?(2��) ��2����V2O5+SO32-+4H+��2VO2++SO42-+2H2O(3��)
��3��NH4����VO3����NH4VO3��(2��) ��4��91%(3��) ��5����VO2����2H����e����VO2����H2O(2��)
�ڲ���������Ӧ��ͨ������Ĥ�����ƶ�ʹ����ͨ����Һ(2��)�� 2mol(2��)
�����������1�����ǻ��õĽ������ܺ������������������ȷ�Ӧ���ɵ��ʷ�������������Ӧ�Ļ�ѧ����ʽΪ3V2O5+10Al 6V+5Al2O3��
6V+5Al2O3��
��2�������ܽ��Ա�֪��������V2O5�����������£�V2O5���������Ʒ���������ԭ��Ӧ����VOSO4����Ӧ�����ӷ�Ӧ����ʽΪV2O5+SO32-+4H+��2VO2++SO42-+2H2O��
��3����Ӧ���Ǹ��ֽⷴӦ����Ӧ�����ӷ���ʽ��NH4����VO3����NH4VO3����
��4������V2O5��SO32-��4H+��2VO2+��SO42-��2H2O��ClO3����6VO2����3H2O��6VO2����6H����Cl����֪��
3V2O5��6VO2+��ClO3��
3mol? 1mol
n? 0.01mol
����n��0.03mol
��˸�ʵ���з��Ļ������� ��100%��91.0%
��100%��91.0%
��5����ԭ����и���ʧȥ���ӣ�����������Ӧ�������õ����ӣ�������ԭ��Ӧ�������ܵķ���ʽ��֪VO2���õ����ӱ���ԭΪVO2������������缫��Ӧʽ��VO2����2H����e����VO2����H2O��
�ڸ��ݢٿ�֪���ŵ�ʱ�������������ӣ����Էŵ�����������ӵ������Dz���������Ӧ��ͨ������Ĥ�����ƶ�ʹ����ͨ����Һ������װ��ͼ��֪�����ʱ��۵缫�͵�Դ���������������������缫��Ӧʽ��VO2����H2O��e����VO2����2H�������Գ��ʱ��ת�Ƶĵ���Ϊ2mol���������Һ��n��H+)�ı仯��Ϊ2mol��
�����Ѷȣ�����
2��ѡ���� �˴Ź�����Ӱ��ǿ�����ڼ�������ϣ���������Ϊҩ���������ڼ��������ơ��п�Ժ��ѧ�о�����������������ôŹ�����Ӱ���о�����ȡ����Ҫ��չ��Ϊ�������������������ҽѧ�����Ӧ���ṩ�˸��㷺��ǰ�����Ʊ����������������Ĺ������£�
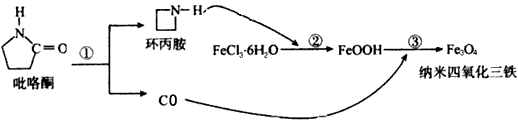
�������������������
[? ]
A. �����������������д��ԣ���Ϊҩ���������ڼ���������
B. ����������������ɢ���ʵ��ܼ��У�������Һ��ɢ��ֱ���൱
C. �ڷ�Ӧ���л����������ÿ����Ǵٽ��Ȼ���ˮ��
D. ��Ӧ�۵Ļ�ѧ����ʽ��6FeOOH+CO=2Fe3O4+3H2O+CO2
�ο��𰸣�B
���������
�����Ѷȣ�һ��
3��ѡ���� ��6.4��CuͶ�뵽һ������������Һ�У�Cuȫ���ܽ⣬��Һ��ʣ��H+amol����Һ�к�NO3-�����ʵ���Ϊmol��
A.0.2
B.a
C.0.2+a
D.����ȷ��
�ο��𰸣�C
�������������������Cu+4HNO3�TCu��NO3��2+2NO2��+2H2O��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O������Cu��NO3��2��Cu��NO3-�Ĺ�ϵ��ʣ��������������
�����CuͶ�뵽һ������������Һ�У�����Cu+4HNO3�TCu��NO3��2+2NO2��+2H2O��3Cu+8HNO3�T3Cu��NO3��2+2NO��+4H2O��
��֪Cu��2NO3-��
n��Cu��=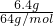 =0.1mol��
=0.1mol��
����Һ��n��NO3-��=0.1mol��2=0.2mol��
����Һ��ʣ��H+amol����ʣ��������n��NO3-��=amol��
���Է�Ӧ����Һ��n��NO3-��=amol+0.2mol=��0.2+a��mol��
��ѡC��
���������⿼������Ļ�ѧ���ʣ���ȷ��Ӧ��Cu����������ӵĹ�ϵ�ǽ����Ĺؼ����ѶȲ���
�����Ѷȣ���
4��ѡ���� ����ʹ�ò��ϵ�����ͱ仯����־�����������Ľ��������в����뻯ѧ�Ʊ��ص���
[? ]
A��ʯ��
B����ͭ��
C������
D���߷��Ӳ���
�ο��𰸣�A
���������
�����Ѷȣ���
5������� �����ѧ���������ɫ���ɡ����룺�ѿ�������̼�����Һ��Ȼ���ٰ�CO2����Һ����ȡ����������ѧ��Ӧ��ʹ֮��Ϊ������ȼ�ϼ״�������ɫ���ɡ����뼼����������
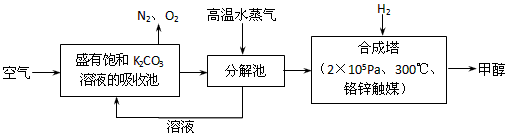
��1������������̼�����Һ�����������_________________��
��2���ֽ���з�Ӧ�Ļ�ѧ����ʽΪ_________________��
��3���ںϳ����У�����4.4kg CO2������H2ǡ����ȫ��Ӧ��������̬��ˮ�ͼ״����ɷų�4947 kJ����������д���ϳ����з�����Ӧ���Ȼ�ѧ����ʽ_________________��
��4����ƽ���ƶ�ԭ������������������ԭ������ת����ʵ�������в���300��ĸ��£�ԭ��֮һ�ǿ��ǵ������Ĵ����ԣ�ԭ��֮����_________________��
��5����ͼ�Ǽ״�ȼ�ϵ�صĽṹʾ��ͼ���״��ڴ����������ṩ����(H+)�͵��ӣ����Ӿ����·�����Ӿ��ڵ�·������һ����������Ӧ������ܷ�ӦΪ��2CH3OH+3O2��2CO2+4H2O ��
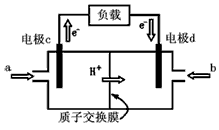
a��ͨ����������________��д���ƣ����缫d��������______�����缫c�������ĵ缫��Ӧ����Ϊ��
_________________��
�ο��𰸣���1�����������е�CO2��Ϊ�ϳɼ״��ṩCO2����������𰸾����֣�
��2��2KHCO3 K2CO3��CO2����H2O
K2CO3��CO2����H2O
��3��CO2(g)+3H2(g)==CH3OH(g)+H2O(g)����H����49.47kJ/mol
��4����֤�нϿ�ķ�Ӧ���ʣ���߲��ʣ��ܴ����������ص���ȷ�𰸼��ɣ�
��5���״�������CH3OH+H2O��6e-=CO2+6H+
���������
�����Ѷȣ�һ��