1������� ��ijһԪ��HA��Һ��NaOH��Һ�������ϣ�
��1����c?��HA��=c?��NaOH��=0��lmol/L����û�Ϻ���Һ��pH��7��
�ٲ���֤��HA��������ʵķ�����______
A�����0.1mol/L?HA��pH��l
B�����NaA��Һ��pH��7
C��pH=l��HA��Һ�����ᣬϡ��100���������pH�仯��
D��������п�ֱ�����ͬpH����ͬ����������HA��Һ��Ӧ������������һ����
�ڻ����Һ�У���ϵʽһ����ȷ����______
A��c��A-����c��Na+����c��OH-����c��H+��?B��c��A-��+c��OH-��=c��Na+��+c��H+��
C��c��HA��+c��A-��=0.1mol/L?D��c��?HA��+c��?H+��=c��OH-��
����HA+B2-��������=A-+HB-��H2B��������+2C-=B2-+2HC��HA+C-=A-+HC������ͬpH��?��NaA��Һ?��Na2B��Һ?��NaHB��Һ?��NaC��Һ�������ʵ���Ũ���ɴ�С��˳��Ϊ______������ţ���
��2����c��?HA��=c��NaOH��=0.1mol/L����û�Ϻ���Һ��pH=7��
���ֽ�һ��Ũ�ȵ�HA��Һ��0.1mol/L?NaOH��Һ�������Ϻ�������Һ��pH����Ũ�ȵ�HA��Һϡ��10����������Һ��pH��ȣ���HA��Һ�����ʵ���Ũ��Ϊ______��
���ñ���NaOH��Һ�ζ�δ֪Ũ�ȵ�HAʱ�����в�������������HAŨ��ƫ�����______��
A��������ˮϴ����ƿ���ô���HA��Һ������ϴ
B���ζ�ǰ���ֵζ��ܵļ��첿�������ݣ��ζ�����ʧ
C��װNaOH�ļ�ʽ�ζ���δ�ñ���NaOH��Һ��ϴ
D���ζ�ǰ���ӣ��ζ����Ӷ���
��3����c��HA��=0.04mol/L��c��NaOH���T0.02mol/L��
����HAΪHCN������Һ�Լ��ԣ�����Һ��c��Na+��______c?��CN-�����С�ڡ��������ڡ����ڡ������ó��ý��۵�������______��
����HAΪCH3COOH������Һ�����ԣ���Һ���������Ӱ�Ũ���ɴ�С���е�˳����______��
����HAΪǿ�ᣬ99��ʱ��Kw=10-12������������Һ�������Ϻ���Һ����ˮ�������H+Ũ��Ϊ______mol/L�������Ϻ���Һ���Ϊ����Һ���֮�ͣ���
�ο��𰸣���1����A�����0.1mol/L?HA��pH��l��˵��HAû����ȫ���룬��A��ȷ��
B�����NaA��Һ��pH��7��˵����Һ�д���A-��ˮ�⣬HAΪ������ʣ���B��ȷ��
C��pH=l��HA��Һ�����ᣬϡ��100���������pH�仯��˵��HAû����ȫ���룬��ˮϡ�ʹٽ����룬HAΪ������ʣ���C��ȷ��
D��������п�ֱ�����ͬpH����ͬ����������HA��Һ��Ӧ������������һ���࣬˵��HAΪǿ����ʣ�����Ŀ��������D����
�ʴ�Ϊ��D��
��A��A-ˮ�⣬��Һ�д���c��Na+����c��A-����ӦΪc��Na+����c��A-����c��OH-����c��H+������A����?
B��������Һ�ĵ�����ԭ����Һ�д��ڣ�c��A-��+c��OH-��=c��Na+��+c��H+������B��ȷ��
C�����ϡ�ͺ�c��HA��+c��A-��=0.05mol/L����C����
D�����������غ㣬����c��HA��+c��A-��=c��Na+����������Һ�ĵ�����ԭ����c��A-��+c��OH-��=c��Na+��+c��H+����������ʽ�ɵã�c��?HA��+c��?H+��=c��OH-������D��ȷ��
�ʴ�Ϊ��BD��?
�۴ӽ��H+�������жϣ�HA+B2-��������=A-+HB-�����ԣ�H2B��HA��HB-��H2B��������+2C-=B2-+2HC�����ԣ�H2B��HB-��HC��
HA+C-=A-+HC�����ԣ�HA��HC���������ԣ�H2B��HA��HB-��HC���ζ�Ӧ����Խ������Ӧ��������ӵ�ˮ��̶�Խ��PH��ͬʱ����Ӧ�����ʵ���Ũ���ɴ�С��˳��Ϊ�ۣ��٣��ڣ��ܣ�
�ʴ�Ϊ���ۣ��٣��ڣ��ܣ�
��2����c��?HA��=c��NaOH��=0.1mol/L����û�Ϻ���Һ��pH=7��˵��HAΪǿ�ᣬ
����HAŨ��Ϊc�����ΪV�����У�cV-0.1V2V=cV10V����c=0.125��
�ʴ�Ϊ��0.125?mol/L��
��A��������ˮϴ����ƿ���ô���HA��Һ������ϴ����V���ƫ������HAŨ��ƫ��A��ȷ��
B���ζ�ǰ���ֵζ��ܵļ��첿�������ݣ��ζ�����ʧ����V���ƫ������HAŨ��ƫ��B��ȷ��
C��װNaOH�ļ�ʽ�ζ���δ�ñ���NaOH��Һ��ϴ����V���ƫ������HAŨ��ƫ��C��ȷ��
D���ζ�ǰ���ӣ��ζ����Ӷ������ᵼ����V���ƫС������HAŨ��ƫС����D����
�ʴ�Ϊ��ABC��
��3������Һ�ʼ��ԣ���c��H+����c��OH-����������Һ�ʵ����ԣ�����c��Na+��+c��H+��=c��CN-��+c��OH-����
����c��Na+����c��CN-����
�ʴ�Ϊ�����ڣ�
��Ϊc��Na+��+c��H+��=c��CN-��+c��OH-������Һ�ʼ��ԣ���c��H+����c��OH-��������c��Na+����c��CN-����
?����Һ�����ԣ�����c��H+����c��OH-����������Һ�ʵ����ԣ�����c��Na+��+c��H+��=c��CH3COO-��+c��OH-����
����c��CH3COO-����c��Na+������Ȼ��Ӧ��ʣ��Ĵ���������ӵ����ʵ�����ȣ�������Ϊ������ʣ����ֵ��룬����
c��Na+����c��H+��������c��CH3COO-����c��Na+����c��H+����c��OH-����
�ʴ�Ϊ��c��CH3COO-����c��Na+����c��H+����c��OH-����
����HAΪǿ�ᣬ��Ӧ������������У�c��H+��=0.04mol/L��V-0.02mol/L��V2V=0.01mol/L��
99��ʱ��Kw=10-12����c��H+����c��OH-��=10-12��
c��OH-��=10-10����ˮ�������c��H+����ȣ�
�ʴ�Ϊ��10-10��
���������
�����Ѷȣ�һ��
2��ѡ���� ��0.1mol/L��CH3COOH��ˮϡ�ͣ��й�ϡ�ͺ������Һ��˵���У�������ǣ�������
A������̶�����
B����Һ��������������
C����Һ��������ǿ
D����Һ�д�����Ӽ���
�ο��𰸣�C
���������
�����Ѷȣ���
3��ѡ���� �������Ϊ1 L��pH������2������ʹ�����Һ�У�Ͷ��0.65 gп��������ͼ��ʾ�ȽϷ��Ͽ���ʵ����
[? ]
A. 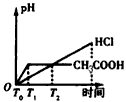
B. 
C. 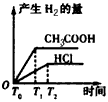
D. 
�ο��𰸣�C
���������
�����Ѷȣ�һ��
4��ѡ���� �����£��й�����������Һ��������ȷ����(������Һ��Ϻ������仯)(����)
���
| ��
| ��
| ��
| ��
|
pH
| 12
| 12
| 2
| 2
|
��Һ
| ��ˮ
| ����������Һ
| ����
| ����
|
?
A.�ڢ١����зֱ�����Ȼ�茶��壬����Һ��pH������
B���ֱ�����Ģٺ͢ڼ�ˮϡ��100����������Һ��pH����>��
C���Ѣ١�������Һ�������Ϻ�������Һ�У�c(Cl��)>c(NH4+)>c(OH��)>c(H��)
D������Һ�ں���Һ�۵������ϣ���Ϻ�������ҺpH��7
�ο��𰸣�B
���������A������Ȼ��ˮ������ԣ����ڢ١����зֱ�����Ȼ�茶��壬����Һ��pH����С������ȷ��B��ֱ�ϡ��100�������ڢ�����������Ϊǿ����ʣ������д��ڰ�ˮ�ĵ���ƽ�⣬����ȷ��C����١�������Һ�������Ϻ�ˮ��������Һ�ʼ��ԣ����ݵ���غ��жϣ��ʲ���ȷ��D�����Һ�ں͢۵������Ϻ����ڴ��������ᣬ��Ӧ�й����϶࣬��Ӧ����Һ�����ԣ��ʲ���ȷ��
�����Ѷȣ�һ��
5������� �����£���Ũ�Ⱦ�Ϊ0.1 mol/L��4����Һ�������������۴����������������ע��������Һ���ʱ ����ı仯��
(1)��������Һ�����������Ϻ���ҺpH=7������У�����ţ�_________��
(2)���ᱵ��������ˮ��ǿ����ʡ�������ܵ������ϣ�������Һ������Ũ���ɴ�С��˳����_____��
�ο��𰸣�(1)�ں͢�
(2)c(OH-)>c(Ba2+)>c(CH3COO-)>c(H+)
���������
�����Ѷȣ�һ��