| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《电解质和非电解质》高频考点强化练习(2020年最新版)(四)
参考答案:C 本题解析: A.纯净物是指只有一种物质,但不一定是由分子构成的,例如金属钠是由原子构成的,故不选A;B.混合物是指含有两种或两种以上的物质,例如氧气和臭氧是两种物质,但只含有一种元素,故不选B;C.同种分子的物质一定是一种物质吗,是纯净物,故选C;D.含有两种元素的化合物中有氧元素的为氧化物,如果含有三种元素的,就不是氧化物,故不选D。 本题难度:一般 2、选择题 按照物质的树状分类和交叉分类,HNO3应属于:①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤难挥发性酸 ⑥强氧化性酸 ⑦一元酸 ⑧化合物 ⑨混合物 |
参考答案:B
本题解析:HNO3为酸,含有O元素,为含氧酸,HNO3具有强氧化性,为强氧化性酸,1个HNO3能电离出1个H+,为一元酸,故B项正确。
考点:本题考查物质的分类。
本题难度:一般
3、选择题 按照物质的交叉分类法判断,H2SO4属于( )
①酸 ②氢化物 ③氧化物 ④含氧酸 ⑤二元酸 ⑥化合物 ⑦混合物
A.①②③④⑤⑥
B.①④⑤⑥
C.①②③④
D.①④⑤⑦
参考答案:B
本题解析:略
本题难度:简单
4、实验题 (10分)过氧化氢是重要的氧化剂、还原剂,它的水溶液又称为双氧水,常用作消毒、杀菌、漂白等。某化学兴趣小组取一定量的过氧化氢溶液,准确测定了过氧化氢的含量,并探究了过氧化氢的性质。
Ⅰ、测定过氧化氢的含量
请填写下列空白:
(1)移取10.00 mL密度为ρ g/mL的过氧化氢溶液至250mL ___________(填仪器名称)中,加水稀释至刻度,摇匀。移取稀释后的过氧化氢溶液25.00mL至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释,作被测试样。
(2)用高锰酸钾标准溶液滴定被测试样,其反应的离子方程式如下,请将相关物质的化学计量数及化学式填写在方框里。
(3)滴定时,将高锰酸钾标准溶液注入 (填“酸式”或“碱式”)滴定管中。滴定到达终点的现象是 。
(4)重复滴定三次,平均耗用c mol/L KMnO4标准溶液V mL,则原过氧化氢溶液中过氧化氢的质量分数为 。
参考答案:Ⅰ、(1) 容量瓶 (2) 2 5 6 2 8 5 O2↑
(3)酸式; 滴入一滴高锰酸钾溶液,溶液呈浅紫色,且30秒内不褪色 (4)17cV/200ρ
本题解析:Ⅰ、(1)容量瓶是一种定容仪器,可以准确量取250mL的液体,故答案为:容量瓶;
(2)双氧水遇到强氧化剂高锰酸钾时表现强的还原性,被氧化为氧气。反应中氧元素的化合价从-1价升高到0价,失去1个电子。Mn元素的化合价从+7价降低到+2价得到5个电子,所以根据电子得失守恒可知配平后的反应方程式为2MnO4-+5H2O2+6H+=2Mn2++8H2O+5O2 ;
(3)高锰酸钾溶液具有强氧化性,能腐蚀橡胶,所以要放在酸式滴定管中;高锰酸钾本身是一种紫红色的液体,高锰酸钾标准溶液注入滴定管中滴定双氧水时,当达到滴定终点时,溶液呈紫红色,且30秒内不褪,故答案为:酸式;滴入最后一滴高锰酸钾溶液,溶液呈紫红色,且30秒内不褪色;
(4)根据高锰酸钾和双氧水反应的方程式,设双氧水的物质的量为n,则
2MnO4-+6H++5H2O2=2Mn2++8H2O+5O2
2 5
cV×10-3mol n
解得n=2.5cV×10-3mol
所以25.00mL双氧水的质量=2.5cV×10-3mol×34g/mol=0.085cVg,250.00mL双氧水的质量=0.85cVg,则双氧水的质量分数为: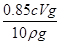 ×100%=
×100%=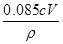 。
。
考点:考查双氧水含量测定的实验设计与探究
本题难度:一般
5、选择题 下列物质中属于强电解质的是
A.稀硫酸
B.BaSO4
C.Al(OH)3
D.NH3・H2O
参考答案:B
本题解析:再水溶液中能完全电离的电解质为强电解质。稀硫酸是混合物,不是电解质,A错误;硫酸钡虽然水溶液是难溶于水的,但溶于水的那部分是完全电离的,故是强电解质,B正确;C、D在水溶液中部分电离,属于弱电解质,答案选B.
考点:强电解质的定义
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点讲解《有机合成与.. | |