1��ѡ���� ����ʵ���ܻ�óɹ�����
A������ˮ���𱽡��Ҵ�����ϩ�����Ȼ�̼
B����Ũ��ˮ������˳�ȥ������������
C��������ˮ�����ۻ���Ƴ��屽
D�����÷�Һ©������������ͼױ�
�ο��𰸣�A
����������������Ȼ�̼����ˮ������ȡ���л���ֱ����ϲ���²㡣�Ҵ�����ˮ���ܣ���ϩ����ˮ�����ӳɷ�Ӧ��A���Լ���B�����ɵ����屽���ܹ��ܽ��ڱ��У����ܳ�ȥ��B����C����ȷ��Ӧ����Һ�壻������ͼױ����ܣ�����ֱ�ӷ�Һ��D����ȷ����ѡA��
�������������л��е����ʳ�ȥ����ô�������ᴿ���������һ��IJ�ͬ���ʱ˴˷ֿ����õ���Ӧ��ֵĸ�������з��롣�ڽ�����ʷ����ᴿ����ʱ,ѡ���Լ���ʵ���������Ӧ��ѭ����ԭ��: 1.���������µ����ʣ�ˮ���⣩���������ᴿ�������Ӧ�Ǵ����������Һ�����������������ʻ������У�2.�����ᴿ�������״̬���䣻3.ʵ����̺Ͳ������������У���ѡ������ᴿ����Ӧ��ѭ��������ѧ���ȼ��ӵ�ԭ��
�����Ѷȣ���
2��ѡ���� ʵ���ú������ʣ�FeO��Fe2O3���ķ�CuO�Ʊ��������徭�����й��̣�Fe3+��PH=5ʱ����ȫ�����������������ǣ�������

A����18mol/LŨ���������ܽ�����4mol/L��ϡ���ᣬ��������һ��ֻ��3��
B������Cu��OH��2���CuOҲ�ɵ�����ҺPH��Ӱ��ʵ����
C��ϴ�Ӿ��壺���˳������©���м�����ˮ��û���壬��Ȼ���£��ظ�2-3��
D����Ҫʵ��ⶨ��������ͭ�����нᾧˮ����ĿҪ�õ�����������ǯ
�ο��𰸣�A����18mol/LŨ���������ܽ�����4mol/L��ϡ���ᣬ�õ���Ͳ���ձ�����ͷ�ιܡ��������Լ�����ƿ����������A����
B��Cu��OH��2��CuO������Һ��H+��Ӧ��������ҺPH�����ã����������µ����ʣ���B��ȷ��
C��������������ԣ�����ʱ�����п��������ʣ������˳������©���м�����ˮ��û���壬��Ȼ���£��ظ�2-3�Σ���ϴ�Ӿ��壬��C��ȷ��
D���ⶨ�ᾧˮ�ĺ�����ͨ�����ȹ��壬��ȥ�ᾧˮ�����������ı仯�ɵĽᾧˮ�ĸ����������õ�����������ǯ����D��ȷ��
��ѡA��
���������
�����Ѷȣ���
3��ѡ���� �����й�ʵ�����������ͽ��ͻ���۶���ȷ���� (? )
ѡ��
| ʵ�����
| ����
| ���ͻ����
|
A
| ������Fe���м���ϡHNO3����ַ�Ӧ����KSCN��Һ
| ��Һ�ʺ�ɫ
| ϡHNO3��Fe����ΪFe3��
|
B
| AgI�����е���ϡKCl��Һ
| �а�ɫ��������
| AgCl��AgI������
|
C
| �����£���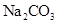 ��Һ�м����� ��Һ�м����� ��ĩ�����ˣ���ϴ���ij����м�ϡ���� ��ĩ�����ˣ���ϴ���ij����м�ϡ����
| �����ݲ���
| ����˵��������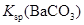
��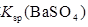 �Ĵ�С��ϵ �Ĵ�С��ϵ
|
D
| �ò�����պȡŨ��ˮ�㵽��ɫʯ����ֽ��
| ��ֽ����ɫ
| Ũ��ˮ�ʼ���
�ο��𰸣�CD
���������
��ȷ�𰸣�C��D
A��3Fe��8HNO3=3Fe(NO3)2��2NO��4H2O����Fe3��������KSCN��Һ�����ʺ�ɫ��
B��AgCl��I�D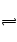 AgI��Cl�D�ǿ��淴Ӧ�� AgI��Cl�D�ǿ��淴Ӧ��
C��CO32�D��BaSO4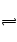 BaCO3��SO42�D,�ǿ��淴Ӧ�����Խ�����ȷ�� BaCO3��SO42�D,�ǿ��淴Ӧ�����Խ�����ȷ��
D������ͽ��۾���ȷ��
�����Ѷȣ���
4��ѡ���� ����ʵ�鷽����ȷ���ǣ�������
A���÷�Һ©�������������������
B����Ʒ����Һ����SO2��CO2��������
C����Ca��OH��2��Һ����Na2CO3��Һ��NaHCO3��Һ
D����ʢ��NaOH��Һ��ϴ��ƿ��ȥCO2�л��е�HCl����
�ο��𰸣�A�������������������ֲ㣬�������÷�Һ�����룬��A����
B�������������Ư���Կ�ʹƷ����ɫ����������̼���ܣ�����Ʒ����Һ����SO2��CO2�������壬��B��ȷ��
C��Na2CO3��Һ��NaHCO3��Һ��Ca��OH��2��Һ��Ӧ�����ɰ�ɫ���������ܼ���Ӧѡ�Ȼ��Ƽ�����ߣ���C����
D��������̼��HCl����NaOH��Һ��Ӧ�������ϳ��ӵ�ԭ����Ӧѡ����̼��������Һ�����ӣ���D����
��ѡB��
���������
�����Ѷȣ���
5��ʵ���� ij��ѧ��ȤС���ͬѧ������ͼ��ʾʵ��װ�ý���ʵ��(ͼ��a��b��c��ʾֹˮ��)��
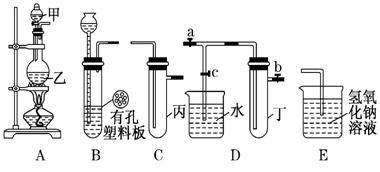
�밴Ҫ����գ�
(1)������������__________________��
(2)����Bװ�ÿ���ȡ��������_________��(д��һ�ּ���)��
(3) A��C��E������ ��װ�ÿ�������ȡCl2��������ص�����ʵ�飮 ��װ�ÿ�������ȡCl2��������ص�����ʵ�飮
���ڱ��м�������ˮ�������Ƶ���ˮ����������ˮ��Ϊ���ݣ����Т�����ʵ�飬ʵ����������������£�
ʵ�����
| ʵ�����
| ����
| ����
| ��
| ����ˮ����Ʒ����Һ
| ��Һ��ɫ
| ������ˮ��Ӧ��
������Ư����
| ��
| ��ˮ�м���
̼�����Ʒ�ĩ
| ����ɫ���ݲ���
| ������ˮ��Ӧ��
�����������
|
?
��������ʵ���Ľ����Ƿ������������������ֱ��˵������
ʵ���___________________________________________________
ʵ���_______________________ _____________________________. _____________________________.
(4)B��D��Eװ����������B��ʢװŨ�����ͭƬ(�����п����ϰ���)�����Ƶò�����NO2�й�ʵ�飮
������Dװ����֤NO2��ˮ�ķ�Ӧ�����������Ϊ���ȹر�ֹˮ��a��b���ٴ�ֹˮ��c��ʹ�ձ��е�ˮ�����Թܶ��IJ�����_______��
���Թܶ��м���NO2������ˮ��ַ�Ӧ�����Թ��ڻ���ͨ��һ������������ֱ���Թ���ȫ������ˮ����������Һ�����ʵ����ʵ���Ũ����_______mol/L(���尴��״������)��
�ο��𰸣�(1)��Һ©����2�֣�
(2)H2��CO2��2�֣�
(3)���١�ʵ�����ۺ�����ʵ�����۲�������?��ȡ�������к���HCl���壬HCl����ˮ������̼�����Ʒ�ĩ��Ӧ�������� ��4�֣�
(4)���١�˫�ֽ���(����)�Թܶ���ʹ�Թ��������ݳ���NO2��ˮ�Ӵ��������ձ��е�ˮ�������Թܶ���?��2�֣�
�� 0.045 mol/L (��1/22.4) ��2�֣�
�����������
�����Ѷȣ�һ��
|