|
高中化学知识点归纳《物质的量》试题特训(2020年最新版)(八)
2020-08-23 08:14:16
【 大 中 小】
|
1、选择题 配置一定物质的量浓度的硫酸溶液是,下列操作会造成所配硫酸溶液浓度偏低的是
A.洗涤了量取浓硫酸的量筒,并把洗涤液转移到容量瓶中
B.转移溶液前,容量瓶中含有少量蒸馏水
C.溶解硫酸用的烧杯、玻璃棒未洗涤
D.定容时俯视容量瓶的刻度线
|
参考答案:C
本题解析:洗涤了量取浓硫酸的量筒,会造成浓硫酸的量增多,浓度偏大,A错;转移溶液前,容量瓶中含有少量蒸馏水,对结果没有影响,B错;溶解硫酸用的烧杯、玻璃棒未洗涤,会造成硫酸有损失,使得浓度偏低,C对;定容时俯视容量瓶的刻度线,会造成体积变小,浓度偏大,D错。
考点:一定物质的量浓度溶液的配制的误差分析。
本题难度:一般
2、填空题 用锌片与稀硫酸反应,实验结果记录如表
次数
| 加入Zn质量/g
| 加入稀硫酸质量/g
| 生成ZnSO 4 质量/g
| 1
| 2
| 60
| 5
| 2
| 4
| 60
|
| 3
| 6
| 60
| 15
| 4
| 8
| 60
| 17
| 5
| 10
| 60
|
| 6
| 12
| 60
| 17
|
(1)第2、5两次产生ZnSO4 的质量依次是______________g.
(2)在图中画出ZnSO4 与Zn的质量函数关系的曲线.

(3)(10+m)g锌与60g稀硫酸充分反应后,剩余固体的质量为______________g.
(4)稀硫酸的溶质质量分数是______________.
参考答案:(1)10g、17g
(2)如图(若没有标出坐标值不对.根据硫酸锌的质量可以计算消耗锌的质量为6.9g)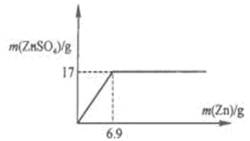
(3)(3.1g+m)g ; (4)17.2%
本题解析:根据表格中前4次的数据可以看出:硫酸的质量不变,Zn的质量增加,产生的ZnSO4 质量也逐渐增加,说明硫酸过量,原因第2次的质量是第一次的2倍,所以产生的ZnSO4质量也是第一次的2倍,质量是2×5g=10g;第四次产生ZnSO4质量是17g,第6次Zn质量增加,而产生的ZnSO4质量不变,说明硫酸反应完全,所以第5次加入Zn质量是10g时产生的ZnSO4质量也是17g;(2)65gZn完全反应会产生161g ZnSO4,则产生17g ZnSO4消耗的Zn的质量是:(17×65g)÷161=6.9g,则ZnSO4 与Zn的质量函数关系的曲线是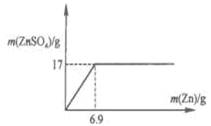 ; ;
(3)(10+m)g锌与60g稀硫酸充分反应后产生ZnSO4质量是17g,消耗Zn的质量是6.9gZn质量再增加,也不会发生反应,所以剩余固体的质量为(10+m)g-6.9g=(3.1g+m)g;(4)根据质量守恒定律可知在17g ZnSO4中含有的SO42-的质量是17g-6.9g=10.1g,则消耗的硫酸的质量是(98÷96)×10.1g=10.3g,所以稀硫酸的溶质质量分数是(10.3g÷60g)×100%=17.2%。
考点:考查实验数据的处理、图像法表示、物质的质量关系及溶液的质量分数的计算的知识。
本题难度:一般
3、简答题 用9mol/L的浓硫酸稀释成0.9mol/L的稀硫酸100mL,回答下列问题:
(1)需要取浓硫酸______?mL
(2)由于错误操作,使得到的浓度数据比正确的偏大,偏小或无影响
A.使用容量瓶配制溶液时,俯视液面定容后所得溶液的浓度______
B.没有用蒸馏水洗烧杯2-3次,并将洗液移入容量瓶中______
C.容量瓶用蒸馏水洗净,没有烘干______
D.定容时,滴加蒸馏水,先使液面略高于刻度线,再吸出少量水使液面凹面与刻度线相切______
E.把配好的溶液倒入用蒸馏水洗净而末干的试剂瓶中备用______.
参考答案:(1)根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,所以xmL×9mol/L=100mL×0.9mol/L,解得:x≈10.0.
所需浓硫酸的体积为10.0mL.
故答案为:10.0.
(2)A.定容时俯视刻度线,使溶液的体积偏小,所配溶液浓度偏大.
B.烧杯未进行洗涤,少量硫酸沾在烧杯壁与玻璃棒上,硫酸的实际物质的量减小,溶液浓度偏小;
C.最后需要定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响;
D.定容时,滴加蒸馏水,先使液面略高于刻度线,导致溶液体积增大,所配溶液浓度偏低,即使再吸出少量水使液面凹面与刻度线相切,剩余溶液浓度与原来配制的浓度相等,故浓度偏小;
F.把配好的溶液倒入用蒸馏水洗净而末干的试剂瓶中,溶液被稀释,试剂瓶内溶液浓度较配制的浓度偏小.
故答案为:偏大;偏小;无影响;偏小;偏小.
本题解析:
本题难度:一般
4、选择题 下列说法正确的是
A.摩尔是一种物理量
B.CO2的摩尔质量是44g
C.气体摩尔体积约为22.4 L
D.500mL0.1mol/LNaOH溶液中含溶质2g
参考答案:D
本题解析:略
本题难度:简单
5、选择题 下列有关微粒或物质的“量”的叙述不正确的是 (? )
A.浓度分别为2 mol/L和1 mol/L的Na2CO3溶液中,C(CO32一)的比值为2:1
B.常温常压下,16 g 02和O3混合气体中含有NA个氧原子
C.46 g NO2和N204混合气体的物质的量之和大于O.5 mol,小于l mol
D.向饱和CuS04溶液中加入1 mol CuS04固体,则析出的晶体的质量大于250 g
参考答案:A
本题解析:略
本题难度:简单
| 