1、选择题 下列溶液中有关微粒的物质的量浓度关系正确的是
A.在醋酸钠溶液中:c(CH3COOH) = c(OH-) - c(H+)
B.等体积等物质的量浓度的NaCl和NaClO溶液中离子总数:N前<N后
C.1mol?L-1的(NH4)2Fe(SO4)2?6H2O溶液中:c(NH4+)=c(SO42-)>c(Fe2+)>c(H+)
D.0.1 mol?L-1NaHX溶液pH=3,则此溶液中:c(HX-)>c(H2X)>c(X2-)
参考答案:A
本题解析:A.醋酸钠是强碱弱酸盐,水解使溶液显碱性C(OH-)=C(H+)(开始)= C(H+)(剩余)+ C(H+)(消耗)= c(H+)+ c(CH3COOH)。所以c(CH3COOH) = c(OH-) - c(H+)。正确。B.等体积等物质的量浓度的NaCl和NaClO,即二者的物质的量相等。混合后对NaClO溶液起到了稀释作用。由水解的离子方程式ClO-+H2O  ?HClO+OH-可看出混合前后溶液中离子总数不变。错误。C.电离方程式为:(NH4)2Fe(SO4)2=2NH4++Fe2++2 SO42-. NH4+发生水解反应NH4++H2O
?HClO+OH-可看出混合前后溶液中离子总数不变。错误。C.电离方程式为:(NH4)2Fe(SO4)2=2NH4++Fe2++2 SO42-. NH4+发生水解反应NH4++H2O NH3・H2O+H+。所以在溶液中:c(SO42-)>c(NH4+)。尽管Fe2+发生水解消耗,但盐电离产生的离子Fe2+比弱电解质水电离产生的离子H+浓度大。所以c(Fe2+)>c(H+)。故离子浓度的大小顺序是c(SO42-)>c(NH4+)> c(Fe2+)>c(H+)。错误。D. 在溶液中电离HX-
NH3・H2O+H+。所以在溶液中:c(SO42-)>c(NH4+)。尽管Fe2+发生水解消耗,但盐电离产生的离子Fe2+比弱电解质水电离产生的离子H+浓度大。所以c(Fe2+)>c(H+)。故离子浓度的大小顺序是c(SO42-)>c(NH4+)> c(Fe2+)>c(H+)。错误。D. 在溶液中电离HX- H++X2-使溶液显酸性,HX-+H2O
H++X2-使溶液显酸性,HX-+H2O  ?H2X +OH-使溶液显碱性。由于0.1 mol?L-1NaHX溶液pH=3,则由此可确定HX-的电离大于水解。故此溶液中:c(HX-)> c(X2-) >c(H2X)。错误。
?H2X +OH-使溶液显碱性。由于0.1 mol?L-1NaHX溶液pH=3,则由此可确定HX-的电离大于水解。故此溶液中:c(HX-)> c(X2-) >c(H2X)。错误。
本题难度:一般
2、选择题 下列关于溶液中离子的说法正确的是?
A.0.1mol・L-1的Na2CO3溶液中离子浓度关系:c(Na+)=2 c(CO )+ c(HCO
)+ c(HCO )+ c(H2CO3)
)+ c(H2CO3)
B.0.1mol・L-1的NH4Cl和0.1mol・L-1的NH3・H2O等体积混合后溶液中的离子浓度关系:
c(Cl-)> c(NH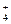 )> c(OH-)> c(H+)
)> c(OH-)> c(H+)
C.常温下,醋酸钠溶液中滴加少量醋酸使溶液的pH=7,则混合溶液中,离子浓度关系:
c(Na+)< c(CH3COO-)
D.等物质的量浓度、等体积的NH4NO3和KNO3溶液中,前者的阳离子浓度小于后者的阳离子浓度
参考答案:D
本题解析:略
本题难度:简单
3、填空题 以粗氧化锌粉(含FeO、Fe2O3、ZnS等)制取活性ZnO的工艺如下:
步骤1:以H2SO4浸出粗氧化锌,同时加入H2O2;
步骤2:过滤,调节滤液的pH;
步骤3:过滤,向滤液中加NH4HCO3,得碱式碳酸锌沉淀;
步骤4:过滤、洗涤、煅烧,得产品。
已知:离子沉淀的pH见下表。
离子
| 开始沉淀pH
| 沉淀完全pH
|
Fe2+
| 7.6
| 9.6
|
Fe3+
| 2.7
| 3.7
|
Zn2+
| 5.4
| 8.0
|
?
(1)加入H2O2时能浸出硫化锌,同时生成淡黄色固体,写出其化学方程式?。
(2)步骤2中调节溶液pH的范围是 ?。
(3)取洗涤、干燥后的碱式碳酸锌68.2 g,充分灼烧后测得残留物质的质量为48.6 g,将所得气体通入足量澄清石灰水中,得沉淀20 g。计算碱式碳酸锌的组成(用化学式表示,写出计算过程)。
参考答案:(1)ZnS+H2O2+H2SO4=ZnSO4+2H2O+S?
(2)3.7~5.4?(3)ZnCO3・2Zn(OH)2・H2O 或Zn3(OH)4CO3・H2O
[计算出n(ZnO) ,2分;计算出n(CO2), 2分;计算出ZnCO3・2Zn(OH)2・H2O,4分。]
本题解析:(1)淡黄色固体应该是硫,根据过氧化氢有强氧化性,做氧化剂,化学方程式ZnS+H2O2+H2SO4=ZnSO4+2H2O+S 。(2)步骤2中调节溶液pH只要满足锌离子不能沉淀,三价铁离子完全沉淀,故范围是 3.7~5.4 。(3)碱式碳酸锌68.2 g,充分灼烧后测得残留物质为氧化锌,质量为48.6 g,物质的量为48.6/81=0.6mol,锌的质量为39g。将所得气体是二氧化碳,沉淀碳酸钙是20 g,物质的量为0.2mol。碳酸根的物质的量为0.2mol。根据电苛守恒氢氧根的物质的量为0.8mol.由碱式碳酸锌68.2 g减去锌的质量,碳酸根和氢氧根的质量,剩下的就为水的质量,求得为0.2mol.故碱式碳酸锌的组成ZnCO3・2Zn(OH)2・H2O 或Zn3(OH)4CO3・H2O。
本题难度:一般
4、简答题 钠、镁、铁、铜及其化合物在科研和生产生活中有广泛的应用。
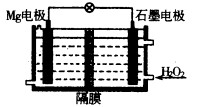
(1)Mg―H2O2电池可用于驱动无人驾驶的潜航器。该电池以海水为电解质溶液,结构如图所示。电池工作时,正极的电极反应式 ?。常温下,用该电池电解200mL的饱和硫酸铜溶液(电极为惰性电极),反应时溶液中水的电离平衡?移动(填“向左”“向右”或“不”);当消耗24mg金属Mg,电解后溶液的pH=?(不考虑溶液的体积变化)。
(2)利用电解法在铁制品上镀铜可以防止铁被腐蚀,以下说法正确的是?。
a.电镀时,铜和石墨都可以做阳极,可溶性铜盐作电解质溶液
b.电镀过程中,温度升高,电解反应速率加快
c.电镀过程中,电能全部转化为化学能
d.电镀过程中,铜离子向阴极移动,发生还原反应
(3)NaHS可作为沉淀剂除去溶液中的Cu2+。常温下,NaHS溶液显碱性,原因是?(用离子方程式和必要的文字说明)。向含有Cu2+的废水中加入少量NaHS固体,废水溶液的pH?(填“增大”“减小”或“不变”)。
参考答案:(1)H2O2+2e―=2OH―;向右;2;(2)ad;(3)HS―+H2O H2S+OH―HS―
H2S+OH―HS― H++S2―水解程度大于电离程度,溶液显碱性;减小。
H++S2―水解程度大于电离程度,溶液显碱性;减小。
本题解析:(1)本题考查原电池原理的应用、新型化学电源、电解原理的应用。由题给装置图分析Mg―H2O2电池中,镁作负极,发生氧化反应,H2O2在石墨电极上发生还原反应,作正极,电 极反应式为H2O2+2e―=2OH―;常温下,用该电池电解200mL的饱和硫酸铜溶液(电极为惰性电极),阳极反应为:2H2O - 4e-== O2↑ + 4H+,反应时溶液中水的电离平衡向右移动;当消耗24mg金属Mg,转移的电子为0.002mol,根据电子守恒结合阳极电极反应式知,产生的氢离子物质的量为0.002mol,氢离子浓度为0.01mol,电解后溶液的pH= 2;(2)考查电解原理的应用、电镀铜;a.电镀时,铜和石墨都可以做阳极,可溶性铜盐作电解质溶液,正确;b.电镀过程中,电解反应速率只与电流强度有关,错误;c.电镀过程中,电能不可能全部转化为化学能,错误;d.电镀过程中,铜离子向阴极移动,发生还原反应,正确,选ad;(3)NaHS为弱酸的酸式盐,常温下,NaHS溶液存在HS―的电离平衡:HS― H++S2―及水解平衡:HS―+H2O
H++S2―及水解平衡:HS―+H2O H2S+OH―,溶液显碱性的原因是HS―的电离程度小于HS―的水解程度;向含有Cu2+的废水中加入少量NaHS固体,Cu2+与S2―反应生成硫化铜沉淀,硫离子浓度减小,HS―的电离平衡:HS―
H2S+OH―,溶液显碱性的原因是HS―的电离程度小于HS―的水解程度;向含有Cu2+的废水中加入少量NaHS固体,Cu2+与S2―反应生成硫化铜沉淀,硫离子浓度减小,HS―的电离平衡:HS― H++S2―向右移动,氢离子浓度增大,废水溶液的pH减小。
H++S2―向右移动,氢离子浓度增大,废水溶液的pH减小。
本题难度:一般
5、选择题 某pH=1的ZnCl2和HCl的混合溶液中含有FeCl3杂质,通过水解除去杂质,需将溶液调至pH=4,在调节溶液pH时,应选用的试剂是
A.NaOH
B.ZnO
C.Na2CO3
D.Fe2O3
参考答案:B
本题解析:溶液中含有FeCl3杂质,将溶液调至pH=4,可使Fe3+水解生成Fe(OH)3沉淀而除去,可加入ZnO,不能加入其它三种物质,因都引入了新的杂质,故选B.
本题难度:一般