1、选择题 下列离子方程式中,只能表示一个化学反应的是
①Fe+Cu2+=Fe2++Cu?②Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓ ③H++OH-=H2O?④CO32-+2H+=CO2↑+H2O? ⑤Ba2++SO42-=BaSO4↓
A.只有①
B.只有②
C.②④
D.③⑤
参考答案:B
本题解析:分析:离子反应的实质是可以代表一类反应,但是有的离子反应只能表示一个化学反应,根据反应来寻找参加反应的反应物和生成物.
解答:①Fe+Cu2+=Fe2++Cu可以表示金属铁从可溶性的铜盐如:氯化铜、硝酸铜、硫酸铜中置换出金属铜的一类反应,故错误;?
②Ba2++2OH-+Cu2++SO42-=BaSO4↓+Cu(OH)2↓只能表示氢氧化钡和硫酸铜之间的反应,故正确;
③H++OH-=H2O代表强酸和强碱反应生成可溶于水的盐和水的反应如:盐酸和氢氧化钠、盐酸和氢氧化钡、硝酸和氢氧化钾等,故错误;?
④CO32-+2H+=CO2↑+H2O代表可溶性的碳酸盐和强酸之间的反应,如:碳酸钠和盐酸、碳酸钠和硝酸等,故错误;
⑤Ba2++SO42-=BaSO4↓代表可溶性的钡盐(或氢氧化钡)和硫酸(或可溶性的硫酸盐)反应,生成硫酸钡和可溶性的盐的一类反应,如:氢氧化钡和硫酸钠、硫酸和硝酸钡等,故错误.
故选B.
点评:本题考查学生离子反应的实质是可以代表一类反应,但是有的离子反应只能表示一个化学反应,可以根据所学知识进行回答,难度不大.
本题难度:一般
2、填空题 写出下列物质的电子式(4分)
H2O? 1??KOH? 2??
CO2:? 3??Na2O2:? 4?
参考答案:1?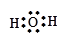 ?2?
?2? ?3?
?3?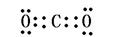 ?4?
?4?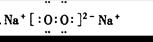
本题解析:1、为共价化合物,把元素最外层电子标出,共用电子对写在原子之间。2、离子化合物,注意有两个化学键,共价键和离子键。3、二氧化碳为共价化合物,碳和氧之间有两对共用电子对。4、过氧化钠的写法中,难点在于把过氧根离子写好。
点评:本题涉及到了常见物质的电子式的书写,离子化合物的电子式的书写注意阳离子的电子式为阳离子本身,而阴离子需要标出最外层所有的电子并打括号,带上电荷。共价化合物的电子式不带电荷,不打括号。
本题难度:一般
3、填空题 (10分)下图是工业生产硝酸铵的流程。
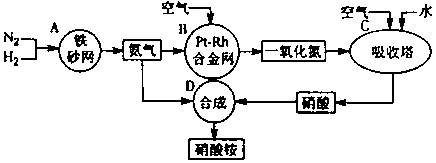
(1)吸收塔C中通入空气的目的是 。
A、B、C、D四个容器中的反应,属于氧化还原反应的是 (填字母)。
(2)已知:4NH3(g)+3O2(g)=2N2(g)+6H2O(g) △H = ―1266.8kJ/mol
N2(g)+O2(g)=2NO(g) △H=" " +180.5 kJ/mol
写出氨高温催化氧化的热化学方程式: ,氨催化氧化反应的化学平衡常数表达式K= 。
(3)已知: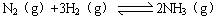 △H= ―92 kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
△H= ―92 kJ/mol。为提高氢气的转化率,宜采取的措施有 。(填字母)
A.升高温度 B.使用催化剂 C.增大压强
D.循环利用和不断补充氮气 E.及时移出氨
(4)在一定温度和压强下,将H2和N2按3:1(体积比)在密闭容器中混合,当该反应达到平衡时,测得平衡混合气中NH3的气体体积分数为17.6%,此时H2的转化率为 。
参考答案:(10分,第1小题每空1分,其余每空2分)
(1)使NO全部转化成HNO3 (1分) ABC(2分)
(2)4NH3(g)+5O2(g)=4NO(g)+6H2O(g) △H=-905.8kJ/mol(2分)
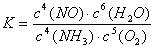 (1分)
(1分)
(3)CDE (2分)
(4)30%(或29.9%)(2分)
本题解析:略
本题难度:简单
4、选择题 据权威刊物报道,1996年科学家在宇宙中发现H3分子.甲、乙、丙、丁四位学生对此报道的认识正确的是( )
A.甲认为上述发现绝对不可能,因为H3分子违背了共价键理论
B.乙认为宇宙中还可能存在另一种氢单质,因为氢元素有三种同位素必然有三种同素异形体
C.丙认为H3分子实质上是H2分子与H+以特殊共价键结合的产物,应写成H3+
D.丁认为如果上述的发现存在,则证明传统的价键理论有一定的局限性有待继续发展
参考答案:A.因理论具有一定的时代性和局限性,宇宙中发现H3分子,则存在该分子,故A错误;
B.同位素的种类与同素异形体的种类无关,则可能还有氢单质,也可能没有,故B错误;
C.分子与离子是不同的微粒,所以H3分子不能写出H3+,故C错误;
D.H3分子的存在,利用传统的价键理论不能解释,即传统的价键理论有一定的局限性有待继续发展,故D正确;
故选D.
本题解析:
本题难度:简单
5、选择题 下列变化中,不需要破坏化学键的是( )
A.氯化氢溶于水
B.浓硝酸见光分解
C.冰雪融化
D.氯化钠熔化
参考答案:A.氯化氢溶于水时H-Cl共价键被破坏,故A不选;
B.浓硝酸见光分解发生化学反应,所以化学键一定被破坏,故B不选;
C.冰雪融化需克服分子间作用力,而化学键没有变化,故C选;
D.氯化钠熔化时破坏离子键,故D不选;
故选C.
本题解析:
本题难度:简单