1������� ijѧϰС����̽��CaSO4����ת��ΪCaCO3�������Ӷ������ȥ�Ŀ����ԣ�����������ϣ�(�������ݺ�ʵ���ָ��25���²ⶨ)
���ܵ����
| CaCO3
| CaSO4
|
Ksp(mol2��L��2)
| 3��10��9
| 9��10��6
|
ʵ�鲽�����£�
����100 mL 0.1 mol��L��1��CaCl2��Һ�м���100 mL 0.1 mol��L��1��Na2SO4��Һ�������а�ɫ�������ɡ�
������������Һ�м������Na2CO3 3 g�����裬���ã���������ȥ�ϲ���Һ��
���ټ�������ˮ���裬���ã�����������ȥ�ϲ���Һ��
��������м������������ᡣ
��1���������������Һ��[Ca2��]��________ mol��L��1
��2��д���ڢڲ�������Ӧ�����ӷ���ʽ��________________________________.
��3����Ƶڢ۲���Ŀ����________________________________________________��
��4���ڢܲ���������������Ϊ�� ��
2��ѡ���� 25��ʱ�������������ε�Ksp����ɫ���ұ�������˵����ȷ����
| AgCl
| Ag2CrO4
| AgI
|
��ɫ
| ��
| ש��
| ��
|
Ksp
| 1.8��10-10
| 1.0��10-12
| 8.5��10-17
|
A��AgCl��Ag2CrO4��AgI������Һ��c(Ag+)���μ�С
B��Ag2CrO4������Һ��c��Ag+��ԼΪ1.0��10-6mol��L-1
C����AgCl����Һ��������KI��Һ���������ɰ�ɫת��Ϊ��ɫ
D�����Ũ�ȵ�KCl��K2CrO4�����Һ�еμ�����AgNO3��Һ��������ש��ɫ����
3��ѡ���� ���л�ѧԭ����Ӧ�ã���Ҫ�ó����ܽ�ƽ��ԭ�������͵���? (? )
���ȴ�����Һ��ϴ����������ǿ��������[BaCl2.Ba(NO3)2]����ʳ��ʳ�ú���0.5�G��Na2SO4��Һ�ⶾ�����ܶ�.ɺ�����γɣ���̼�ᱵ�����������͡������ᱵ���ܣ�����ĭ���������ԭ����
A���ڢۢ�
B���٢ڢ�
C���ۢܢ�
D��ȫ��
4������� �ظ����ι㷺������������Ƥ�������ȡ��Ը���ʯ����Ҫ�ɷ���Cr2O3����FeO��Al2O3�� SiO2������)Ϊԭ����ȡ�ظ����Ƶ��������£�
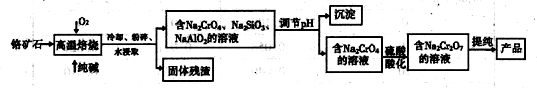
��ش��������⣺
��1��д��Cr2O3�ڸ��±���ʱ��Ӧ�Ļ�ѧ����ʽ______________________
��2��д�������ữʹNa-2CrO4ת��ΪNa2Cr2O7�����ӷ���ʽ ______________��
��3��ij��������ʯī�缫���Na2CrO4��Һ��ʵ ���� Na2CrO4��? Na2Cr2O7��ת������ԭ����ͼ��ʾ��

�������ӽ���Ĥ��һ�ֲ����Ǿ۱�ϩ����(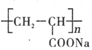 )���۱�ϩ���Ƶ���Ľṹ��ʽ��________��
)���۱�ϩ���Ƶ���Ľṹ��ʽ��________��
��д�������ĵ缫��Ӧʽ__________
��4�� Na2Cr2O7�����ڲⶨ��ˮ�Ļ�ѧ����������COD��ָÿ��ˮ���л�ԭ�����ʱ����� ����ҪO2��������������ijˮ��100��00 mL���ữ�����C1 mol/L��Na2Cr2O7��Һ V1 mL��ʹˮ�еĻ�ԭ��������ȫ��������Cr2O72-��ԭΪCr3+��������C2mol/L��FeSO4��Һ�ζ�ʣ ���Cr2O72-���������FeSO4��ҺV2 mL��
�ٸ�ˮ����CODΪ______________mg/L��
�ڼ���������Ӧ��������Һ��Fe3+��Cr3+�����ʵ���Ũ�Ⱦ�Ϊ0��1 mol/L��ҪʹFe3 +�� ����ȫ��Cr3+��δ��ʼ���������������ҺpH�ķ�Χ�� _______��
(�����õ������ݣ�KSPFe(OH)3=4��0��10-38, KSPCr(OH)3=6��0��10-31��
5������� ���û�ѧ��Ӧԭ���о��������ȡ���ȵ��ʼ��仯����ķ�Ӧ����Ҫ����
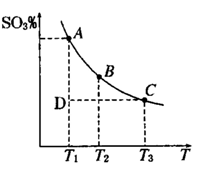
��1�����������У�SO2����������SO3�� 2SO2��g��+O2��g�� 2SO3��g���������ϵ��SO3 �İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣬
2SO3��g���������ϵ��SO3 �İٷֺ������¶ȵĹ�ϵ����ͼ��ʾ���������κ�һ�㶼��ʾƽ��״̬��������ͼʾ�ش��������⣬
��2SO2��g��+O2��g�� 2SO3��g���ġ�H 0
2SO3��g���ġ�H 0
���>����<���������ں��¡���ѹ������������ƽ����ϵ��ͨ�뺤����ƽ�� �ƶ�����������ҡ�������
�����¶�ΪT1��T2����Ӧ��ƽ�ⳣ���ֱ�ΪK1��K2����K1 K2����Ӧ���е�״̬Dʱ�� 
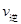 ���>����<����=����
���>����<����=����
��2�����ǵ����Ϻ����ḻ��һ��Ԫ�أ������仯�����ڹ�ũ ҵ������������������Ҫ���ã�
����ͼ��һ�����¶Ⱥ�ѹǿ��N2��H2��Ӧ����lmolNH3�����������仯ʾ��ͼ����д����ҵ�ϳɰ����Ȼ�ѧ����ʽ��
����H����ֵ�ú���ĸQ1��Q2�Ĵ���ʽ��ʾ��
�ڰ�������ˮ�õ���ˮ����25���£���a mol��L-1�İ�ˮ��b mol��L-1������������ϣ���Ӧ����Һ�����ԣ���c��NH4+�� c��Cl-�����>������<����=�������ú�a��b�Ĵ���ʽ��ʾ���û����Һ�а�ˮ�ĵ���ƽ�ⳣ�� .
��3����ˮ�к��д�����Ԫ�أ�����Ԫ�����ȣ���Ԫ����⣬���ں�ˮ�о��Ի���̬���ڣ���25���£���0��1L0.002mol��L-l��NaCl��Һ����μ���������0��1L0.002mol��L-l��������Һ���а�ɫ�������ɣ��ӳ����ܽ�ƽ��ĽǶȽ��Ͳ���������ԭ���� ����Ӧ�����Һ�м�������0��1L0.002mol��L-1��NaI��Һ�������������� �������������ԭ���ǣ������ӷ���ʽ��ʾ�� ��
����֪��25��ʱKSP��AgCl��=1.6��l0-10 KSP��AgI��=1.5��l0-16��