1��ѡ���� �±����������ε��ܶȻ�����(25 ��)�������й�˵���������(����)
��ѧʽ
| AgCl
| Ag2SO4
| Ag2S
| AgBr
| AgI
|
�ܶȻ�
| 1.8��10��10
| 1.4��10��5
| 6.3��10��50
| 7.7��10��13
| 8.5��10��16
|
A.���������ڳ������ܽ��������Ag2SO4
B����AgCl�ܽ���ˮ�������м���Na2S����������ɺ�ɫ��Ag2S����
C�������ܽ�ƽ��Ľ������������ģ���������ı�ʱ��ƽ��Ҳ�ᷢ���ƶ�
D�������£�AgCl��AgBr��AgI�������ʵ��ܽ��������
�ο��𰸣�D
�������������Ksp���Կ���Ag2SO4���ܽ�����A�ԡ��ܽ�ȴ������������ת����ܽ��С�������B�ԡ���������ı䣬�����ܽ�ƽ���ƶ���C�������Դ����ѡ����D��
������Ksp����ֱ��ȷ���ܽ�ȵĴ�С�����Ƕ���ͬһ���͵����ʣ�KspԽ���ܽ��Խ��
�����Ѷȣ�һ��
2������� ��ͼ��ij�о���ѧϰС����ƵĶ�һ�ַϾɺϽ�ĸ��ɷ֣�����Cu��Fe��Si ���ֳɷ֣����з��롢���������õĹ�ҵ���̣�ͨ�������̽����ɷ�ת��Ϊ���õĵ��ʼ������
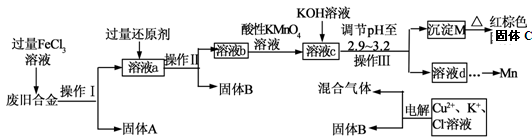
��֪��298Kʱ��Ksp[Cu(OH)2]=2.2��10-20��Ksp[Fe(OH)3]=4.0��10-38�� Ksp[Mn(OH)2] =1.9��10-13��
�����������̻ش��й����⣺
��1��������ָ����?��
��2���������FeCl3��Һ�����п����漰�Ļ�ѧ����ʽ��?��
��3�������Ļ�ԭ��Ӧ��?��
��4��������Һb�м�������KMnO4��Һ������Ӧ�����ӷ���ʽΪ?��
������X mol/L KMnO4��Һ������Һb����ǡ�ý���Һ�е���������ȫ����ʱ����KMnO4��ҺYmL����������ú���ɫ����C������Ϊ?g���ú�X��Y�Ĵ���ʽ��ʾ����
��5��������,����Һc�������Ľ���������Ũ����ȣ�����Һc����μ���KOH��Һ�������ֽ��������ӳ������Ⱥ�˳��Ϊ��?��?��??��(�����������)
��6�����һ��������ö��Ե缫���һ��ʱ�����������B������ΪZ g��ͬʱ������������ռ��������������ȣ��������������ɵ����һ���������Ϊ?L���ú�Z�Ĵ���ʽ��ʾ�����õ缫�ķ�ӦʽΪ? .
�ο��𰸣���1�����ˣ�1�֣�
��2��2FeCl3 +Fe = 3FeCl2��2�֣���? 2FeCl3 + Cu= 2FeCl2 +CuCl2��2�֣�
��3��Cu�ۣ�2�֣�?
��4����? MnO4�� + 5Fe2+ + 8H+= Mn2++ 5Fe3++4H2O��2�֣�?�� 0.4XY��2�֣�
��5��Fe3+��Cu2+��Mn2+��2�֣�?
��6��22.4Z/64 ��2�֣���? 4OH��?�D4e����O2��?+ 4H2O��2�֣�
��������������������ͼ����Ϣ֪���ϾɺϽ𣨺���Cu��Fe��Si ���ֳɷ֣������FeCl3��Һ��Ϸ����ķ�ӦΪ2FeCl3 +Fe = 3FeCl2��2FeCl3 + Cu= 2FeCl2 +CuCl2�����ˣ�����A�ijɷ�ΪSi����Һa�ijɷ�ΪFeCl3 ��FeCl2 ��CuCl2�Ļ��Һ����⺬Cu2+��Cl����K+����Һ�Ĺ���B��B�ijɷ�ΪCu����Һa�ӹ�����ԭ����Ӧ����˵ù���B��Cu������ԭ��Ϊͭ�������ķ�ӦΪ2FeCl3 + Cu= 2FeCl2 +CuCl2����Һb�ijɷ�ΪFeCl2 ��CuCl2�Ļ��Һ����Һb�м������Ը��������Һ���������ӱ�����Ϊ�����ӣ�������������Һ������Һ��PH��������ת��Ϊ�����������������յ�����������Һd�������Ľ����̡���1��������ͼ֪��������Ϊ�����Һ�����IJ�����ָ���ǹ��ˣ���2���������FeCl3��Һ�����п����漰�Ļ�ѧ����ʽ��2FeCl3 +Fe = 3FeCl2��2FeCl3 + Cu= 2FeCl2 +CuCl2����3������������֪�������Ļ�ԭ��Ӧ��Cu�ۣ���4��������Һb�м�������KMnO4��Һ�������ӱ�����Ϊ�����ӣ���Ӧ�����ӷ���ʽΪMnO4�� + 5Fe2+ + 8H+= Mn2++ 5Fe3++4H2O���ڸ�����ط�Ӧ�Ĺ�ϵʽ��2MnO4������ 10Fe2+����5Fe2O3����X mol/L KMnO4��Һ������Һb����ǡ�ý���Һ�е���������ȫ����ʱ����KMnO4��ҺYmL����������ú���ɫ����C������Ϊ0.4XYg����5����������֪����Һc�������Ľ���������ΪFe3+��Cu2+��Mn2+��������Ũ����ȣ�����Һc����μ���KOH��Һ����������ܶȻ������жϣ�Fe3+����������Ũ����С�ȳ�����Mn2+����������Ũ������������������ֽ��������ӳ������Ⱥ�˳��Ϊ��Fe3+��Cu2+��Mn2+����6����������֪�������̵ĵ缫��Ӧʽ����Ϊ��������4OH��?�D4e����O2��?+ 4H2O��������Cu2+ + 2e-= Cu��2H+ + 2e- = H2�������ݵ����غ���㣬������������ɵ����һ���������Ϊ22.4Z/64L��
�����Ѷȣ�����
3������� ���ô�������Ӧ��SO2ת��ΪSO3�ǹ�ҵ����������Ĺؼ����裮
��֪��SO2+
O2?SO3��H=-98KJ?mol-1
��1����T1�¶�ʱ���÷�Ӧ��ƽ�ⳣ��K=�����ڴ��¶��£���100L�ĺ����ܱ������У�����3.0molSO2��16.0molO2��3.0molSO3����Ӧ��ʼʱ����Ӧ����______�淴Ӧ���ʣ����������������=������
��2����T2�¶�ʱ����ʼ��100L���ܱ������м���4.0molSO2��10.0molO2��һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����196kJ����ʱ���������ת����Ϊ______��
��3���ڣ�2���еķ�Ӧ�ﵽƽ��ı�������������ʹSO2ƽ��Ũ�ȱ�ԭ����С����______������ĸ����
A�������¶Ⱥ�����������䣬����1.0molO2
B�������¶Ⱥ�������ѹǿ���䣬����2.0molSO2��5.0molO2
C�������¶�
D����������������ʱ����С�������ݻ�
��4��������������ͼ��ʾװ���õ绯ѧԭ���������ᣬд��ͨ��SO2�ĵ缫�ĵ缫��Ӧʽ��______��
��5����������Ƶ������Σ���һ���¶��£���K2SO4��Һ�еμ�Na2CO3��Һ��BaCl2��Һ�������ֳ�������ʱ��=______��[��֪���¶�ʱ��KSP(BaSO4)=1.3��10-10��KSP(BaCO3)=5.2��10-9]��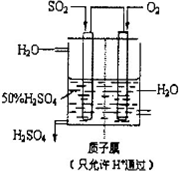
�ο��𰸣���1��SO2+12O2?SO3��H=-98KJ?mol-1����100L�ĺ����ܱ������У�����3.0molSO2��16.0molO2��3.0molSO3��
��ΪŨ����QC=c(SO3)c(SO2)[c(O2)]12=3.0mol100L3.0mol100L��(16.0mol100L)12=2.5��K�����Ի�ѧ��Ӧ������У���v��������v���棩���ʴ�Ϊ������
��2����T2�¶�ʱ����ʼ��100L���ܱ������м���4.0molSO2��10.0molO2��һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����196kJ����1molSO2��ȫ��Ӧ����98KJ����һ�������µ���Ӧ�ﵽƽ��ʱ���ų�����196kJ�����Ķ����������ʵ���=1mol��196KJ98KJ=2mol�����ݻ�ѧƽ������ʽ��ʽ���㣺
? ?SO2��g��+12O2��g��?SO3��g��
��ʼ����mol��?4? 10? 0
�仯����mol��? 2? 1?2
ƽ������mol�� ?2?9? 2
����SO2��ת���ʦ�=2mol4mol��100%=50%���ʴ�Ϊ��50%��
��3��A�������¶Ⱥ�����������䣬O2��Ũ������ƽ�������ƶ���SO2��Ũ�ȼ�С������A��ȷ��
B�������¶Ⱥ�������ѹǿ���䣬����2.0molSO2��5.0molO2���µ�ƽ����ԭƽ���Ч��SO2��Ũ�Ȳ��䣬����B����
C�������¶ȣ�ƽ������ȵķ����ƶ���������ӦΪ���ȣ�����ƽ�������ƶ���SO2��Ũ�ȼ�С������C��ȷ��
D����������������ʱ����С�������ݻ���SO2��Ũ��˲������֮��ƽ��������������ٵķ����ƶ�����������Ӧ�����ƶ���SO2��Ũ�ȼ�С���ٴε���ƽ��ʱSO2��Ũ���Ա�ԭ��������D����
�ʴ�Ϊ��A��C��
��4������ͼװ�÷�������������ʧ���ӷ���������Ӧ��������������Ϊ������������ˮ��������缫��ӦΪ��SO2+2H2O=SO42-+4H++2e-��
�ʴ�Ϊ��SO2+2H2O=SO42-+4H++2e-��?
��5����һ���¶��£���K2SO4��Һ�еμ�Na2CO3��Һ��BaCl2��Һ�������ֳ�������ʱ�������ܶȻ�������֪���������ᱵ��������ת����BaCO3+SO42-=BaSO4+CO32-�����̼�ᱵ�����ᱵ�ܶȻ�������
c(CO22-)c(SO42-)=Ksp(BaCO3)Ksp(BaSO4)=5.2��10-91.3��10-10=40��
�ʴ�Ϊ��40��
���������
�����Ѷȣ�һ��
4��ѡ���� ��֪Ksp(AgCl)��1.8��10��10��Ksp(AgI)��8.5��10��17�����й���������֮��ת����˵���д������? (����)
A��AgCl������ˮ������ת��ΪAgI
B�������������Ksp���Խ���������Խ����ת��Ϊ�����ܵ�����
C��AgI��AgCl��������ˮ������AgCl����ת��ΪAgI
D�������£�AgCl��Ҫ��NaI��Һ�п�ʼת��ΪAgI����NaI��Ũ�ȱ��벻����6.34��10��12mol��L��1
�ο��𰸣�A
���������Ksp(AgI)С��Ksp(AgCl)��AgI��AgCl��������ˮ��AgCl����ת��ΪAgI������AgCl��Һ��Ag��Ũ��Ϊ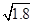 ��10��5 mol��L��1������c(Ag��)��c(I��)>Ksp(AgI)ʱ����AgI������I����Ũ�ȱ��벻����
��10��5 mol��L��1������c(Ag��)��c(I��)>Ksp(AgI)ʱ����AgI������I����Ũ�ȱ��벻����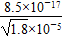 mol��L��1��6.34��10��12 mol��L��1��
mol��L��1��6.34��10��12 mol��L��1��
�����Ѷȣ���
5��ѡ���� ����ʱ��CaCO3��ˮ�еij����ܽ�ƽ��������ͼ��ʾ����֪CaCO3���ܶȻ������£�Ϊ2.8��10-9,����˵��?�в���ȷ���ǣ�?��
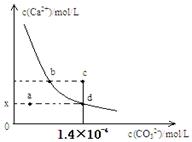
A��x����ֵΪ2��10-5
B��c��ʱ��CaCO3����
C����������ˮ��ʹ��Һ��d����a��
D��b����d���Ӧ���ܶȻ����
�ο��𰸣�C
�����������
�����Ѷȣ���