1、填空题 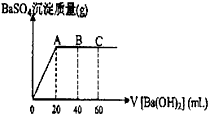
在t℃时,稀硫酸和盐酸混合液中,c(H+)=10-a mol・L-1,c(OH-)=10-b mol・L-1,已知a+b=12.向20mL该混合酸溶液中逐滴加入pH=11Ba(OH)2溶液,生成BaSO4的量如上图所示,当加入60mL Ba(OH)2溶液时,C点溶液的pH=6(体积变化忽略不计),
试计算:
(1)最初混合酸溶液中c(H2SO4)=___________ ,c(HCl)= ____________;
(2)A点pH=____________________ ;
(3)B点比最初混合酸的pH增加多少(写出计算过程)?(lg3=0.48) ____________________________________________________________________。
参考答案:(1)c(H2SO4)=0.05mol・L-1,c(HCl)=0.20mol・L-1
(2)pH=1
(3)最初混合酸c(H+)=0.05mol・L-1×2+0.20mol・L-1=0.30mol・L-1 pH=0.52 B点还没有完全中和,酸有剩余 c(H+)= =mol・L-1 pH=1.48,
所以B点比最初混合酸的pH增加1.48-0.52=0.96
本题解析:
本题难度:一般
2、选择题 在10mL0.1mol?L-NaOH溶液中加入同体积、同浓度的HAc溶液,反应后溶液中各微粒的浓度关系正确的是( )
A.c(Na+)>c(Ac-)>c(H+)>c(OH-)
B.c(Na+)=c(Ac-)>c(OH-)=c(H+)
C.c(OH-)=c(H+)+c(HAc)
D.2c(Na+)+c(H+)=2c(Ac-)+c(OH-)+c(HAc)
参考答案:A、相同物质的量的醋酸氢氧化钠碱恰好完全反应,生成醋酸钠,醋酸钠是强碱弱酸盐能水解导致溶液呈碱性,即氢氧根离子的物质的量浓度大于氢离子的物质的量浓度,故A错误.
B、相同物质的量的醋酸氢氧化钠碱恰好完全反应,生成醋酸钠,醋酸钠是强碱弱酸盐能水解导致溶液呈碱性,即氢氧根离子的物质的量浓度大于氢离子的物质的量浓度,故B错误.
C、相同物质的量的醋酸氢氧化钠碱恰好完全反应,生成醋酸钠,n(Na+)=0.001mol,根据物料守恒知,n(Ac-)+n(HAc)=0.001mol,根据电荷守恒知,n(Na+)+n(H+)=n(Ac-)+n(OH-),所以n(OH-)=n(H+)+n(HAc),同一溶液中溶液的体积相同,所以C(OH-)=c(H+)+c(HAc),故C正确.
D、根据电荷守恒得nC(Na+)+C(H+)=C(Ac-)+C(OH-),根据物料守恒得C(Na+)=n(Ac-)+n(HAc)=0.001mol,所以2C(Na+)+c(H+)=2c(Ac-)+c(OH-)+c(HAc),故D正确.
故选CD.
本题解析:
本题难度:一般
3、选择题 室温下,将PH分别为12和2、体积相等的氨水和盐酸两种溶液混合后所得溶液的酸碱性判断正确的是( ? )
A.混合后溶液呈酸性
B.混合后溶液呈碱性
C.混合后溶液呈中性
D.无法确定
参考答案:B
本题解析:
本题难度:一般
4、选择题 有人建议用AG表示溶液的酸度,AG的定义为AG=lg
.下列表述不正确的是( )
A.在25℃时,若溶液呈中性,则pH=7,AG=1
B.在25℃时,若溶液呈酸性,则pH<7,AG>0
C.在25℃时,若溶液呈碱性,则pH>7,AG<0
D.在25℃时,溶液的pH与AG的换算公式为:AG=2(7-pH)
参考答案:A.在25℃时,若溶液呈中性,C(H+)=C(OH-)=1×10-7mol?L-1,pH=-lgC(H+)=lg(10-7)=7,AG=lgC(H+)C(OH-)=lg1=0,故A错误;
B.在25℃时,若溶液呈酸性,则C(H+)>C(OH-),即C(H+)>10-7mol?L-1,故pH<7,AG=lgC(H+)C(OH-)>lg1,即AG>0,故B正确;
C.在25℃时,岩溶液呈碱性,则C(H+)<C(OH-),即C(OH-)>10-7mol?L-1,故pH>7,AG=lgC(H+)C(OH-)<lg1,即AG<0,故C正确;
D.在25℃时,KW=C(H+)×C(OH-)=10-14,C(OH-)=kwc(H+),PH=-lgc(H+),根据AG和pH的计算公式可得AG=lgC(H+)C(OH-)=lgC(H+)10-14C(H+)=2(7-pH),故D正确;
故选A.
本题解析:
本题难度:简单
5、简答题 将等体积的氨水与盐酸溶液混和后,若混和溶液中[NH4+]=[Cl-],则溶液中的pH值为______7,混和前[NH3?H2O]______[HCl],氨水中[OH-]______盐酸中[H+].(填>、<或=,下同)
参考答案:反应后溶液呈电中性,则溶液中存在:c(NH4+)+c(H+)=c(Cl-)+c(OH-),因c(NH4+)=c(Cl-),则c(H+)=c(OH-),
所以溶液PH=7,
如等浓度、等体积混合,则完全反应生成NH4Cl,NH4+水解呈酸性,而溶液呈中性,则氨水需过量.所以混合前氨水浓度大于盐酸浓度,即c(NH3?H2O)>c(HCl),
因氨水为弱电解质,且c(NH3?H2O)>c(HCl),如氨水中c(OH-)≥盐酸中c(H+),则反应后溶液呈碱性,
所以氨水中c(OH-)<盐酸中c(H+),
故答案为:=,>,<.
本题解析:
本题难度:一般