| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高中化学知识点总结《物质的量》试题预测(2020年最新版)(四)
参考答案:(1)18.4 (2)6.8 本题解析:(1)硫酸质量为500乘以1.84乘以0.98等于901.6克,则硫酸物质的量为901.6除以98等于9.2mol,则硫酸物质的量浓度为9.2除以0.5等于18.4 mol/L;(2)稀释前后溶质物质的量不变,即250乘以0.5等于18.4V,则V等于6.8mL;(3)配制一定物质的量浓度溶液所需的仪器:量筒、250mL容量瓶、烧杯、玻璃棒;(4)定容时,若加入的水超过刻度线,必须采取的措施是重新配制溶液;(5)A、溶质的量减少,所配的浓度偏低;B、定容时还需加蒸馏水,所以容量瓶用蒸馏水洗净后仍残留蒸馏水,对实验结果无影响;C、定容时,俯视容量瓶,所配的溶液浓度偏高;D、定容后,再加水,相等于稀释溶液,浓度偏低。 本题难度:困难 2、填空题 (14分)(1)448mL某气体在标准状况下的质量为1.28g,该气体的摩尔质量约为 参考答案:(1)64g/mol;(2)62g/mol 16 (3)220g ; 112L; 3.01×1024; 6.02×1024 本题解析:略 本题难度:一般 3、填空题 现用98%的浓H2SO4( |
参考答案:(1)AEFDCB;(2)①13.6?②15?偏低?③防止暴沸,使稀释浓硫酸产生的热量及时散发出去?偏低?④ 静置冷却?偏高?偏低?⑤偏高?偏低(每一个空1分)
本题解析:(1)本题考查一定物质的量浓度溶液配制的操作步骤;操作步骤有计算、量取、溶解、移液、洗涤、定容、摇匀等操作,其操作正确顺序为AEFDCB;(2)①根据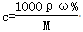 计算浓H2SO4的物质的量浓度为18.4mol/L,根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=500mL×0.5mol/L,解得:x=13.6mL;②量取13.6mL浓硫酸,需要使用15mL的量筒;量取时发现量筒不干净用水洗净后直接量取,浓硫酸被蒸馏水稀释,导致浓硫酸的浓度偏低,将使实验最终结果偏低;③浓硫酸稀释放热,将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是防止暴沸,使稀释浓硫酸产生的热量及时散发出去,若搅拌过程中有液体溅出,溶质损失,会使最终结果偏低;④浓硫酸稀释放热,溶液的温度升高,转移前必须冷却稀释的溶液,否则冷却后配制的溶液的体积偏低,最终导致浓度偏高;洗涤烧杯和玻璃棒2~3次,洗液也要转入容量瓶,否则会使配制的溶液中溶质的物质的量减小,浓度偏低;⑤定容时俯视,导致溶液体积偏小,所配溶液的浓度偏高;若仰视,导致溶液的体积偏大,配制的溶液浓度偏低。
计算浓H2SO4的物质的量浓度为18.4mol/L,根据稀释定律,稀释前后溶质硫酸的物质的量不变,设浓硫酸的体积为xmL,所以xmL×18.4mol/L=500mL×0.5mol/L,解得:x=13.6mL;②量取13.6mL浓硫酸,需要使用15mL的量筒;量取时发现量筒不干净用水洗净后直接量取,浓硫酸被蒸馏水稀释,导致浓硫酸的浓度偏低,将使实验最终结果偏低;③浓硫酸稀释放热,将浓H2SO4沿烧杯内壁慢慢注入盛水的烧杯中,不断搅拌的目的是防止暴沸,使稀释浓硫酸产生的热量及时散发出去,若搅拌过程中有液体溅出,溶质损失,会使最终结果偏低;④浓硫酸稀释放热,溶液的温度升高,转移前必须冷却稀释的溶液,否则冷却后配制的溶液的体积偏低,最终导致浓度偏高;洗涤烧杯和玻璃棒2~3次,洗液也要转入容量瓶,否则会使配制的溶液中溶质的物质的量减小,浓度偏低;⑤定容时俯视,导致溶液体积偏小,所配溶液的浓度偏高;若仰视,导致溶液的体积偏大,配制的溶液浓度偏低。
本题难度:一般
4、选择题 在硫酸、明矾和硫酸铝组成的混合溶液中,c(Al3+)="0.3" mol・L-1,c(SO42-)=0.7mol・L-1, 由水电离的c(H+)=10-13 mol・L-1,则c(K+)为
A.0.15mol・L-1
B.0.2mol・L-1
C.0.3mol・L-1
D.0.4mol・L-1
参考答案:B
本题解析:由水电离的c(H+)=10-13 mol・L-1,所以由水电离的c(OH―)=10-13 mol・L-1,说明水的电离主要受到硫酸电离的抑制。所以溶液中的c(H+) =10-1 mol・L-1,c(OH―)=10-13 mol・L-1,根据电荷守恒可得正确答案为B。
本题难度:一般
5、填空题 在标准状况下1.7g氨气所占的体积为 ,它与同条件下 mol H2S含有相同的氢原子。
参考答案:2.24L 0.15mol
本题解析:氨气的物质的量为:n=m/M=1.7g÷17g/mol=0.1mol,在标准状况下的体积为V=n×22.4L/mol=2.24L,H的物质的量为n(H)=0.1mol×3=0.3mol, H2S的物质的量为n(H2S)=0.3mol÷2=0.15mol。
考点:有关有关物质的量的计算。
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点归纳《物质结构和.. | |