|
|
|
高中化学知识点总结《化学反应与能量》典型例题(七)
2021-02-18 05:13:37
【 大 中 小】
|
1、选择题 已知:①1 mol H2分子中化学键断裂时需要吸收436 kJ的能量;②1 mol Cl2分子中化学键断裂时需要吸收
243 kJ的能量;③由H原子和Cl原子形成1 mol HCl分子时释放431 kJ的能量。下列叙述正确的是
[? ]
A.氢气和氯气反应生成氯化氢气体的热化学方程式是H2(g)+Cl2(g)=2HCl(g)
B.氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH=183 kJ・mol-1
C.氢气和氯气反应生成2 mol氯化氢气体,反应的ΔH=-183 kJ・mol-1
D.氢气和氯气反应生成1 mol氯化氢气体,反应的ΔH=-183 kJ・mol-1
2、选择题 某实验小组学生按照课本实验要求,用50 mL 0.5 mol・L-1盐酸与50 mL 0.55 mol・L-1 NaOH溶液在如图所示的装置中进行中和反应。通过测定反应过程中放出的热量计算中和热。下列说法正确的是
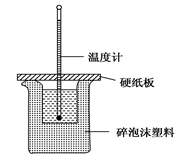
A.实验过程中没有热量损失
B.图中实验装置缺少环形玻璃搅拌棒
C.烧杯间填满碎泡沫塑料的作用是固定小烧杯
D.酸或碱的物质的量越大,所测中和热的数值越大
|
3、选择题 下列说法中错误的是
A.化学反应必然伴随发生能量变化。
B.化学变化中的能量变化主要是由化学键变化引起的。
C.能量变化是化学反应的基本特征之一。
D.化学变化中能量变化的大小与反应物的质量的多少无关。
|
4、填空题 (12分)红磷P(s)和Cl2(g)发生反应生成 PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。

根据上图回答下列问题:
(1)P和Cl2反应生成PCl3的热化学方程式______________________________。
(2)PCl5分解成PCl3和Cl2的热化学方程式_________________ ____
(3)P和Cl2分两步反应生成1molPCl5的△H3=_________,P和Cl2一步反应生成1molPCl5的△H4______△H3(填“大于”、“小于”或“等于”)。
5、填空题 实验室利用如图装置进行中和热的测定。回答下列问题:
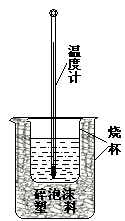
(1)该图中有两处实验用品未画出,它们是 、 ;
(2)在操作正确的前提下提高中和热测定的准确性的关键是: 。
(3)如果用0.5mol?L-1的盐酸和氢氧化钠固体进行实验,则实验中所测出的“中和热”将 (填“偏大”、“偏小”、“不变”)原因是 。
 PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
PCl3(g)和PCl5(g)。反应过程和能量关系如图所示(图中的△H表示生成1mol产物的数据)。
