1、选择题 下列关于晶体的说法一定正确的是(?)
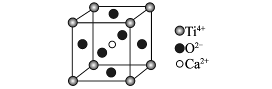
CaTiO3的晶体结构模型(图中Ca2+、O2-、
Ti4+分别位于立方体的体心、面心和顶点)
A.分子晶体中都存在共价键
B.CaTiO3晶体中每个Ti4+与12个O2-相邻
C.SiO2晶体中每个硅原子与两个氢原子以共价键相结合
D.金属晶体的熔点都比分子晶体的熔点高
参考答案:B
本题解析:有些单原子分子晶体中不存在共价键,如稀有气体构成的晶体,A错;因在晶体中Ti4+位于顶点而O2-位于面心,所以CaTiO3晶体中每个Ti4+与12个O2-相邻,B正确;SiO2晶体、Si原子与4个O原子以共价键结合,C错;金属晶体中有些比分子晶体的熔点低,如汞常温下为液体,D错。
本题难度:简单
2、填空题 (12分)硫酸铜是一种重要的化工原料,工业上常用硫酸为原料来制备硫酸铜。
(1)工业上生产硫酸过程中,焙烧硫铁矿时产生的废渣是一种二次资源。
①为了从废渣中磁选获得品位合格的铁精矿,高温下利用CO使弱磁性Fe2O3转化为强磁性Fe3O4。写出该反应的化学方程式?;实验发现:CO太多或太少都会导致磁铁矿产率降低,原因是?。
②氯化焙烧工艺是将废渣用氯化钙水溶液调和、成球、高温焙烧,废渣中SiO2与CaCl2等在高温下反应放出HCl,HCl与金属氧化物等反应生成氯化物。反应生成的各金属氯化物以气态形式逸出,进而回收有色金属和回返氯化钙溶液。写出氯化焙烧工艺中生成HCl的化学方程式?。
(2)测定硫酸铜品体中结品水含量的实验步骤为:
步骤1:准确称量一个洁净、干燥的坩埚;
步骤2:将一定量的硫酸铜晶体试样研细后,放入坩埚中称重
步骤3:将盛有试样的坩埚加热,待晶体变成白色粉末时,停止加热;
步骤4:将步骤3中的坩埚放入干燥器,冷却至室温后,称重:
步骤5:?;
步骤6:根据实验数据计算硫酸铜晶体试样中结晶水的质量分数。
请完成实验步骤5。?
(3)已知硫酸铜品体受热可以逐步失去结品水,温 度升高还町以分解生成铜的氧化物。观取25.0g CuSO4・5H2O品体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:
度升高还町以分解生成铜的氧化物。观取25.0g CuSO4・5H2O品体均匀受热,缓慢升温至1200℃并恒温1小时,实验测得固体残留率(剩余固体的质量/原始固体质量)与温度的关系如下图所示:

在110℃时所得固体的成分为?;在1200℃并恒温1小时,反应所 得气态产物除去水后,物质的量为?。(填字母)
得气态产物除去水后,物质的量为?。(填字母)
A.0 mol
B.0.1mol
C.0.125mol
D.大于0.125mol
参考答案:(12分,每空2分)
(1)①3Fe2O3+CO
CO太多导致Fe3O4还原为铁,CO太少Fe2O3没有全部转化成Fe3O4
②CaCl2+SiO2+H2O
(2)将步骤4中的坩埚再加热一定时间,放入干燥器中冷却至室温后称越。重复本操作,直至两次称量结果不变;
(3)CuSO4・3H2O,D
本题解析:略
本题难度:简单
3、选择题 下面有关晶体的叙述中,正确的是(?)
A.分子晶体中一定存在共价键
B.第ⅦA族氢化物随相对分子质量增加,熔沸点逐渐升高,HF沸点最低
C.离子晶体在熔化时,离子键被破坏,而分子晶体熔化时,化学键不被破坏
D.熔融状态下导电的晶体一定是金属晶体
参考答案:C
本题解析:稀有气体原子的最外层电子已经达到稳定结构,所以稀有气体形成的分子中没有化学键,A不正确。氟化氢中存在氢键,其沸点最高,B不正确。离子晶体是靠离子键形成的,分子晶体是通过分子间作用力形成,所以选项C正确。D中也可以是离子晶体,不正确。答案选C。
本题难度:一般
4、选择题 下列性质适合于离子晶体的是
A.熔点1070 ℃,易溶于水,水溶液能导电
B.熔点10.31 ℃,液态不导电,水溶液能导电
C.能溶于CS2,熔点112.8 ℃,沸点444.6 ℃
D.熔点97.81 ℃,质软,导电,密度0.97 g・cm-3
参考答案:A
本题解析:A中物质熔点1070 ℃,较高,易溶于水,水溶液能导电,是离子晶体的性质,故A是离子晶体。B、C中物质熔点较低,液态不导电,能溶于CS2,不是离子晶体的性质,故B、C不是离子晶体。D中物质导电,不是离子晶体的性质,故D不是离子晶体。
本题难度:简单
5、选择题 铁有δ、γ、α三种同素异形体,如下图所示,三种晶体在不同温度下能发生转化。下列说法不正确的是( )

A.将铁加热到1500°C分别急速冷却和缓慢冷却,得到的晶体类型相同
B.α-Fe晶体中与每个铁原子等距离且最近的铁原子有6个
C.若δ-Fe晶胞边长为a cm,α-Fe晶胞边长为b cm,则两种晶体密度比为2b3:a3
D.δ-Fe晶体中与每个铁原子等距离且最近的铁原子有8个
参考答案:A
本题解析:根据已知信息可知,将铁加热到1500°C分别急速冷却和缓慢冷却,得到的晶体分别是α-铁和δ-铁,类型不相同,选项A不正确。根据晶胞的结构特点可知,选项B正确;δ-Fe晶胞中含有2个铁原子,α-Fe晶胞中含有1个碳原子,所以两种晶体密度比为2b3:a3,选项C正确;题意根据晶胞可知,选项D正确,答案选A。
点评:该题是高考中的常见题型和考点,属于中等难度试题的考查,试题综合性强,侧重对学生能力的培养和训练,有利于培养学生的逻辑推理能力、自学能力和知识的迁移能力,提高学生灵活运用基础知识解决实际问题的能力。
本题难度:简单