1、简答题 乙醇是生活中常见的有机物,能进行如图所示的多种反应,且A、C都是有机物.则:
(1)乙醇分子中官能团的名称是?;
(2)写出下列反应的化学方程式:
反应①:?;
反应②:?;
反应③:?;
(3)比较反应①与钠和水反应的现象有什么相同和不同??;
(4)乙醇是一种重要的燃料,其优点是?(填字母).
①燃烧时发生氧化反应?②充分燃烧的产物不污染环境
③乙醇是一种可再生能源?④燃烧时放出大量热能
A.①②③B.①②④C.①③④D.②③④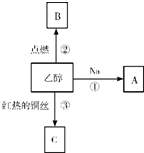
参考答案:(1)醇中含有羟基官能团,故答案为:羟基;
(2)①乙醇能和金属钠反应置换氢气,即2CH3CH2OH+2Na→2CH3CH2ONa+H2↑,故答案为:2CH3CH2OH+2Na→2CH3CH2ONa+H2↑;
②乙醇具有可燃性,燃烧方程式为:CH3CH2OH+3O2点燃
本题解析:
本题难度:一般
2、选择题 下列化学用语表示正确的是?
A.镓、锑的元素符号分别为Ge、Sb
B.三氟化氮的电子式:
C.次氯酸的结构式:H-O-Cl
D.熔融状态下硫酸氢钾的电离方程式:KHSO4 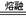 K++H++SO42-
K++H++SO42-
参考答案:C
本题解析:A 错误,镓的元素符号分别为Ga
B 错误,三氟化氮的电子式中,F原子周围也要画出8个黑点
C 正确。
D 错误,KHSO4 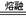 K++H SO4-
K++H SO4-
本题难度:一般
3、选择题 工业制ClO2的化学反应:2NaClO3+SO2+H2SO4=2ClO2+2NaHSO4,下列说法正确的是( )
A.NaClO3在反应中化合价降低,失去电子
B.SO2在反应中发生还原反应
C.1mol氧化剂在反应中得到电子数目为NA
D.H2SO4在反应中作氧化剂
参考答案:A.Cl元素化合价降低,被还原,NaClO3在反应中得电子,故A错误;
B.S元素化合价升高,被氧化,SO2在反应中发生氧化反应,故B错误;
C.由方程式可知,Cl元素化合价降低1价,则1mol氧化剂在反应中得到电子数目为NA,故C正确;
D.H2SO4中各元素的化合价都没有变化,在反应中起到酸性的作用,故D错误.
故选C.
本题解析:
本题难度:简单
4、填空题 过氧化氢(H2O2,O的化合价为-1价)俗称双氧水,医疗上利用它有杀菌消毒作用来清洗伤口。研究下列涉及H2O2的反应,完成下列各题:
A.Ag2O+ H2O2=2Ag+O2 ↑+ H2O
B.3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O
(1)写出一个H2O2既体现氧化性又体现还原性的化学反应方程式?。
(2)将下列物质:H2O2、K2SO4、MnSO4、H2SO4、KMnO4、O2的化学式分别填在空白处组成一个不需配平的化学方程式:?+ ?+______? →?+ ?+ ?+ H2O
①该反应中的还原剂是?。
②该反应中,发生还原反应的元素是?。
(3)氧化性:KMnO4_____K2CrO4(填“>”或“<”)。
参考答案:(1)2H2O2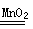 2H2O + O2↑ (2)H2O2+KMnO4+H2SO4→MnSO4+O2+K2SO4+ H2O
2H2O + O2↑ (2)H2O2+KMnO4+H2SO4→MnSO4+O2+K2SO4+ H2O
①H2O2?②Mn?(3)>
本题解析:(1)H2O2既体现氧化性又体现还原性,这说明该反应一定是双氧水的分解反应,反应的化学方程式为2H2O2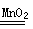 2H2O + O2↑。
2H2O + O2↑。
(2)高锰酸钾具有强氧化性,其氧化性强于双氧水的,所以高锰酸钾能把双氧水氧化生成氧气,而高锰酸钾的还原产物是硫酸锰,因此该反应的方程式可以表示为H2O2+KMnO4+H2SO4→MnSO4+O2+K2SO4+ H2O。
①双氧水中氧元素的化合价从-1价升高到0价,被氧化,因此双氧水是还原剂。
②高锰酸钾中Mn元素的化合价从+7价降低到+2价,得到电子,被还原,所以被还原的元素是Mn。
(3)在反应3H2O2+Cr2(SO4)3+10KOH=2K2CrO4+3K2SO4+8H2O中,双氧水是氧化剂,K2CrO4是氧化产物,则根据氧化剂的氧化性强于氧化产物的可知,氧化性是双氧水强于K2CrO4;在反应H2O2+KMnO4+H2SO4→MnSO4+O2+K2SO4+ H2O中,高锰酸钾是氧化剂,其氧化性强于双氧水的,所以高锰酸钾的氧化性强于K2CrO4。
本题难度:一般
5、选择题 下列变化属于氧化还原反应的是( )
A.Na2CO3+2HCl=2NaCl+H2O+CO2↑
B.CaO+H2O=Ca(OH)2
C.Fe+CuSO4=FeSO4+Cu
D.Al2O3+6HCl=2AlCl3+3H2O
参考答案:C
本题解析:
本题难度:简单