1、填空题 下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1) 在化合物YZ2中Y的化合价为________;Y2-与Na+的半径大小为_______________;
(2) R原子的电子轨道排布图为
____________________________________________________________________________;
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是______________________;X与Y的第一电离能:X___Y(填“<”、“>”或“=”),其理由是__________________________________。
(4)有一种酸HX3的酸性与醋酸相近,HX3溶液与NaOH溶液反应的离子方程式为_________
__________________________________。
参考答案:(9分) (1)+2价; O2->Na+或Na+<O2-?(2) 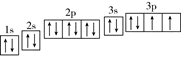
(3)F>O>N; >; N原子的2p轨道电子数为半充满状态,较稳定
(4)HN3+OH-===N+H2O【(2)、(4)2分,其余每空1分】
本题解析:(1)根据元素在周期表中的位置可知,X、Y、Z是第二周期元素,R是第三周期元素,W四第四周期元素,J是第五周期元素。其中X是N,Y是O,Z是F,W是Cl,J是Kr。所以在OF2中氧元素的化合价是+2价。氧离子与钠离子的核外电子排布相同,所以离子半径是O2->Na+。
(2)根据构造原理可知,S原子的电子轨道排布图为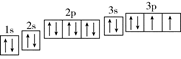 。
。
(3)非金属性越强,电负性越大,则电负性大小顺序是)F>O>N。由于N原子的2p轨道电子数为半充满状态,较稳定,所以氮元素的第一电离能大于氧元素的第一电离能。
(4)酸HX3的酸性与醋酸相近,这说明HN3是一元弱酸,因此该溶液与NaOH溶液反应的离子方程式为HN3+OH-===N+H2O。
点评:该题是中等难度的试题,试题基础性强,难易适中,贴近高考。注重对学生能力的考查与训练。本题主要是元素“位、构、性”三者关系的综合考查,比较全面考查学生有关元素推断知识和灵活运用知识的能力。该题以“周期表中元素的推断”为载体,考查学生对元素周期表的熟悉程度及其对表中各元素性质和相应原子结构的周期性递变规律的认识和掌握程度。考查了学生对物质结构与性质关系以及运用元素周期律解决具体化学问题的能力。
本题难度:一般
2、选择题 已知钡的活动性介于钠和钾之间,下列叙述正确的是(?)
A.钡与水反应不如钠与水反应剧烈
B.钡可以从KCl溶液中置换出钾
C.氧化性:K+>Ba2+>Na+
D.碱性:KOH>Ba(OH)2>NaOH
参考答案:D
本题解析:A中由于钡的活动性比钠强,所以钡与水反应比钠与水反应更剧烈,故A错;B中钡的活动性不如钾且先与水发生反应,故不能置换出钾,故B错;C中由于金属性:K>Ba>Na,故氧化性为Na+>Ba2+>K+,故C错;D中元素的金属性越强,其对应的最高价氧化物的水化物的碱性越强,故KOH>Ba(OH)2>NaOH,D说法正确。
本题难度:一般
3、选择题 有几种元素的粒子的结构示意图如下图所示,其中:

(1)某中性粒子一般不和其他元素的原子发生反应,这种粒子的符号______。
(2)某粒子的盐溶液,加入AgNO3溶液时会出现白色沉淀,这种粒子的符号是______。
(3)某粒子氧化性很弱,但得到1个电子后还原性很强,这种粒子的符号是______。
(4)某粒子具有很强的还原性,且这种粒子失去了2个电子即变为原子,这种粒子的符号是______。
参考答案:(1)Ar? (2)Cl-?(3)K+?(4)S2-
本题解析:各粒子核外电子数均为18。(1)中的粒子呈电中性即核电荷数为18,为Ar原子;(2)中的粒子与Ag+作用生成白色沉淀,为Cl-;(3)中粒子得一个电子变成中性,则该粒子带一个单位正电荷:K+;(4)中粒子失去2个电子即变为原子,则该粒子带两个单位负电荷:S2-。
本题难度:简单
4、选择题 某元素负一价阴离子的核外有10个电子,该元素在周期表中的位置是
A.二周期IA族
B.三周期ⅦA族
C.二周期ⅦA族
D.三周期IA族
参考答案:C
本题解析:一价阴离子核外有10个电子说明该元素原子电子数为9,该元素为F。
点评:周期数等于电子层数,主族序数等于核外电子数。
本题难度:一般
5、填空题 (10分)现有四种短周期元素X、Y、Z、W,其中:①X、W原子的电子层数与最外层电子数之比分别为3:1和1:3②Y元素的某原子核内无中子③Z元素原子的最外层电子数是其内层电子总数的2倍。回答下列问题:
(1)X元素在周期表中的位置是。
(2)化合物X2W2的电子式是。
(3)向含1molNa2SiO3的溶液中缓慢通入2mol的ZO2,反应的离子方程式是。
(4)由Y、Z、W元素中的两种或三种可以组成多种分子,其中含有18个电子的分子是(只需填一个化学式)。
(5)用KMnO4溶液可以通过滴定来测定Y2Z2W4溶液的物质的量浓度。向2500mL的Y2Z2W4溶液中加入500mL050mol/L酸性KMnO4溶液恰好完全反应,得到ZO2和Mn2+,则此种Y2Z2W4溶液的物 质的量浓度是mol/L。
质的量浓度是mol/L。
参考答案:(1)第三周期、第ⅠA族(2)
(3)2CO2+2 H2O+SiO32―==2HCO3―+H2SiO3↓(4)H2O2(CH4O、C2H6)(5)025
H2O+SiO32―==2HCO3―+H2SiO3↓(4)H2O2(CH4O、C2H6)(5)025
本题解析:略
本题难度:简单