| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点总结《水的电离平衡》高频考点特训(2020年练习版)(三)
F.胶头滴管 G.玻璃棒 ②滴定操作中,左手__________,右手__________,眼睛________________________。 ③Ba(OH)2溶液的物质的量浓度是________________________________________; ④过滤所得浊液的目的是_________________________________________________; ⑤此空气样品中含CO2的体积分数为______________________________________。 2、选择题 室温时,向20 mL 0.1 mol・L-1NH4HSO4溶液中滴加0.1 mol・L-1NaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示(假设滴加过程中无气体产生,且混合溶液的体积可看成混合前两溶液的体积之和),下列说法不正确的是: |
3、选择题 水的电离平衡曲线如图所示.下列说法正确的是( )
A.图中对应点的温度关系为:a>b
B.水的电离常数KW数值大小关系为:b>d
C.温度不变,加入少量NaOH可使溶液从c点变到a点
D.在b点对应温度下,将pH=2的H2SO4与pH=10的NaOH溶液等体积混合后,溶液显酸性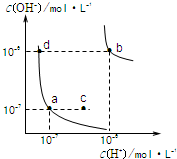
4、选择题 在10mL pH=12的NaOH溶液中,加入10mL某酸,再滴入紫色石蕊试液,溶液显红色,这种酸可能是
A 0.01mol/L CH3COOH B 0.01mol/L HNO3
C pH=2的H2SO4溶液 D pH=2的CH3COOH溶液
5、选择题 下列图示与对应的叙述相符的是( )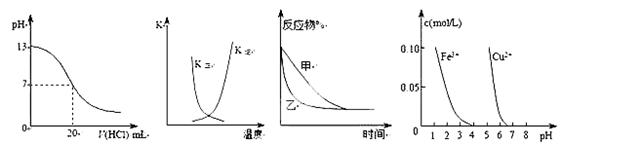
① ② ③ ④
A.图①表示25℃时,用0.1 mol・L-1盐酸滴定20 mL 0.1 mol・L-1NaOH溶液,溶液的pH随加入酸体积的变化
B.图②中曲线表示反应2A(g) + B(g) 2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
2C(g) ΔH > 0,正、逆反应的平衡常数K随温度的变化
C.图③表示压强对可逆反应2A(g)+2B(g)  3C(g)+D(s)的影响,乙的压强比甲的压强大
3C(g)+D(s)的影响,乙的压强比甲的压强大
D.据图④若除去CuSO4溶液中的Fe3+可向溶液中加入适量CuO至pH在4左右。
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点总结《弱电解质电.. | |