1、选择题 常温下,下列溶液可用铝制容器盛装的是?
A.稀盐酸
B.稀硫酸
C.浓硝酸
D.氢氧化钠溶液
参考答案:C
本题解析:考点:铝的化学性质.
分析:根据铝的性质进行解答,能持续发生反应则不能用铝制容器来盛放.
解:
A、盐酸是弱氧化性的酸,能和铝反应生成氢气,不能用铝制品容器盛放,故A错误;
B、稀硫酸有弱氧化性,能和铝反应生成氢气,不能用铝制品容器盛放,故B错误;
C、铝在浓硝酸中发生钝化现象,故铝制品容器可以盛放浓硝酸,故C正确.
D、氢氧化钠溶液能和铝反应,不能用铝制品容器盛放,故D错误;
故选C
本题难度:困难
2、选择题 已知甲、乙、丙、X是4种中学化学中常见的物质,其转化关系符合下图。则甲和X(要求甲和X互换后也能符合要求)是
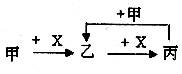
①Na2CO3溶液和稀盐酸;②Cl2和Fe;③C和O2;④SO2和NaOH溶液;⑤AlCl3溶液和NaOH溶液
A.①②③④均可以
B.②③④⑤均可以
C.①②③⑤均可以
D.①③④⑤均可以
参考答案:D
本题解析:试题分析:①Na2CO3+HCl=NaHCO3+NaCl,NaHCO3+HCl=NaCl+H2O+CO2↑Na2CO3+H2O+CO2=2NaHCO3.正确
②3Cl2+2Fe=2FeCl3后面反应无法继续进行。错误。
③2C+O2=2CO,2CO+O2=2CO2,CO2+C=2CO.正确
④SO2+NaOH=NaHSO3NaHSO3+NaOH=Na2SO3+H2ONa2SO3+H2O+SO2=2NaHSO3
⑤AlCl3+3NaOH=Al(OH)3↓+3NaCl,Al(OH)3+NaOH=NaAlO2+2H2O.3NaAlO2+AlCl3+6H2O=4Al(OH)3↓+3NaCl,正确。所以符合要求的为①③④⑤。选项是D。
考点:考查元素及化合物反应时量的多少对反应的影响等相关知识。
本题难度:简单
3、选择题 纯铁的实际应用范围有限,人们大量使用的是铁的合金。钢铁是铁和碳的合金的总称,其强度高、价格便宜、应用广泛。在以下关于不锈钢和普通钢的认识中,不正确的是
A.它们的组成元素是相同的
B.耐腐蚀的性能不一样
C.它们都属于钢,因此物理性能一样
D.构成普通钢和不锈钢的主要元素都是铁,因此它们的化学性质完全相同
参考答案:CD
本题解析:试题分析:A选项中,不锈钢和普通钢都是含有铁元素和碳元素,只是其中的比例不同;B选项,不锈钢比普通钢更耐腐蚀;C选项中,不锈钢和普通钢中碳元素含量不同,使其熔点、硬度等各个物理性质也不同;D选项中,两者所含碳元素不同,不锈钢更耐腐蚀,所以其更加难以发生相应的化学变化
考点:不锈钢与普通钢的区别
点评:本题考查的是不锈钢与普通钢的相关知识,两者的区别与联系
本题难度:简单
4、选择题 下列有关物质性质、应用的说法中正确的是
A.SiO2既能溶于NaOH溶液又能溶于HF,说明SiO2是两性氧化物
B.浓硫酸能干燥SO2等气体,说明浓硫酸具有吸水性
C.将铜片放入浓硫酸中,无明显现象,说明铜在冷的浓硫酸中发生钝化
D.自来水厂可用明矾对水进行消毒杀菌
参考答案:B
本题解析:试题分析:A、二氧化硅只能和HF反应,因此二氧化硅是酸性氧化物,A不正确;B、浓硫酸具有吸水性,可以干燥SO2气体,B正确;C、Fe或Al放入浓硫酸中,表面生成致密的氧化物,发生钝化,而铜在冷的浓硫酸中不反应,故C错误;D、明矾溶于水电离出的Al3+水解生成氢氧化铝胶体具有吸附悬浮杂质能起到净化水的作用,不能对水进行消毒杀菌,D不正确,答案选B。
考点:考查了浓硫酸的性质,明矾净水以及二氧化硅的性质等
本题难度:一般
5、选择题 加入下列物质不可能实现Fe2O3→Fe转化的是
A.H2
B.CO
C.Al
D.Cl2气
参考答案:D
本题解析:试题分析:实现Fe2O3→Fe转化,需要加入还原剂,其中A中 H2、B中CO、C中Al 都有还原性,而D中Cl2主要表现氧化性。
考点:考查氧化还原反应规律分析和常见还原剂和氧化剂
点评:熟悉氧化还原反应规律,熟悉常见还原剂和氧化剂的性质,属于简单题型
本题难度:简单