| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学知识点归纳《物质的量》高频试题强化练习(2020年最新版)(二)
参考答案:D 本题解析:略 本题难度:一般 2、选择题 设NA表示阿伏加德罗常数,下列叙述正确的是 参考答案:B 本题解析:A错,熔融的KHSO4的电离方程式为KHSO4==K++HSO4―;13.6g熔融的KHSO4的物质的量为0.1mol,13.6g熔融的KHSO4中含有0.1NA个阳离子;B正确;C错,二氧化氮气体可自发转化为四氧化二氮;D错,白磷为空心正四面体结构,31 g P4(正四面体结构)所含共价键数为6NA 本题难度:一般 3、选择题 设NA为阿伏加德罗常数的值,下列叙述正确的是 |
参考答案:C
本题解析:A、标准状况下苯不是气态,不能适用于气体摩尔体积,A错误;B、不能确定氯气所处的状态,因此不能计算氯气的物质的量,B错误;C、铜离子在溶液中水解,因此1L1mol・L-1氯化铜溶液中Cu2+的数目小于NA,C正确;D、0.1mol铁在0.1molCl2中充分燃烧,铁过量,氯气完全反应,转移的电子数为0.2NA,D错误,答案选C。
考点:考查阿伏伽德罗常数的计算与判断
本题难度:一般
4、选择题 下列溶液中,c (Cl-)最小的是
[? ]
A.20 mL 0.5 mol/L AlCl3溶液
B.30 mL 1 mol/L KCl溶液
C.7.5 mL 2 mol/L MgCl2溶液
D.10 mL 3 mol/L NaCl溶液
参考答案:B
本题解析:
本题难度:简单
5、填空题 (1)写出图1中序号①~④仪器的名称: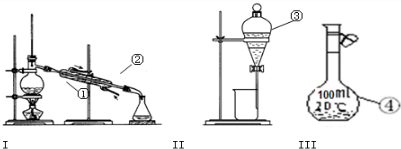
①______②______③______④______
(2)仪器①~④中,使用时必须检查是否漏水的有______.(填仪器序号)
(3)分离碘水中的碘应先选择装置______(填装置序号)进行操作A,再选装置进行______操作(填操作名称).进行操作A时,需在碘水中加一试剂,在选择试剂时,下列性质你认为哪些性质是必需的:______(填序号).
①常温下为液态②I2在其中溶解程度大③与水互溶程度小④密度要比水大
(4)图2是某学校实验室从化学试剂商店买回的浓硫酸试剂标签上的部分内容.现用该浓硫酸配制480mL1mol/L的稀硫酸.
可供选用的仪器有:①胶头滴管;②烧瓶;③烧杯;④药匙;⑤量筒;⑥托盘天平.
请回答下列问题:
a.配制稀硫酸时,还缺少的仪器有______、______(写仪器名称);
b.经计算,配制480mL1mol/L的稀硫酸需要用量筒量取上述浓硫酸的体积为______mL,量取硫酸时应选用______mL规格的量筒;
A.10mLB.50mLC.100mLD.200mL
c.对所配制的稀硫酸进行测定,发现其浓度大于1mol/L,配制过程中下列各项操作可能引起该误差的原因有______.
A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸
B.定容时,俯视容量瓶刻度线进行定容
C.将稀释后的稀硫酸立即转入容量瓶后,紧接着就进行以后的实验操作
D.转移溶液时,不慎有少量溶液洒到容量瓶外面
E.容量瓶用蒸馏水洗涤后未干燥,含有少量蒸馏水
F.定容后,把容量瓶倒置摇匀后发现液面低于刻度线,便补充几滴水至刻度处.
参考答案:(1)由图中仪器的结构可知,①为蒸馏烧瓶、②是冷凝管、③是分液漏斗、④是100mL容量瓶,
故答案为:蒸馏烧瓶;冷凝管;分液漏斗;100mL容量瓶;
(2)因分液漏斗和100mL容量瓶在使用前要检查是否漏水,蒸馏烧瓶、冷凝管不需要检查是否漏水,
故答案为:③④;
(3)碘在四氯化碳中的溶解度较在水中大,并且四氯化碳和水互不相溶,可用萃取的方法分离,接着可用分液方法将两层液体分开,故分离碘水中的碘应选择装置II;
四氯化碳易挥发,可用蒸馏的方法分馏得到四氯化碳,分离碘与四氯化碳;
碘在萃取剂中的溶解度大于在水中的溶解度,萃取剂和水不互溶,且萃取剂和碘不反应,故选②③,
故答案为:II;蒸馏;②③;
(4)a、没有480mL容量瓶,选择500mL容量瓶.
操作步骤有计算、量取、稀释、移液、洗涤移液、定容、摇匀等操作,用量筒量取(用到胶头滴管)浓硫酸,在烧杯中稀释,用玻璃棒搅拌,冷却后转移到500mL容量瓶中,并用玻璃棒引流,洗涤2-3次,将洗涤液转移到容量瓶中,加水至液面距离刻度线1~2cm时,改用胶头滴管滴加,最后定容颠倒摇匀.
由提供的仪器可知还需要仪器有:500mL容量瓶、玻璃棒;
故答案为:500mL容量瓶、玻璃棒;
b、浓H2SO4的物质的量浓度c=1000×1.84×98%98mol/L=18.4mol/L.根据稀释定律,稀释前后溶质的物质的量不变,来计算浓硫酸的体积,设浓硫酸的体积为xmL,
所以xmL×18.4mol/L=500mL×1mol/L,解得:x≈27.2,
所需浓硫酸的体积为27.2mL.量筒规格越接近所需浓硫酸体积误差越小,所以选择50mL量筒,
故答案为:27.2;B;
c、A.用量筒量取浓硫酸时,仰视刻度线取浓硫酸,量取浓硫酸的体积增大,所配溶液浓度偏高,故A符合;
B.定容时,俯视容量瓶刻度线,液面在刻度线以下,导致所配溶液体积减小,所配溶液浓度偏高,故B符合;
C.溶液有热胀冷缩的性质,浓硫酸稀释,放出大量的热,溶解后未恢复室温立即转移到容量瓶中定容,导致所配溶液体积减小,所配溶液浓度偏高,故C符合;
D.转移溶液时,不慎有少量溶液洒到容量瓶外面,移入容量瓶中的溶质硫酸的物质的量减小,所配溶液浓度偏低,故D不符合;
E.最后需要加水定容,容量瓶不干燥,含有少量蒸馏水,对溶液浓度无影响,故E不符合;
F.摇匀后液面下降,一部分溶液留在瓶塞与瓶口之间,再加蒸馏水至刻度线,导致溶液体积偏大,所以溶液浓度偏低,故F不符合;
故选:ABC.
本题解析:
本题难度:一般
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高考化学必考知识点《新型材料》.. | |