| 高考省级导航 | |
|
|
| 高考省级导航 | |
|
|
|
高考化学必考知识点《碳族元素》高频试题巩固(2020年最新版)(二)
(5)实验结束后,分液漏斗中的NaOH溶液已经全部加入烧瓶,量筒中收集到水的体积为a L,若当时的实验条件为标准状况,则样品中的AlN的质量分数为___________(AlN的式量为41),这一测定结果比实际值偏高,你认为可能的原因是__________________________。 (6)有人建议改用图Ⅱ装置进行同样实验,欲通过测定烧杯中硫酸的增重来确定样品中AlN的质量分数。你认为这样的改进是否可行?________________(填“可行”或“不可行”)。理由是________________________。 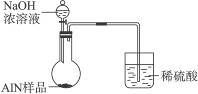 图Ⅱ 参考答案:(1)c、a、b、d 本题解析:根据题意,该实验为一定量实验,因此按装置图连接装置后,首先要检验装置的气密性,其方法是:关闭分液漏斗活塞,在量筒中加适量水浸没导管口,使装置密闭,再微热圆底烧瓶,使装置内气体体积膨胀,若量筒中产生气泡,恢复到室温时导管中形成一段水柱,则气密性良好。由于NH3极易溶于水,因此,用NH3排水时,必须用试剂X将NH3与H2O隔开,广口瓶中的试剂X必须具备两个条件:①不与NH3、H2O反应,不溶解NH3,不溶于水;②密度比H2O小。所以试剂X可选用植物油。实验结束后,若烧瓶中还有固体,则样品中含有的杂质是碳,因为AlN和Al2O3能与NaOH溶液反应,溶解于NaOH溶液中。 本题难度:简单 5、选择题 下列物质的用途错误的是 参考答案:B 本题解析:A正确,硅能够将太阳能转化为电能的材料;B错,常温下可用铁罐或铝罐装运浓硝酸,发生钝化;C正确,胃酸的主要成分为HCL,小苏打和氢氧化铝的碱弱较弱可以作为胃药的成分;D正确,工厂废气中的SO2可回收生产硫酸既可以消除对环境的影响,又可废物利用; 本题难度:一般 |
| 【大 中 小】【打印】 【繁体】 【关闭】 【返回顶部】 | |
| 下一篇:高中化学知识点大全《弱电解质电.. | |