1、选择题 下列有关硅的叙述中,正确的是
A.硅只有在高温下才能跟氢气起化合反应。
B.硅是构成矿物和岩石的主要元素,硅在地壳中的含量在所有的元素中居第一位。
C.硅的化学性质不活泼,在常温下不与任何物质反应。
D.硅在电子工业中,是最重要的半导体材料。
参考答案:A、D
本题解析:A正确?因为硅的化学性质稳定,常温下除了少数物质外,它不易与其他物质如氢气、氧气、氯气等反应。B不正确?氧元素在地壳中的含量居第一位。C不正确?硅的化学性质不活泼,但可与F2、HF和强碱等反应。D 正确?硅是常温下化学性质稳定的半导体材料,广泛应用于计算机技术领域。
本题难度:简单
2、选择题 NaOH、KOH等碱性溶液可以贮存在下列哪种试剂瓶中
A.具有橡胶塞的细口瓶
B.具有玻璃塞的广口瓶
C.带滴管的滴瓶
D.具有玻璃塞的细口瓶
参考答案:A
本题解析:固体药品一般放在广口瓶中,液体试剂一般放在细口瓶中。NaOH、KOH等碱性物质的溶液容易与玻璃中的成分SiO2发生反应:2OH -+SiO2= SiO32-+H2O。产生的Na2SiO3、K2SiO3有粘性,容易将玻璃瓶与玻璃塞黏在一起。所以NaOH、KOH等碱性溶液可以贮存在具有橡胶塞的细口瓶中。选项为:A。
本题难度:一般
3、选择题 下列关于硅及其化合物的说法正确的是
A.SiO2是酸性氧化物,硅酸的酸酐, 但是它不与水、烧碱反应
但是它不与水、烧碱反应
B.硅元素是自然界构成岩石、矿物的主要成分,其单质是半导体,不与任何酸碱反应
C.硅酸钠溶液加入盐酸产生白色浑浊,再加入足量的烧碱,溶液恢复澄清
D.硅酸钠溶液中 缓慢通入足量二氧化碳,先产生浑浊后恢复澄清
缓慢通入足量二氧化碳,先产生浑浊后恢复澄清
参考答案:C
本题解析:略
本题难度:一般
4、计算题 有一铅锡合金质量为100g,完全氧化后得到氧化物的混合物质量为116g,求合金中铅、锡的质量分数各为多少?
参考答案:合金中铅、锡分别占56.8%、43.2%
本题解析:解法一:
分析:设100g铅锡合金中含锡xg,则含铅(100-x)g。①Sn氧化后的稳定产物是SnO2(+4价氧化物稳定),Sn的相对原子质量为

Pb氧化后的稳定产物是PbO(+2价氧化物稳定), Pb的相对原子质量为207,PbO的式量为223,(100-x)g Pb氧化生成的PbO质量必
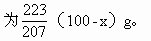
因为SnO2与PbO质量共为116g,故可列一元一次方程,解方程求出Sn、Pb质量。
[解] 设100g锡铅合金中含锡xg,含铅为(100-x)g。
根据化学式所表示的元素质量分数及题意,列代数方程式:
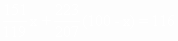
解得x=43.2(g)
100-x=100-43.2=56.8(g)

答:合金中锡、铅质量分数分别为43.2%、56.8%
解法二:
分析:此题利用物质的量计算也很方便。设100g合金中含xg,含铅为(100-x)g
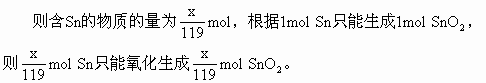

将SnO2与PbO由物质的量换算成质量,质量和为116g。
解:设100g锡铅合金中含锡为xg,含铅为(100-x)g
Sn的物质的量=SnO2的物质的量

Pb的物质的量=PbO的物质的量

SnO2与PbO质量和为116g
解得 x=43.2(g)
(锡的质量)
100-x=56.8(g)
(铅的质量)
本题难度:简单
5、选择题 氯气用途十分广泛,可用于生产半导体材料硅,其生产的流程如下,下列说法不正确的是(?)

A.①③是置换反应,②是化合反应
B.高温下,焦炭与氢气的还原性均强于硅的
C.任一反应中,每消耗或生成28 g硅,均转移4 mol电子
D.高温下将石英砂、焦炭、氯气、氢气按一定比例混合可得高纯硅
参考答案:D
本题解析:在高温下将石英砂、焦炭、氯气、氢气按一定比例混合,则石英砂与焦炭反应,氯气与氢气反应,就不再按照题干的流程进行,不会得到高纯硅。
本题难度:一般