1、填空题 (10分)铬是人体必需元素,如含量不足会影响糖类和脂类的代谢,过高则会引起急性中毒。有关含铬化合物的相互转化关系如下

回答下列问题:
(1)上述反应中需用氧化剂的是?(填编号)。
(2)工业上处理含Cr2O72-的废水时,一般将剧毒的Cr2O72-转化为Cr3+,以碳为阴极,铁作阳极,电解处理含NaCl、Cr2O72-的酸性废水。写出电极反应和溶液中进行的反应的离子方程式:
阳极 ?阴极
溶液中
(3)反应⑤是可逆反应,在Na2CrO4溶液中加入稀硫酸,溶液由黄色逐渐变成橙色,写出该反应的离子方程式??。
参考答案:(1)? 4? 8?
(2 )2H++2e-=H2↑? Fe-2e-=Fe2+? Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O
(3)2CrO42-+2H+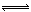 Cr2O72-+H2O
Cr2O72-+H2O
本题解析:本题考查了氧化还原反应、离子反应及电化学的相关知识;
(1)根据铬的化合价可知,化合价升高的反应必然是由外界提供氧化剂
(2)阳极铁要失电子 Fe-2e-=Fe2+,再根据离子的放电顺序知道H+在阴极放电2H++2e-=H2↑ ;
Fe2+的产生提供了还原剂,被Cr2O72-氧化:Cr2O72- + 6Fe2+ + 14H+ = 2Cr3+ +6Fe3++7H2O
(3)主要考查离子方程式的书写与配平
本题难度:一般
2、选择题 根据下图,下列判断中正确的是(? )
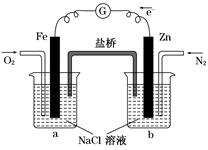
A.烧杯a中的溶液pH升高
B.烧杯b中发生氧化反应
C.烧杯a中发生的反应为2H++2e-=H2
D.烧杯b中发生的反应为2Cl--2e-=Cl2
参考答案:AB
本题解析:由图知,烧杯b中的Zn棒失去电子,发生氧化反应,电子转移到Fe棒上,烧杯a中通入的氧气在Fe棒表面得电子生成氢氧根离子,使a中溶液的pH升高。所以正确的为A、B。
本题难度:一般
3、选择题 实验发现,298 K时,在FeCl3酸性溶液中加入少量锌粒后,Fe3+立即被还原成Fe2+。某化学兴趣小组根据该实验事实设计了如图所示的原电池装置。下列有关说法中正确的是? ( )
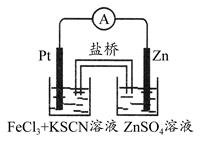
A.该原电池的正极反应是:Zn-2e-=Zn2+
B.左烧杯中溶液的红色逐渐褪去
C.该电池铂电极上有气泡出现
D.该电池总反应为:3Zn+2Fe3+=2Fe+3Zn2+
参考答案:B
本题解析:正极是得电子的反应,A错误;左烧杯中的电极反应式为Fe3++e-=Fe2+,B正确、C错误;因为在金属活动性顺序中铁排在H的前面,在酸性溶液中不会生成Fe,D错误。
本题难度:一般
4、选择题 一种新燃料电池,一极通入空气,另一极通入丁烷气体;电解质是掺杂氧化钇(Y2O3)的氧化锆(ZrO2)晶体,在熔融状态下能传导O2-。下列对该燃料说法正确的是
A.在熔融电解质中,O2-由负极移向正极
B.电池的总反应是:2C4H10 + 13O2 → 8CO2 + 10H2O
C.通入空气的一极是正极,电极反应为:O2 + 4e- 2H2O= 4OH-
D.通入丁烷的一极是正极,电极反应为:C4H10 + 26e- + 13O2 = 4CO2 + 5H2O
参考答案:B
本题解析:在原电池中较活泼的金属作负极,失去电子,发生氧化反应。电子经导线传递到正极上,所以溶液中的阳离子向正极移动,阴离子向负极移动。正极得到电子,发生还原反应。所以丁烷在负极通入,空气在正极通入,所以选项AD不正确。由于电解质是熔融的氧化物,所以正极反应式为O2 + 4e-= 2O2-,C不正确,所以正确的答案是B。
本题难度:一般
5、选择题 下列装置中,属于原电池的是? ( )
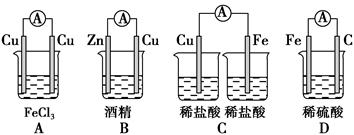
参考答案:D
本题解析:利用组成原电池的条件分析,A项两电极相同;B项酒精为非电解质;C项缺少盐桥;只有D项符合。
本题难度:一般