1、选择题 现需要物质的量浓度约为2 mol・L-1的NaOH溶液100 mL,下面的操作正确的是(? )
A.称取7.8 g Na2O2固体,放入250 mL烧杯中,用100 mL 量筒量取100 mL蒸馏水,加入烧杯中,同时不断搅拌至固体溶解
B.称取8 g NaOH固体,放入100 mL量筒中,边搅拌边慢慢加入蒸馏水,待固体完全溶解后用蒸馏水稀释至100 mL
C.称取8 g NaOH固体,放入100 mL容量瓶中,加入适量蒸馏水,振荡容量瓶使固体溶解,再加入水到刻度,盖好瓶塞,反复摇匀
D.用100 mL量筒量取40 mL 5 mol・L-1NaOH溶液,倒入250 mL烧杯中,再用另一量筒量取60 mL蒸馏水,不断搅拌下,慢慢倒入烧杯中
参考答案:D
本题解析:A不正确,因为过氧化钠要消耗水;B不正确,量筒不能稀释溶液;同样容量瓶也不能稀释溶液,C不正确,因此正确的答案选D。
本题难度:一般
2、选择题 在4℃时向100ml水中溶解了22.4LHCl气体(标准状况)后形成溶液。下列说法中正确的是
[? ]
A.该溶液物质的量浓度为10mol/L
B.该溶液物质的量浓度因溶液的密度未知而无法求得
C.该溶液中溶质的质量分数因溶液的密度未知而无法求得
D.所得溶液的体积为22.5L
参考答案:B
本题解析:
本题难度:一般
3、计算题 将6.5g锌放入足量的稀硫酸中充分反应,得到80mL密度为1.25g/mL的溶液。试计算所得溶液中硫酸锌的物质的量浓度和质量分数各是多少? 生成标况下氢气多少毫升?
参考答案:1.25mol/L;16.1%;2240 ml
本题解析:
本题难度:一般
4、选择题 用NA表示阿伏加德罗常数的值,下列说法中正确的是(?)。
A.将NA个HCl分子溶于500 mL水中得到2.0 mol・L-1的盐酸
B.在加热条件下,100 mL 18.4 mol・L-1的浓硫酸与足量金属铜反应得到的SO2的分子数为0.92NA
C.密闭容器中,1 mol SO2与0.5 mol O2充分反应,转移的电子数小于2NA
D.用惰性电极电解AgNO3溶液,产生11.2 L O2时,转移2 mol电子
参考答案:C
本题解析:500 mL是溶剂的体积,不是溶液的体积,A项错误;随着反应进行,浓硫酸逐渐变稀,稀到一定程度后不再与Cu反应,故实际得到的SO2的分子数小于0.92NA,B项错误;SO2与O2的反应为可逆反应,故转移的电子数小于2NA,C项正确;没有指明气体所处的状况是否为标准状况,无法确定转移的电子数,D项错误。
本题难度:一般
5、选择题 下列有关说法正确的是(?)
A.9.2 g NO2气体中含有分子数目为0.2NA
B.标准状况下,2.24 L SO3中含有氧原子数目为0.3NA
C.2 g 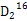 O中含中子、质子、电子数目均为NA
O中含中子、质子、电子数目均为NA
D.标准状况下2.24 L Cl2通入足量水中或NaOH溶液中,转移电子数目均为0.1NA
参考答案:C
本题解析:由于存在平衡:2NO2(g) N2O4(g),故含有的分子数<0.2NA,A错误;SO3在标准状况下是固体,B错误;2 g
N2O4(g),故含有的分子数<0.2NA,A错误;SO3在标准状况下是固体,B错误;2 g 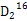 O 的物质的量为0.1 mol,而
O 的物质的量为0.1 mol,而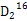 O中含中子(10)、含质子(10)、电子(10)数目均为0.1×10×NA=NA,C正确;标准状况下2.24 L Cl2即0.1 mol,由于Cl2与H2O的反应为可逆反应,故转移的电子数小于0.1NA,D错误。
O中含中子(10)、含质子(10)、电子(10)数目均为0.1×10×NA=NA,C正确;标准状况下2.24 L Cl2即0.1 mol,由于Cl2与H2O的反应为可逆反应,故转移的电子数小于0.1NA,D错误。
本题难度:一般