1、实验题 (15分)已知氨可以与灼热的氧化铜反应得到氮气和金属铜,用下图中的装置可以实现该反应。

回答下列问题:
(1)A中加入的物质是______________,发生反应的化学方程式是_____________。
(2)B中加入的物质是________,其作用是?。
(3)实验时在C中观察到的现象是__________________________,发生反应的化学方程式是____________________。
(4)实验时在D中观察到的现象是________,D中收集到的物质是________,检验该物质的方法和现象是________________________。
参考答案:(1)固体氯化铵和氢氧化钙、2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O
CaCl2+2NH3↑+2H2O
(2)碱石灰(或氧化钙)?除去氨气中的水蒸气
(3)黑色粉末逐渐变为红色?3CuO+2NH3 3Cu+N2+3H2O
3Cu+N2+3H2O
(4)出现无色液体?氨水
用红色石蕊试纸检验,试纸变蓝,说明有氨气存在,用无水硫酸铜粉末检验,无水硫酸铜变蓝,说明有水存在。
本题解析::C为氨气还原氧化铜的装置,A为制氨气的发生装置,B为干燥装置,水蒸气在D中冷凝,NH3溶于水形成氨水,E中收集N2。
(1)实验室加热氯化铵和氢氧化钙混合物制氨气,方程式为:
NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O。
CaCl2+2NH3↑+2H2O。
(2)B中固体为碱石灰或生石灰或固体氢氧化钠,作用是除去氨气中的水蒸气。
(3)C中现象为黑色固体变红,反应方程式为3CuO+2NH3 3Cu+N2+3H2O。
3Cu+N2+3H2O。
(4)水蒸气在D中冷凝,NH3溶于水形成氨水。可用红色石蕊试纸检验其中的NH3、用无水硫酸铜检验其中的H2O。
点评:本题综合考查NH3的制备和性质。
本题难度:一般
2、实验题 工业尾气中氮氧化物通常采用氨催化吸收法,其原理是NH3与NOx在催化剂作用下反应生成无毒的物质。某校活动小组同学采用以下装置和步骤模拟工业上氮氧化物的处理过程。
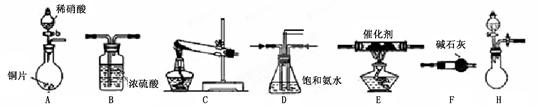
I.探究制取NH3的方法
(1)在上述装置中,H能快速、简便制取NH3,装置中需要添加的反应试剂为?。
(2)为探究更好的实验效果,活动小组同学采用上述C装置来制取氨气,在控制实验条件相同的情况下,获得下表中实验数据。
试剂组合序号
| 固体试剂
| NH3体积(mL)
|
a
| 6.0 g Ca(OH)2(过量)
| 5.4 g NH4Cl
| 1344
|
b
| 5.4g (NH4)2SO4
| 1364
|
c
| 6.0 g NaOH(过量)
| 5.4 g NH4Cl
| 1568
|
d
| 5.4g (NH4)2SO4
| 1559
|
e
| 6.0 g CaO(过量)
| 5.4 g NH4Cl
| 1753
|
f
| 5.4 g (NH4)2SO4
| 1792
|
?
分析表中数据,你认为哪种方案制取氨气的效果最好?(填序号),从该方案选择的原料分析制气效果好的可能原因是?。
II.模拟尾气处理
活动小组同学选用上述部分装置,按下列顺序连接成模拟尾气处理装置进行实验。
(1)请从上述装置中选择你认为合理的进行补充(所选装置不能重复)。
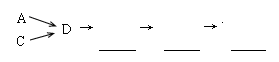
(2)A中反应的离子方程式为 ?。
(3)D装置的作用有:使气体混合均匀、调节气流速度、?。
(4)D装置中的液体还可换成?(填序号)。
a.H2O? b.CCl4? c.浓H2SO4? d.CuSO4溶液
(5)该小组同学所设计的模拟尾气处理装置中还存在一处明显的缺陷是?。
参考答案:I.(1)生石灰与浓氨水(或烧碱与浓氨水) (答化学式给分)(2分)?
(2)f?(2分)? (NH4)2SO4受热不分解,CaO又有吸水作用(合理答案均给分)(2分)
II.(1)F? E? B?(2分)
(2)3Cu + 2NO3-+8H+ ?3Cu2+ + 2NO↑ +4H2O (2分)
?3Cu2+ + 2NO↑ +4H2O (2分)
(3)防止氨气溶解(或防止倒吸)(2分)
(4)b(2分)
(5)未反应的NO无法处理,会污染环境 (2分)
本题解析:(1)依据装置分析制备氨气气体是利用液体通过分液漏斗滴入烧瓶中不加热进行的反应,实验目的是制取、干燥和收集氨气的装置,制备氨气先干燥再收集,氨气比空气轻,应用向下排气法收集;制备氨气可以利用浓氨水滴入氧化钙或固体氢氧化钠或碱石灰,溶解放热时一水合氨分解生成氨气;
(2)因为NH4Cl受热易分解,生成的部分NH3和HCl又重新结合成NH4Cl,而用NaOH或Ca(OH)2作反应物产生的水较多,吸收的NH3较多,由表中数据可以看出,f制NH3产率最高;?
II.(1)混合气体干燥后进入反应装置,然后用浓硫酸吸收没有反应的氨气。
(2)稀硝酸具有强氧化性,与铜发生氧化还原反应生成硝酸铜和NO等,反应的离子方程式为3Cu + 2NO3-+8H+ ?3Cu2+ + 2NO↑ +4H2O;
?3Cu2+ + 2NO↑ +4H2O;
(3)D装置使气体混合均匀、调节气流速度,另外,氨气难溶于饱和氨水,可防止倒吸;
(4)氨气可溶于硫酸铜溶液、水以及硫酸中,可产生倒吸,氨气为极性分子,不溶于非极性溶剂,可用CCl4代替饱和氨水;
(5)缺少尾气处理装置,过量的NO会污染空气。
本题难度:一般
3、计算题 氨在高温下进行催化氧化以制取NO不考虑NO与O2反应)时,其
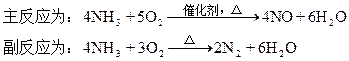
今在相同条件下将每1L氨混合10升空气后通入反应器。空气中O2和N2的体积百分含量分别以20%和80%计。上述反应完成后,测得混合气体中不含NH3,而O2与N2的物质的量之比为1∶10。试求参加主反应的氨占原料氨的体积百分含量(保留小数点后一位)。
参考答案:88.9%
本题解析:设1L氢中有x升与O2发生反应生成NO(即主反应),则参加副反应的氢为(1-x)L。
4NH3+5O2 4NO+6H2O
4NO+6H2O
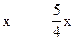
4NH3?+? 3O2? ?2N2+6H2O
?2N2+6H2O
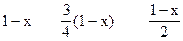

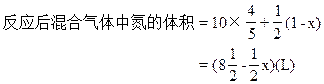
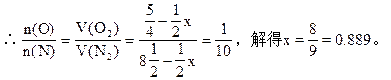
本题难度:一般
4、选择题 工业上用废铜屑作原料制备硝酸铜。为了节约原料和防止污染环境,宜采用的方法是(? )
A.Cu + HNO3(浓) → Cu(NO3)2
B.Cu +HNO3(稀) → Cu(NO3)2
C.Cu CuO
CuO  Cu(NO3)2
Cu(NO3)2
D.Cu  CuO
CuO 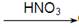 Cu(NO3)2
Cu(NO3)2
参考答案:C
本题解析:根据反应的方程式可知,选项ABD中都能产生大气污染物NO2、NO、SO2,C中没有污染物产生,且原料利用率高,所以正确的答案选C。
本题难度:一般
5、选择题 将3体积NO2气体依次通过三个分别装有①NaHCO3饱和溶液;②浓硫酸;③Na2O2的装置后,用排水法收集残留气体.此时气体的成分是(同温同压下测定)
A.1体积NO
B.2体积NO2和0.5体积O2
C.2体积O2
D.0.25体积O2
参考答案:D
本题解析:3体积的NO2气体与NaHCO3饱和 溶液反应,得到2体积CO2和1体积NO,通过盛有浓硫酸及Na2O2的装置后,生成的1体积O2、1体积NO与H2O反应后,剩余0.25体积O2.
本题难度:简单