1、选择题 Al-Ag2O电池是一种可用作水下动力的优良电源,其原理如图所示。该电池工作时总反应式为2Al+3Ag2O+2NaOH=2NaAlO2+6Ag+H2O,则下列说法错误的是? ( )。

A.工作时正极发生还原反应
B.当电极上生成1.08 g Ag时,电路中转移的电子为0.01 mol
C.Al电极的反应式为Al-3e-+4OH-=AlO2―+2H2O
D.工作时电解液中的Na+透过隔膜移向Al电极
参考答案:D
本题解析:正极发生还原反应,A对;1.08 g银的物质的量为0.01 mol,B对;由总反应式可知,Al电极是负极,电极反应式为Al-3e-+4OH-=AlO2―+2H2O,C对;阳离子应移向正极,D错。
本题难度:一般
2、选择题 镁--H2O2酸性电池采用海水作电解质(加入一定量酸),下列说法正确的是
[? ]
A.电池总反应为:Mg+H2O2+2H+=Mg2++2H2O
B.负极反应为:H2O2+2e-+2H+=2H2O
C.电池工作时,正极周围海水的pH减小
D.电池工作时,溶液中的H+向负极移动
参考答案:A
本题解析:
本题难度:一般
3、选择题 下列四种装置中电解质溶液均为稀H2SO4,不属于原电池的是(?)
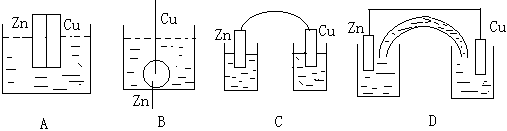
参考答案:C
本题解析:由于C装置没有形成闭合电路,所以C不是。
本题难度:简单
4、选择题 某实验兴趣小组用如图所示装置做完实验后,在读书卡片上记下了如下6条记录,其中合理的是


A.①②③
B.③④⑤
C.④⑤⑥
D.②③④
参考答案:B
本题解析:原电池中较活泼的金属是负极,失去电子,发生氧化反应。电子经导线传递到正极,所以溶液中的阳离子向正极移动,正极得到电子,发生还原反应。锌比铜活泼,所以锌是负极,铜是正极,溶液中的氢离子在正极得到电子,因此选项③④⑤正确,其余选项都是错误的,答案选B。
点评:该题是中等难度试题的考查,主要是检验学生对原电池原理的熟悉了解程度,意在巩固学生的基础知识,提高学生灵活运用基础知识解决实际问题的能力,难度不大,记住原电池原理,以及电子的得失守恒进行计算即可。
本题难度:简单
5、选择题 某同学利用家中废旧材料制作一个可使玩具扬
声器发出声音的电池,装置如右图所示。下列
说法正确的是 ( )
A.电流方向为:
铝质易拉罐→导线→扬声器→导线→炭棒
B.铝质易拉罐将逐渐被腐蚀
C.电池总反应为:4Al+3O2+6H2O=4Al(OH)2
D.炭棒上发生的主要反应为:2H++2e-=H2↑