|
���л�ѧ֪ʶ���ȫ����ѧʵ��Ļ�����������Ƶ���㹮�̣�2020��ģ��棩(��)
2021-02-18 07:27:15
�� �� �� ��
|
1��ѡ���� ʵ�� ���о���ѧ�Ļ�������ͼ����ʾ��ʵ�鷽����װ�û������ȫ��ȷ����
[? ]
A.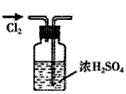
? ����Cl2
B.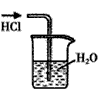
? ����HCl
C.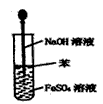
?��ȡFe(OH)2����
D.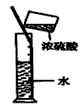
?ϡ��ŨH2SO4
�ο��𰸣�C
���������
�����Ѷȣ�һ��
2������� ʵ���⣺�����9�֣�ij�ռ���Ʒ�����������������õ����ʣ�Ϊ�˵ζ��䴿�ȣ��������µζ�������?
A����250 mL������ƿ������250 mL�ռ���Һ��
B���ü�ʽ�ζ�����ȡ25.00 mL�ռ���Һ����ƿ�в��μӼ��η�̪��ָʾ����?
C������ƽ��ȷ��ȡ�ռ���ƷW��g�����ձ���������ˮ�ܽ⣻
D�������ʵ���Ũ��Ϊcmol/L�ı�������Һװ����ʽ�ζ��ܡ�����Һ����¿�ʼ����ΪV1 mL��E.����ƿ�µ�һ�Ű�ֽ���ζ����һ������ɫ�պ���ʧ Ϊֹ������Ӻָ���ɫ�����¶���V2 mL��? Ϊֹ������Ӻָ���ɫ�����¶���V2 mL��?
| �ʹ�ʵ�����������գ�?
(1)��ȷ���������˳���ǣ�(�ñ����ĸ��д)??��
( 2)�۲�ζ�����Һ��ĸ߶�ʱӦע�⣺?��? 2)�۲�ζ�����Һ��ĸ߶�ʱӦע�⣺?��?
(3)E����IJ���������ƿ�µ�һ�Ű�ֽ��������?��
(4)D����IJ�����Һ��Ӧ���ڵ�?�����첿��Ӧ?��
(5)ijѧ��ʵ��ʱ����ƿ���ռ���Ʒϴ�ӣ�ʹ�ⶨ��Ũ��ƫ����ƫ��??
(6)���ռ���Ʒ���ȵļ���ʽΪ��?
�ο��𰸣�(1)��ȷ���������˳���ǣ�CABD(2)Ҫƽ�ӡ�(3)�������Թ۲졣(4)���ڵ���̶Ȼ���̶����£������� (5)ƫ��(6) [(V2-V1)/1000]*c*2*40*10/W
�����������
�����Ѷȣ���
3��ʵ���� ijNa2CO3��Ʒ�л���һ������Na2SO4 (��������ᾧˮ����ij��ѧ��ȤС��������ַ����ⶨ����Ʒ��Na2CO3�������������Իش��������⡣
����һ���������з������Na2CO3���������Ĝy��
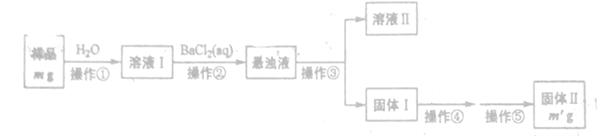
(1)�����ۺܵ͢����Ʒֱ�Ϊ_______��
(2)���������١����У�ʹ�õ�����������______(��������)��
(3)�жϲ����ڷ���ɵķ�����______
��������������ͼʵ��װ�ã��г�������ʡ�ԣ�.ѡ�������Լ�: a.Ũ����b.����NaHCO3��ҺC.6mol/L����D.2mol/L����, e.��ʯ��f. ��ˮCaCl2,�y����Ʒ��Na2CO3,������������
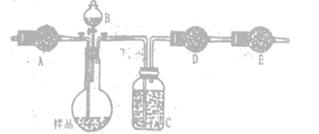
(4)��д���пո�
����
| �Լ�
| ������Լ���Ŀ��
| A
| ?
| �������ʱϴȥCO2
| B
| ?
| ʹ��Ʒ��ַ�Ӧ�ų�����
| C
| a
| ?
| D
| e
| �������CO2
| E
| e
| ?
|
?
�ο��𰸣���1�����ˡ�ϴ�ӣ�2�֣�?��2���٢ۢܣ�2�֣�?��3��ȡ�ϲ���ҹ�ټ����Ȼ�����Һ��������ٲ�����ɫ��������˵���������Ѿ���ɣ���֮û����ɣ�2�֣�
��4����ÿ��2�֣���8�֡�����A��B�е��Լ����Լ�����Ҳ���֣�
����
�Լ�
������Լ���Ŀ��
A
e
?
B
d
?
C
?
��ȥCO2�е�ˮ����
D
?
?
E
?
��ֹ�����е�CO2��ˮ������D�еļ�ʯ������
�����������1���������Һ�з�����IJ����ǹ��ˣ���˲������ǹ��ˡ����˺�õ��Ĺ�����Ҫϴ�Ӻ����������ϴ�ӡ�
��2���ܽ⡢���˺�ϴ�Ӿ���Ҫ�����������Բ����١����У�ʹ�õ����������Т٢ۢܡ�
��3������������Ѿ���ɣ����ټ����Ȼ�����Һ�����������ɫ�����������жϲ����ڷ���ɵ�ʵ�鷽����ȡ�ϲ���ҹ�ټ����Ȼ�����Һ��������ٲ�����ɫ��������˵���������Ѿ���ɣ���֮û����ɡ�
��4��̼�����ܺ��ᷴӦ����CO2�����Կ���ͨ���������ɵ�CO2�������ⶨ̼���ƵĴ��ȡ�Ϊ�˰�װ���е�CO2����ȫ�����գ���Ҫͨ����������������ڿ�����Ҳ����CO2��ˮ����������Aװ����ʢ�ŵ��Ǽ�ʯ�ҡ������ӷ�������Ӧ����ϡ�����̼���Ʒ�Ӧ����Bװ����ʢ�ŵ���ϡ���ᡣ���ɵ�CO2�����к���ˮ������������Ҫ�����ܣ�Ũ����������CO2�е�ˮ���������ɵ�CO2����Ӧ���ü�ʯ�����գ�����Dװ����ʢ�ŵļ�ʯ�ҡ�����Ϊ������Ҳ����CO2��ˮ����������Eװ����Ҳ����ʢ�ż�ʯ�ң��Է�ֹ�����е�CO2��ˮ������D�еļ�ʯ�����ա�
�����Ѷȣ�һ��
4��ʵ���� ��12�֣�Ϊ�ⶨijNa2SO3��Ʒ��������Na2SO4���ʣ��Ĵ��ȣ�ʵ���Ұ����²�����У��ٳ�ȡag��Ʒ�������ձ��У��ڼ�����������ˮ��ʹ��Ʒ�ܽ⣬Ȼ�����Ƴ�250mL��Һ����ȷ��ȡ25.00mL���������õ���Һ��
Ȼ�ɲ����������ַ������вⶨ��
����һ
| ������
| �ܽ�25.00mL��Һ�����ձ��У����������ϡ�����ֽ��裻
�ݼ������BaCl2��Һ����ֽ��裬ʹ������ȫ��
���ˡ�ϴ�ӡ���������������õ�bg���塣
| �ܽ�25.00mL��Һ������ƿ�У�
����0.1 mol/L������KMnO4��Һ���еζ����ﵽ�ζ��յ�ʱ������10.00mL��Һ��
|
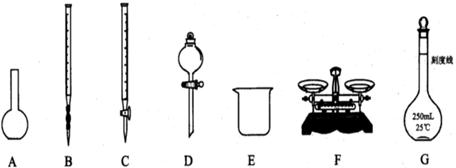
���������ʵ�飬�ش�
��1����ͼ��ʾ�����У���ʵ�鲽��٢ڢ��б����õĵ�������E��?������ĸ����
��2���ڷ���һ���м������ϡ�����Ŀ����?��
��3���ڷ���һ�ⶨ�õ�Na2SO3��Ʒ�Ĵ�����?���г���ʽ���ɲ�����
��4���ڷ������У��Ƿ���Ҫ����ָʾ��?����ǡ��������������?��
��5���ڷ������дﵽ�ζ��յ��ȡ����ʱ������Һ�棬��ⶨ���?
���ƫ�ߡ�����ƫ�͡�������Ӱ�족����
�ο��𰸣���12�֣�ÿ��2�֣���1��B��F��G��ȫ�ԲŸ��֣���
��2����Na2SO3ȫ��ת����SO2����ʹ��Һ�����ԣ��ų�SO32���ĸ��š�
��3��? 1��142b/233a��
��4����KMnO4��������ָʾ������KMnO4��Һ����ʱ����Һ���Ϻ�ɫ��
��5��ƫ�͡�
�����������
�����Ѷȣ�һ��
5��ѡ���� ������Һ��ֱ�����ˮ��ϲ������ú��Ϊ���㣬���㼸��������ɫ����?
A?��ˮ? B?��ϩ? C?��? D?�⻯����Һ
�ο��𰸣�B
�����������
�����Ѷȣ���
|  2)�۲�ζ�����Һ��ĸ߶�ʱӦע�⣺?��?
2)�۲�ζ�����Һ��ĸ߶�ʱӦע�⣺?��?